-
硅、锗(32Ge,熔点 937℃)和镓(31Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
(1)硅在元素周期表中的位置是________。
(2)硅和锗与氯元素都能形成氯化物 RCl4(R代表Si和Ge),从原子结构角度解释原因 _______。
(3)自然界矿石中锗浓度非常低,因此从锗加工废料(含游离态锗)中回收锗是一种非常重要的方法。如图是一种提取锗的流程:
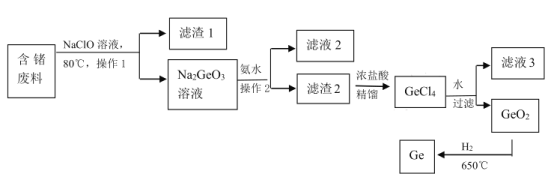
①NaClO 溶液浸取含锗废料中的锗时发生反应的离子方程式为_____;为了加NaClO 溶液浸取含锗废料的速率,可以采取的措施有_____。
②操作 1 和操作 2 是____。
③ GeO2 的熔点为 1086℃,利用氢气还原GeO2,每生成 146kg 的锗放出 akJ 的热量,该反应的热化学方程式为_______。
-
镓(Ga)、锗(Ge)、硅(Si)、硒(Se)的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料,应用于航空航天测控、光纤通讯等领域。回答下列问题:
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为[Ar]_______;与硒同周期的p区元素中第一电离能大于硒的元素有_____种;SeO3的空间构型是_______。
(2)根据元素周期律,原子半径Ga ___As,第一电离能Ga _____As。(填“大于”或“小于”)
(3)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是______,硅与氢结合能形成一系列的二元化合物SiH4、Si2H6等,与氯、溴结合能形成SiCl4 、SiBr4,上述四种物质的沸点由高到低的顺序为__________,丁硅烯(Si4H8)中σ键与π键个数之比为___。
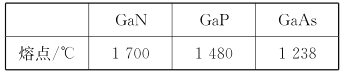
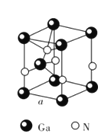
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化原因___。
(5)GaN晶体结构如图所示。已知六棱柱底边边长为a cm,阿伏加德罗常数的值为NA。
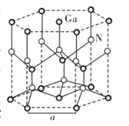
①晶体中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_____。
②从GaN晶体中“分割”出的平行六面体如图所示。若该平行六面体的体积为 cm3,GaN晶体的密度为____g/cm3(用a、NA表示)。
cm3,GaN晶体的密度为____g/cm3(用a、NA表示)。
-
镓(Ga)、锗(Ge)、硅(Si)、硒(Se)的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料,应用于航空航天测控、光纤通讯等领域。回答下列问题:
(1)硒常用作光敏材料,基态硒原子的核外电子排布式为[Ar]_______;与硒同周期的p区元素中第一电离能大于硒的元素有_____种;SeO3的空间构型是_______。
(2)根据元素周期律,原子半径Ga ___As,第一电离能Ga _____As。(填“大于”或“小于”)
(3)水晶的主要成分是二氧化硅,在水晶中硅原子的配位数是______,硅与氢结合能形成一系列的二元化合物SiH4、Si2H6等,与氯、溴结合能形成SiCl4 、SiBr4,上述四种物质的沸点由高到低的顺序为__________,丁硅烯(Si4H8)中σ键与π键个数之比为___。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化原因___。
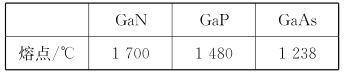
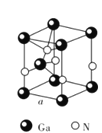
(5)GaN晶体结构如图所示。已知六棱柱底边边长为a cm,阿伏加德罗常数的值为NA。
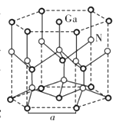
①晶体中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_____。
②从GaN晶体中“分割”出的平行六面体如图所示。若该平行六面体的体积为 cm3,GaN晶体的密度为____g/cm3(用a、NA表示)。
cm3,GaN晶体的密度为____g/cm3(用a、NA表示)。
-
和硅同一主族的锗也是重要的半导体材料,锗应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:

已知:①“碱浸”过程中的反应为:GeO2+2NaOH=Na2GeO3+H2O、As2O3+2NaOH=2NaAsO2+H2O
② GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃。
(1)砷的原子序数为33,砷在元素周期表中的位置为第______周期第________族。
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应的离子方程式为:___________________________________________________________________。
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是_________________。
(4)“蒸馏”过程中的反应的化学方程式为:________________________________。
(5)“水解”操作时保持较低温度有利于提高产率,其最可能的原因是_____________(答一条即可)。
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的较纯二氧化锗产品,则杂质脱除率为_________。
(7)和砷同一主族的锑也可以用于半导体中。一种突破传统电池设计理念的镁—锑液态金属二次电池工作原理如图所示:

该电池由于密度的不同,在重力作用下分为三层,工作时中间层熔融盐的组成不变。充电时,C1-向______(填“上”或“下”)移动;放电时,正极的电极反应式为______。
-
镓(31Ga)、锗(32Ge)都是重要的稀有金属,在化学催化剂、半导体材料、新能源等领域应用广泛,可从锗煤燃烧后的粉煤灰(含 Ga2O3、GeO2、SiO2、Al2O3)中提取, 部分流程如下:
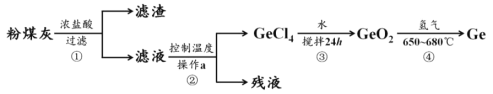
已知:
| 物质 | GaCl3 | GeCl4 | AlCl3 |
| 沸点/℃ | 201 | 84 | 183(升华) |
(1)滤渣的主要成分为_____。
(2)①中发生的反应有 Al2O3+6H+=2Al3++3H2O、Ga2O3+6H+=2Ga3++3H2O 和_____。
(3)操作 a 的名称是_____,②中控制温度的范围是_____(填字母序号)。
a.20~84℃ b.84~183℃ c.84~201℃
(4)④中发生反应的化学方程式是__________________________________________。
(5)镓能与沸水剧烈反应生成氢气,锗在加热条件下与盐酸或稀硫酸不反应。从原子结构角度解释其原因:______________________
(6)用浓盐酸酸化的磷酸三丁酯(TBP)可以从残液中萃取 Ga3+,相关反应为:TBP+GaCl3+HCl TBPH+·GaCl
TBPH+·GaCl 。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:_________________。
。用稀 NaOH 溶液对有机相进行反萃取,用盐酸调节反萃取液 pH 至 5~6,然后升温至 85~95℃水解得到 Ga(OH)3,经后续处理得到粗镓。结合化学用语解释用稀 NaOH 溶液对有机相进行反萃取的原因:_________________。
(7)电解法可以提纯粗镓,具体原理如图所示。镓在阳极溶解生成的 Ga3+与 NaOH 溶液反应生成 GaO ,GaO
,GaO 在阴极放电的电极反应式是_____________________。
在阴极放电的电极反应式是_____________________。
-
镓(Ga)与铝位于同一主族,金属镓的熔点是29. 8℃,沸点是2403℃,是一种广泛用于电子工业和通讯领域的重要金属。
(1)工业上利用镓与NH3在1000℃高温下合成固体半导体材料氮化镓(GaN),同时生成氢气,每生成lmol H2时放出10.27 kJ热量。
写出该反应.的热化学方程式___________________。
(2) 在密闭容器中,充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。
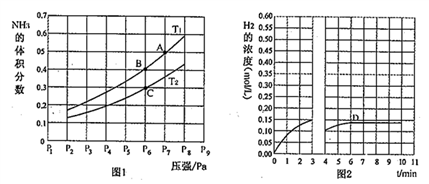
①图1中A点和C点化学平衡常数的大小关系是:KA_____ KC,(填“<”“=”或“>”),理由
是____________。
②在T1和P6条件下反应至3min时达到平衡,此时改变条件并于D点处重新达到平衡,H2的浓度随反应时间的变化趋势如图2所示(3〜4 min的浓度变化未表示出来),则改变的条件为________(仅改变温度或压强中的一种)。
(3)气相平衡中用组份的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),用含P6的式子表示B点的Kp=_____________。
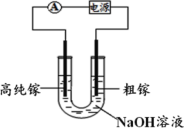
(4)电解精炼法提纯嫁的具体原理如下:以粗镓(含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH溶液为电解质,在电流作用下使粗镓溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+3+2+2+。电解精炼镓时阳极泥的成分是________________。
②镓在阳极溶解生成的Ga3+与.NaOH溶液反应生成GaO2-,该反应的离子方程式为_________________;
GaO2-在阴极放电的电极反应式是________________。
-
[化学——选修3:物质结构与性质]
硒化锌是一种透明色半导体,也可作为红外光学材料,熔点是1 520 ℃。
(1)基态锌原子的价电子排布式是________。
(2)根据元素周期律,电负性Se________S,第一电离能Se________As(填“>”或“<”)。
(3)H2S分子的电子式:________,H2Se分子构型是_______,
其中硒原子的杂化轨道类型是________。
(4)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是________。
(5)晶体Zn为六方最密堆积,其配位数是________。
(6)ZnSe晶胞如图,假设阿伏加德罗常数的值为NA,则144 g ZnSe晶体中的晶胞数是________。

-
Ⅰ. 硒化锌是一种透明半导体,也可作为红外光学材料,熔点是1 520 ℃。
(1)基态锌原子的价电子排布式是_______。
(2)根据元素周期律,电负性Se____S,第一电离能Se____As(填“>”或“<”)。
(3)H2Se的分子构型是____,其中硒原子的杂化轨道类型是____。
(4)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是________________。
(5)晶体Zn为六方最密堆积,其配位数是____。
Ⅱ 氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)C、N、O三种元素第一电离能从大到小的顺序是________。
(2)1 mol N2F2含有____ mol σ键。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含____ mol配位键。
(4)安全气囊打开时发生的化学反应为10NaN3+2KNO3 = K2O+5Na2O+16N2↑。
①写出与N2互为等电子体的分子________。
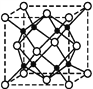
②Na2O的晶胞结构如图所示,晶胞边长为566 pm,晶胞中氧原子的配位数为____,Na2O晶体的密度为______(只要求列算式,不必计算出结果),Na+ 与O2-间的最短距离为_____pm。
-
氮化镓(GaN)是制造LED的重要材料,被誉为“第三代半导体材料”。镓(31Ga)的氧化物和氢氧化物均为两性化合物,工业制备氮化镓的工艺流程如图所示。下列判断正确的是
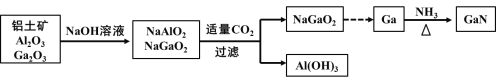
A.Ga位于第五周期第IIIA族 B.酸性:Al(OH)3>Ga(OH)3
C.Ga(OH)3可与NaOH反应生成NaGaO2 D.Ga与NH3反应的另一种生成物可用作航天燃料
-
金属镓(31Ga)是一种广泛应用于电子工业的重要金属,其化学性质与铝相似。
(1)工业上利用Ga与NH3合成固体半导体材料氮化镓(GaN)同时有氢气生成。反应中消耗1molNH3放出15.4kJ的热量。
①该反应的热化学方程式为____________________________;其平衡常数表达式为_____________。
②氮化镓(GaN)性质稳定,但能缓慢的溶解在热的NaOH溶液中,该反应的离子方程式是_________________________。
③0.1mol/L的氨水中加入少量的NH4Cl固体,溶液的pH_________(填“升高”或“降低”);若加入少量明矾,溶液中NH4+的浓度___________(填“增大”或“减小”)。
(2)将一块镓铝合金完全溶于烧碱溶液中得到X溶液。已知:Al(OH)3、Ga(OH)3的酸式电离常数分别为2×10-11、1×10-7,则往X溶液中缓缓通入CO2,最先析出的氢氧化物是______。
(3)工业上以电解精炼法提炼镓的原理如下:以待提纯的粗镓(内含Zn、Fe、Cu杂质)在阳极溶解,通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+2+2+2+,电解精炼镓时阳极泥的成分是_____________。
②GaO2-在阴极放电的电极方程式是________________________。














