-
(12分)甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大。甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍。在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
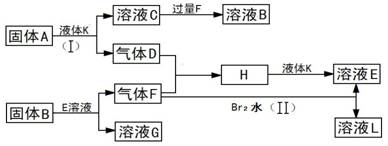
试回答:
(1)甲元素的名称为________,溴元素在周期表的位置________丁元素的阴离子结构示意图为________。
(2)A的电子式为________;所含化学键类型为________。
(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示)________。
(4)反应(I)的化学方程式为________。
(5)反应(II)的离子方程式为。
-
甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大.甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍.在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
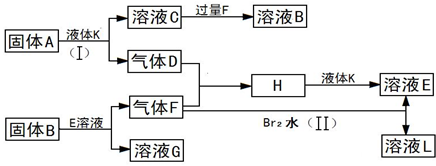
试回答:
(1)甲元素的名称为______,溴元素在周期表的位置______丁元素的阴离子结构示意图为______.
(2)A的电子式为______;所含化学键类型为______.
(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示)______.
(4)反应(I)的化学方程式为______.
(5)反应(II)的离子方程式为______.
-
甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大。甲和乙可形成常见液态化合物K,固体A中含有丙元素的正一价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍。在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
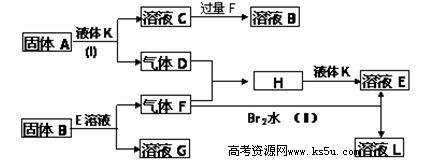
试回答:
(1)A的电子式为________;所含化学键类型为________、________。(各1分)
(2)溴元素在周期表的位置________丁元素的阴离子结构示意图为________。(各2分)
(3)反应(I)的化学方程式为。(2分)
(4)反应(II)的离子方程式为________。(2分)
(5)含1mol C的溶液中缓慢通入15.68 L 的CO2(标况),所得溶液中溶质的物质的量之比为 ________(式量大的比式量小的)
-
甲、乙、丙、丁、戊是五种短周期元素,其原子序数依次增大,它们可以组成下列框图所有物质.甲与乙、丙与乙均可形成原子个数比为2:1和1:1的化合物,丁元素原子的最外层电子数是其电子层数的2倍,框图中溶液M为黄绿色.在一定条件下,下列各物质可发生如图所示的变化.试回答:
(1)戊元素的原子结构示意图为________
(2)A的电子式为________
(3)工业上由F制备H的条件是________
(4)反应(Ⅰ)的离子方程式为________.
(5)反应(Ⅱ)的化学方程式为________.
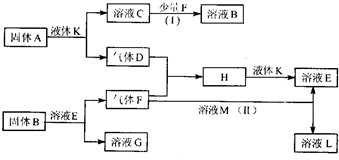
-
 、
、 、
、 、
、 是原子序数依次增大的四种短周期主族元素。已知
是原子序数依次增大的四种短周期主族元素。已知 能形成多种单质,其中两种单质的硬度差异极大;
能形成多种单质,其中两种单质的硬度差异极大; 能形成两种常见的液态二元化合物
能形成两种常见的液态二元化合物 、
、 ,其中
,其中 是生物生存所必需的物质;
是生物生存所必需的物质; 与Y同主族。下列说法错误的是( )。
与Y同主族。下列说法错误的是( )。
A.最高价氧化物对应水化物的酸性:
B. 中只含有共价键
中只含有共价键
C. 、
、 可分别形成两种常见的酸性氧化物
可分别形成两种常见的酸性氧化物
D.简单氢化物的稳定性:
-
A、B、C、D、E为前四周期原子序数依次增大的五种元素。A原子半径是周期表中原子半径最小的;B可以和A形成两种常见的液态化合物甲和乙,且原子个数之比分别是1:1和1:2;C、 D为同周期元素,C是所属周期的主族元素中电负性最小的;D的单质晶体是分子晶体,原子最外层有两个未成对电子;E位于周期表的ds区,E元素原子最外层有一个未成对电子。回答下列问题:
(1)E2+的简化电子排布式是__________;甲和乙沸点较高的是___________(填化学式);
(2)D与B形成常见的具有还原性的阴离子立体构型是三角锥形;则D显最高正价时与B形成的常见化合物的中心原子的杂化类型是_________
(3)同时由A、B、C、D四种元素组成的两种盐M和W,写出这两种盐溶液反应的离子方程式___________
(4)由B、D、E三种元素组成常见盐溶液丙,向丙溶液加入过量NaOH溶液可生成[E(OH)4]2-,不考虑空间构型,[E(OH)4]2-的结构可用示意图表示为__________
(5)根据周期表对角线规则,铍和铝的性质有相似性,则书写铍单质和C的最高正价氧化物对应水化物溶液发生反应的离子方程式是___________________
-
A、B、C、D、E为前四周期原子序数依次增大的五种元素。A原子半径是周期表中原子半径最小的;B可以和A形成两种常见的液态化合物甲和乙,且原子个数之比分别是1:1和1:2;C、 D为同周期元素,C是所属周期的主族元素中电负性最小的;D的单质晶体是分子晶体,原子最外层有两个未成对电子;E位于周期表的ds区,E元素原子最外层有一个未成对电子。回答下列问题:
(1)E2+的简化电子排布式是__________;甲和乙沸点较高的是___________(填化学式);
(2)D与B形成常见的具有还原性的阴离子立体构型是三角锥形;则D显最高正价时与B形成的常见化合物的中心原子的杂化类型是_________
(3)同时由A、B、C、D四种元素组成的两种盐M和W,写出这两种盐溶液反应的离子方程式___________
(4)由B、D、E三种元素组成常见盐溶液丙,向丙溶液加入过量NaOH溶液可生成[E(OH)4]2-,不考虑空间构型,[E(OH)4]2-的结构可用示意图表示为__________
(5)根据周期表对角线规则,铍和铝的性质有相似性,则书写铍单质和C的最高正价氧化物对应水化物溶液发生反应的离子方程式是___________________
-
[化学—选修3:物质结构与性质]
A、B、C、D、E是前四周期原子序数依次增大的五种元素。A元素原子的核外电子等于其电子层数;B元素基态原子有三个能级电子数相同;A和D可形成两种常见液态化合物甲、乙,其原子数之比分别为1:1,2:1;E元素原子的K、L层电子数之和等于其M、N层电子数之和。回答下列问题(涉及元素用相应化学符号表示):
(1)B、C、D三种元素中电负性最大的元素其基态原子的电子排布式为 。
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用 形象化描述。在B的基态原子中,核外存在 对自旋相反的电子。
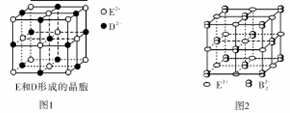
(3)由E和D形成的晶胞如图1所示,晶体中E2+周围等距且最近的E2+有 个;ED的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,焰色反应的原理是 。E和B可形成的晶体的晶胞结构与NaCl晶体的相似(如图2所示),但该晶体中含有的哑铃形B22-的存在,使晶胞沿一个方向拉长。晶体中E2+的配位数为_______________;该化合物的化学式为 。
(4)用高能射线照射液态化合物乙时,一个乙分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干乙分子形成的“网”捕获,乙分子间能形成“网”的原因是 。
②由乙分子释放出电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 。
-
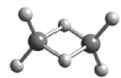
W、X、Y、Z为原子序数依次增大的短周期主族元素,它们分别位于三个不同的周期。常温下,元素W与X可形成两种液态物质;Y、Z两种元素可组成二聚气态分子(如图所示),其中Y原子的最外层电子数等于其电子层数。下列叙述不正确的是( )
A.W与Z具有相同的负化合价
B.四种元素的简单离子半径由大到小的顺序:Z>Y>X>W
C.Y2Z6分子中所有原子的最外层均满足8电子稳定结构
D.工业上可电解X与Y形成的熔融化合物制取Y的单质
-
A、B、C、D为四种短周期元素,A、B、D的原子序数和原子半径均依次增大,B、D同主族且能组成一种能形成“酸雨”的化合物.A、B可以形成A2B和A2B2的两种通常情况下呈液态的共价化合物;B、C形成的两种离子化合物溶于水,所得的溶液均呈强碱性;C的单质常温下可与A2B剧烈反应.试回答下列问题:
(1)B、C两元素以微粒个数比1:1形成的化合物X中,阴、阳离子个数比为________.
(2)在A2B2作用下,铜与稀硫酸制硫酸铜的化学反应的化学方程为:________.
(3)表示形成DB2型“酸雨”的化学反应方程式有多个,请你选择一个合适的反应,写出这个反应的平衡常数表达式K=________.
(4)已知常温下 17gA、D两元素组成的化合物与足量的DB2完全反应时放出热量为a kJ,则该反应的热化学方程式为________.
(5)已知 25℃时,Ksp(CaCO3)=1×10-9.Ksp(CaSO4)=9×10-6.长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率.水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去.
①CaSO4转化为CaCO3的离子方程式为________;
②请分析CaSO4转化为CaCO3的原理________.





