-
我国采用的Cu2O/TiO2–NaBiO3光催化氧化技术能深度净化工业含有机物的废水。回答下列问题:
(1)钛(Ti)的基态原子M能层中能量不同的电子有_____________种。
(2)该技术能有效将含有机物废水中的农药、醇、油等降解为水、二氧化碳、硝酸根离子等小分子。
①H2O、CH3OH、 分子中O-H键的极性最强的是_____________。
分子中O-H键的极性最强的是_____________。
②C、N、O三种元素的电负性由大到小的顺序是_____________。
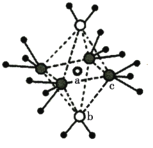
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为深蓝色。深蓝色离子的结构如图所示,lmol该离子中所含σ键为_____________mol(包括配位键);向深蓝色溶液中缓慢加入乙醇,得到深蓝色晶体,加热该晶体先失去组分b的原因是_____________。
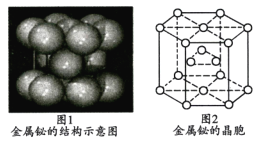
(4)铋合金具有凝固时不收缩的特性,用于铸造高精度铸型。金属铋的结构示意图如图1所示,其晶胞结构如图2所示。若铋原子的半径为rpm,则该晶体的密度为_____________g•cm-3 (用含r和NA数学表达式表示)。
-
(选修3:物质结构与性质)
工业上用合成气(CO和H2)制取乙醇的反应为2CO+4H2 CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
(1)Ti基态原子核外电子排布式为_______。和O同一周期且元素的第一电离能比O大的有_____(填元素符号),和O同一周期且基态原子核外未成对电子数比O多的有____(填元素符号)。
(2)在用合成气制取乙醇反应所涉及的4种物质中,沸点从低到高的顺序为______________。
(3)工业上以CO、O2、NH3为原料,可合成氮肥尿素[CO(NH2)2],CO(NH2)2分子中含有的σ键与π键的数目之比为_________。
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。

①该晶体的化学式为______;其硬度超过金刚石的原因是___________。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加德罗常数,则该晶胞的空间利用率为__________________(用含d、r1、r2、NA的代数式表示)。
-
2015年巴黎气候变化大会召开,旨在保护环境造福人类。下列说法不正确的是
A.扩大铅蓄电池、汞锌锰干电池的生产,满足消费需求
B.采用碳捕集和储存技术,逐步实现二氧化碳的零排放
C.对工业废水、生活污水净化处理,减少污染物的排放
D.催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾
-
2015年巴黎气候变化大会召开,旨在保护环境造福人类。下列说法不正确的是
A.扩大铅蓄电池、汞锌锰干电池的生产,满足消费需求
B.采用碳捕集和储存技术,逐步实现二氧化碳的零排放
C.对工业废水、生活污水净化处理,减少污染物的排放
D.催化处理汽车尾气,减轻氮氧化物污染和光化学烟雾
-
(6分)随着我国工业化水平的不断发展,研究空气污染、废水处理等问题成为重要课题。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
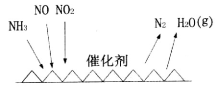
①SCR技术中的氧化剂为____________
②当NO2与NO的物质的量之比为1:l时,与足量氨气在一定条件下发生反应。该反应的化学方程式为_______。当有3 mol电子发生转移时,则参与反应的NO的物质的量为________。
(2)电镀废水中常含有毒的NaCN、HCN等。NaCN水溶液显碱性的原因是_____________(用离子方程式表示);HCN的Ka=6.17×10-10,用NaOH溶液调节含CN-的废水至pH=9,此时废水中c(CN-)_______c(HCN)(填“>”、“<”或“=”)。
(3)室温下有如下数据:草酸(H2C2O4)的K1=5.4×10-2,K2=5.4×10-5;醋酸的电离平衡常数K=1.75×10-5;碳酸的电离平衡常数K1=4.2×10-7,K2=4.5×10-11;Ksp(CaC2O4)=5.0×10-9;Ksp (CaCO3)=2.5×10-9
①用醋酸溶液鉴别CaC2O4和CaCO3两种白色固体的实验现象是___________;
②向0.6 mol·L-1的Na2CO3溶液中加入足量CaC2O4粉末后(忽略溶液体积变化),充分搅拌,发生反应:CO32-(aq)+ CaC2O4 (s) CaCO3 (s)+ C2O42-(aq),静置后沉淀转化达到平衡,此时溶液中的c(C2O42-)(不考虑其他诸如水解之类副反应)为_____________。
CaCO3 (s)+ C2O42-(aq),静置后沉淀转化达到平衡,此时溶液中的c(C2O42-)(不考虑其他诸如水解之类副反应)为_____________。
-
工业上用合成气(CO和H2)制取乙醇的反应为2CO+4H2 CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
(1)Ti基态原子核外电子排布式为_________。和O同一周期且元素的第一电离能比O大的有______(填元素符号),和O同一周期且基态原子核外未成对电子数比O多的有____(填元素符号)。
(2)H2O分子中O原子的价层电子对数是________,CH3CH2OH分子中亚甲基(-CH2-)上的C原子的杂化形式为_______。
(3)在用合成气制取乙醇反应所涉及的4种物质中,沸点从低到高的顺序为_________,原因是__________。
(4)工业上以CO、O2、NH3为原料,可合成氮肥尿素[CO(NH2)2],CO(NH2)2分子中含有的σ键与π键的数目之比为_________。
(5)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。
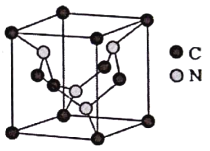
①该晶体硬度超过金刚石的原因是____________。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加德罗常数,则该晶胞的空间利用率为________(用含d、r1、r2、NA的代数式表示)。
-
工业上常采用“电催化氧化—化学沉淀法”对化学镀镍废水进行处理,电解过程中电解槽中H2O、Cl-放电产生·OH、HClO,在活性组分作用下,阴阳两极区发生的反应如下(R表示有机物):
①R+·OH→CO2+H2O
②R+HClO→CO2+H2O+Cl-
③H2PO +2·OH-4e-=PO
+2·OH-4e-=PO +4H+
+4H+
④HPO +·OH-2e-=PO
+·OH-2e-=PO +2H+
+2H+
⑤H2PO +2ClO-=PO
+2ClO-=PO +2H++2Cl-
+2H++2Cl-
⑥HPO +ClO-=PO
+ClO-=PO +H++Cl-
+H++Cl-
⑦Ni2++2e-=Ni
⑧2H++2e-=H2↑
下列说法不正确的是( )
A.·OH、HClO在阳极上产生
B.增大电极电压,电化学氧化速率加快
C.电解时,阴极附近pH逐渐升高,Ni2+去除率逐渐减小
D.向电解后的废水中加入CaCl2可以去除磷元素
-
工业上常采用“电催化氧化—化学沉淀法”对化学镀镍废水进行处理,电解过程中电解槽中H2O、Cl-放电产生·OH、HClO,在活性组分作用下,阴阳两极区发生的反应如下(R表示有机物):
①R+·OH→CO2+H2O
②R+HClO→CO2+H2O+Cl-
③H2PO +2·OH-4e-=PO
+2·OH-4e-=PO +4H+
+4H+
④HPO +·OH-2e-=PO
+·OH-2e-=PO +2H+
+2H+
⑤H2PO +2ClO-=PO
+2ClO-=PO +2H++2Cl-
+2H++2Cl-
⑥HPO +ClO-=PO
+ClO-=PO +H++Cl-
+H++Cl-
⑦Ni2++2e-=Ni
⑧2H++2e-=H2↑
下列说法不正确的是( )
A.·OH、HClO在阳极上产生
B.增大电极电压,电化学氧化速率加快
C.电解时,阴极附近pH逐渐升高,Ni2+去除率逐渐减小
D.向电解后的废水中加入CaCl2可以去除磷元素
-
纳米级TiO2是一种光催化材料,可处理甲醛、氮氧化物等污染物,工业上也可用其催化乙醇脱氢制备乙醛:CH3CH2OH CH3CHO + H2↑。
CH3CHO + H2↑。
(1)Ti原子基态核外电子排布式为____。
(2)CH3CHO分子中碳原子轨道的杂化类型是____,1 mol CH3CHO分子中含有 σ 键的数目为____。
(3)与NO互为等电子体的一种阳离子为____(填化学式)。
(4)乙醇可以与水以任意比互溶,除因为它们都是极性分子外,还因为____。
(5)一种TiO2的晶胞结构如图所示,其中与每个氧原子直接相连的钛原子数目为____。
 。
。
-
钛矿工业中的酸性废水富含Ti、Fe等元素,其综合利用如下:
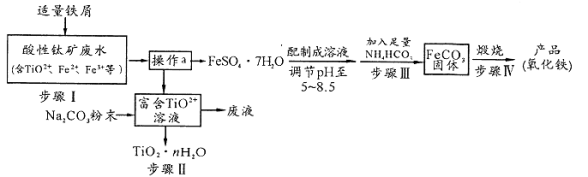
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为
(2)步骤I中检验钛矿废水中加入铁屑是否足量的试剂是 。
(3)操作a是蒸发浓缩、冷却结晶、 。
(4)步骤Ⅲ中发生反应的化学方程式为____________;反应温度一般需控制在35℃以下,其目的是 。
(5)已知 s。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是 。
s。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是 。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末得到固体TiO2·nH2O。请结合原理和化学用语解释其原因 。
分子中O-H键的极性最强的是_____________。





 。
。