-
CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
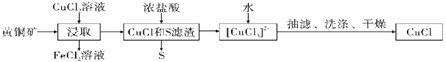
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq) [CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
[CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
A.浸取阶段,参加反应的CuFeS2和CuCl2的物质的量之比为3:l
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s)+2Cl-(aq) [CuCl3]2-(aq)平衡逆向移动,析出CuCl
[CuCl3]2-(aq)平衡逆向移动,析出CuCl
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
-
CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
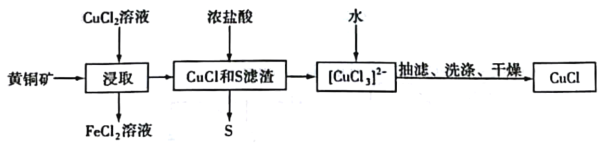
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)⇌[CuCl3]2-(aq)(无色溶液)。下列叙述正确的是
A.“浸取”过程中的主要反应为CuFeS2+4CuCl2=4CuCl+FeCl2+2S
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s) +2Cl-(aq)⇌[CuCl3]2-(aq)平衡逆向移动,析出CuCl,Cl-浓度增大
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
-
CuCl常用作催化剂,石油工业中脱硫与脱色,是一种不溶于水和乙醇的白色粉末,在潮湿空气中可被迅速氧化。某课外学习小组用辉铜矿(主要成分为Cu2S,少量的Fe2O3和SiO2)制取氯化亚铜的流程如下:
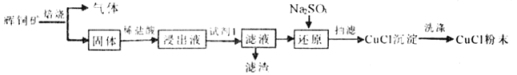
(1)“焙烧”过程发生反应的化学方程式___________;为加快浸取速率常采取的措施___________(写两条)。
(2)加入“试剂1”可调节浸出液的pH,“试剂1”可以是___________;“滤渣”的成分是___________(填化学式)。
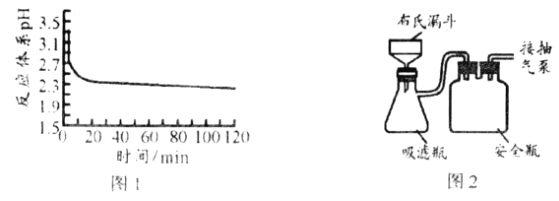
(3)①图1是反应体系pH随时间的变化关系图。写出“还原”制备CuCl的离子方程式___________。
②制备过程中,当n(Na2SO3)与n(CuCl2)比值过大时CuCl产率会变小,其原因可能是_________。
(4)反应完成后经抽滤、洗涤、干燥获得产品。图2为抽滤”装置,抽气泵可使吸滤瓶和安全瓶内压强减小,与普通过滤相比,采用抽滤的优点是___________。
(5)CuCl沉淀的“洗涤”需要经过酸洗、水洗和醇洗。用“去氧水洗后再用“乙醇”洗涤的原因是_______。
(6)取1.0g制备的CuCl粉末样品,先加入足量FeCl3溶液使其完全溶解,再稀释到100mL,从中取出25.00mL,用0.1mol·L-1Ce(SO4)2标准液滴定至终点[Ce(SO4)2被还原为Ce2(SO4)3];三次滴定平消耗标准液的体积为22.00mL。则粉末中CuCl的质量分数为___________。
-
(16分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程如下:
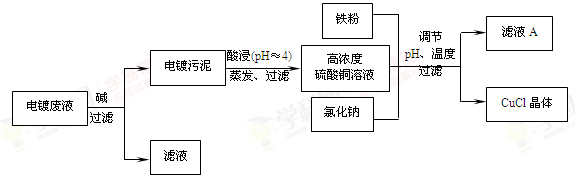
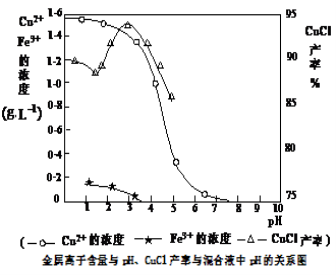
请回答下列问题:
(1)电镀污泥的主要成分是 (写化学式)。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
。
(3)析出CuCl晶体时的最佳pH在 左右。
(4)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是 。
(5)从滤液A中可回收的主要物质是 (写化学式)。
(6)以碳棒为电极电解CuCl2溶液可得到CuCl。写出电解CuCl2溶液后的阴极上发生的反应为
-
(15分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
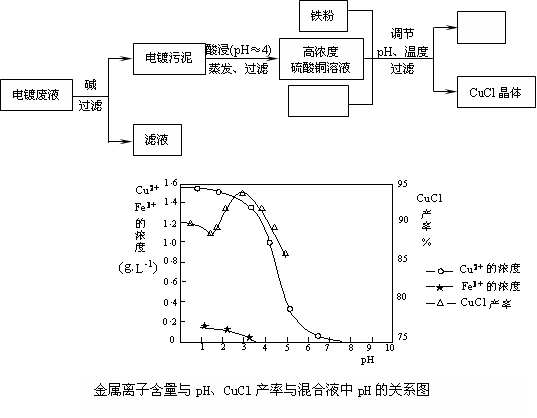
请回答下列问题:
(1)电镀污泥的主要成分是________(写化学式);
(2)酸浸时发生反应的离子方程式是________;
(3)析出CuCl晶体时的最佳pH在________左右;
(4)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
________;
(5)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是________。
-
CuCl常用于有机合成催化剂,并用于颜料、防腐等。工业上以黄铜矿 主要成分是
主要成分是 ,含有少量
,含有少量 为主要原料制备CuCl的主要流程如下:
为主要原料制备CuCl的主要流程如下:
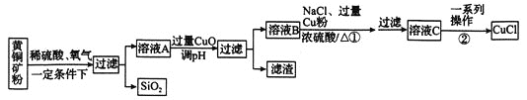
已知:CuCl难溶于水和乙醇,在空气中易被氧化,在水溶液中存在平衡: 白色
白色 无色溶液
无色溶液 。
。
回答下列问题:
 滤渣的主要成分是________
滤渣的主要成分是________ 填化学式
填化学式 。
。
 溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
 ①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
 ②中的一系列操作是________。
②中的一系列操作是________。
 已知:常温下
已知:常温下 ,
, 。若溶液A中
。若溶液A中 ,加入氧化铜
,加入氧化铜 忽略溶液体积变化
忽略溶液体积变化 ,使溶液中
,使溶液中 恰好沉淀完全,此时是否有
恰好沉淀完全,此时是否有 沉淀生成_______
沉淀生成_______ 列式计算
列式计算 。
。 已知:溶液中离子浓度
已知:溶液中离子浓度 时可认为沉淀完全
时可认为沉淀完全 。
。
 工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
-
(16分)CuCl是应用广泛的有机合成催化剂,可采取不同方法制取。
方法一 铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+ 2Cl-  [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。
(1)将废铜板浸入热的H2SO4溶液中,并通入空气,可以生成CuSO4。该反应的离子方程式为 。
(2)①中,“加热”的目的是 ,当观察到 现象,即表明反应已经完全。
(3)②中,加入大量水的作用是 。
(4)潮湿的CuCl在空气中易发生水解和氧化。上述流程中,为防止水解和氧化所添加的试剂或采取的操作是 。
方法二 铜电极电解饱和食盐水(实验装置如图)
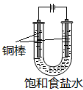
(5)阳极的电极反应式为 。
(6)实验开始时,阳极附近没有产生CuOH沉淀的原因是 。
(已知:Ksp(CuCl)=1.2×10-6,Ksp(CuOH)=1.2×10-14)
-
(16分)
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取。
方法一 铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+ 2Cl-  [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。
(1)将废铜板浸入热的H2SO4溶液中,并通入空气,可以生成CuSO4。该反应的离子方程式为 。
(2)①中,“加热”的目的是 ,当观察到 现象,即表明反应已经完全。
(3)②中,加入大量水的作用是 。
(4)潮湿的CuCl在空气中易发生水解和氧化。上述流程中,为防止水解和氧化所添加的试剂或采取的操作是 。
方法二 铜电极电解饱和食盐水(实验装置如图)
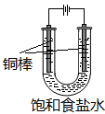
(5)阳极的电极反应式为 。
(6)实验开始时,阳极附近没有产生CuOH沉淀的原因是 。(已知:Ksp(CuCl)=1.2×10-6,Ksp(CuOH)=1.2×10-14)
-
氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇;在空气中迅速被氧化,风光则分解。某实验小组用工业废液(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液,设计流程如:
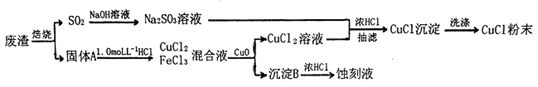
根据以上信息回答下列问题:
(1)固体A的成分为Fe2O3和_________,为提高固体A的溶解速率,可采取的措施是__________(任写一种)。
(2)沉淀B为________,不宜将沉淀剂CaO改为NaOH溶液,其理由是______________________。
(3)在Na2SO3的水溶液中逐滴加入CuCl2的水溶液中,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀,写出该反应的离子方程式________________________ _,CuCl沉淀的洗涤剂应选用_________以减少沉淀的溶解损失,所得CuCl粉末应密封在真空或充有______的避光装置中保存。
(4)熔融态氯化亚铜时快时导电性差,实验测得氯化亚铜蒸汽的相对分子质量为199,则氯化亚铜分子式为_________,属___________(填:共价或离子)化合物。
(5)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式________ _______。
-
有兴趣研究小组用工业废渣(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液。资料显示:氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,通常是一种白色粉末,微溶于水、不溶于乙醇,在潮湿空气中易水解氧化成绿色;见光则分解。
他们设计流程如下:

据此流程和以上信息回答下列问题:
(1)验证焙烧气体产物是SO2的方法______________________________________;溶解固体A对应的化学方程式为_____________________________________。
(2)SO2吸收用NaOH溶液,为得到纯净的Na2SO3溶液,其操作应为_____________________________________________________________________。
(3)在Na2SO3的水溶液中逐滴加入CuCl2溶液,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀.写出该反应的离子方程式______。
(4)CuCl沉淀的洗涤需要经过酸洗、水洗和醇洗,水洗操作为____________________;醇洗不能省略,原因是______。
(5)得到CuCl沉淀要迅速真空干燥、冷却,密封包装。这样操作的目的是_______________________________________________________。
(6)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式_________________。













