-
学校化学兴趣小组利用下列所给试剂,探究不同温度下相同质量的铝与稀盐酸反应速率的影响因素。
(实验试剂)铝条、铝粉、1mol·L—1盐酸、2mol·L—1盐酸
(设计并实验)每次实验盐酸用量均为10mL
实验编号
金属
温度(℃)
盐酸的浓度
均收集50mL所用的时间(s)
①
铝条
25
1mol·L—1盐酸
32.6
②
铝条
25
c(HCl)
18.1
③
铝粉
25
1mol·L—1盐酸
24.3
④
铝粉
100
1mol·L—1盐酸
8.3
(1)铝与稀盐酸反应的离子方程式为________________________。
(2)实验③和④是探究________________对该反应速率的影响。
(3)实验①和②是探究浓度对该反应速率的影响,表中c(HCl)应选取_______mol·L—1。
(4)由表中数据得出结论:_______________________________,反应速率越快。
高二化学实验题中等难度题查看答案及解析
-
贞丰中学化学兴趣小组甲、乙、丙、三名同学探究化学反应速率的影响因素,实验如下。
(1)甲同学探究“温度对化学反应速率的影响”。取两支试管A、B,分别加入25mL 1mol/L 的HNO3溶液和0.5g相同的铜片,将A放在常温下,将B放在60摄氏度的水浴中。观察实验现象:铜片最先完全溶解的是 (填A或B)。据此得出结论 ,温度影响反应速率的本质原因 ,
(2)乙同学取两支试管C、D,各加入4mL0.01mol/LKMnO4酸性溶液,C中加入2mL0.1mol/LH2C2O4溶液,D中加入2mL0.2mol/LH2C2O4溶液,观察到的现象是 ,据此乙同学得出“反应物浓度越大,反应速率越快”的结论。写出KMnO4酸性溶液与H2C2O4溶液反应的离子方程式 ,
(3)丙同学探究0.1mol/L FeCl3溶液对10%的H2O2溶液分解速率的影响,请你为她设计实验。
实验原理: (用化学方程式表示)。
实验操作: 。
高二化学填空题困难题查看答案及解析
-
某实验小组选用CaCO3固体与盐酸的反应来探究化学反应速率的影响因素,下列条件下产生气体速率最快的是
选项
酸的浓度
固体状态
温度
A
1mol/L HCl
块状CaCO3
20℃
B
1mol/L HCl
粉状CaCO3
25℃
C
2 mol/L HCl
块状CaCO3
20℃
D
2 mol/L HCl
粉状CaCO3
25℃
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表:
实 验 步 骤
现 象
结 论
①分别取等体积的2 mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg。
反应快慢:
Mg>Fe>Cu
反应物的性质越活泼,反应速率越快。
(1)该同学的实验目的是 ;
要得出正确的实验结论,还需控制的实验条件是 。
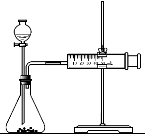
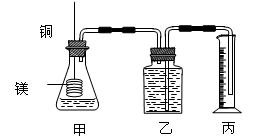
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验可选用的实验药品是 ;
应该测定的实验数据是 。
高二化学填空题中等难度题查看答案及解析
-
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
实 验 步 骤
现 象
结 论
①分别取等体积的2 mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg。反应快慢:
Mg>Fe>Cu反应物的性质越活泼,
反应速率越快。(1)该同学的实验目的是_________________________________________;
要得出正确的实验结论,还需控制的实验条件是_____________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品可以是(从题中所给药品中挑选)_________________________________________________________;
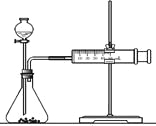
实验二:
已知: 2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_______________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________________。
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水
高二化学实验题中等难度题查看答案及解析
-
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素.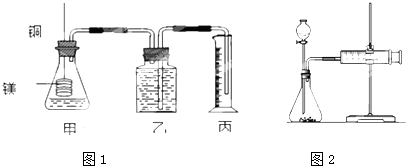
(1)甲同学研究的实验报告如下表:
该同学的实验目的是研究______对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持______相同.实 验 步 骤 现 象 结 论 ①分别取等体积的2mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg.反应快慢:
Mg>Fe>Cu反应物的性质越活泼,反应速率越快.
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图1装置进行定量实验.完成该实验应选用的实验药品是Mg(或Fe)和______ (从给出的药品去选);应该测定的实验数据是______.
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(3)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你的猜想还可能是______的影响.
(4)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是______
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰.高二化学解答题中等难度题查看答案及解析
-
(12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
(1)甲同学研究的实验报告如下表:
①分别取等体积的2 mol/L
硫酸于试管中;
②分别投入大小、形状相同
的Cu、Fe、Mg。
反应快慢:
Mg>Fe>Cu
反应物的性质越活泼,反应速率越快。
该同学的实验目的是研究 ________ 对化学反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持________条件相同。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。
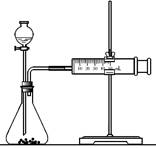
完成该实验应选用的实验药品是________
________;应该测定的实验数据是________。
高二化学实验题简单题查看答案及解析
-
某探究性学习小组拟通过锌与盐酸的反应研究影响反应速率的因素.
该探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如表所示:
实验编号
锌的状态
反应温度/℃
收集100mL氢气所需时间/s
Ⅰ
薄片
15
200
Ⅱ
薄片
25
90
Ⅲ
粉末
25
10
(1)该实验的目的是探究 、 对锌和稀盐酸反应速率的影响;
(2)实验Ⅰ和Ⅱ表明 ,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是 和 ,实验结论是 ;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响: .
高二化学实验题简单题查看答案及解析
-
(8分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
(1)甲同学研究的实验报告如下表:
实 验 步 骤
现 象
结 论
①分别取等体积的2 mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg。
反应快慢:
Mg>Fe>Cu
反应物的性质越活泼,反应速率越快。
该同学的实验目的是研究_____________对反应速率的影响;
根据控制变量法,要得出正确的实验结论,还需控
制的实验条件是保持______条件相同。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品是____;应该测定的实验数据是________________________。

实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和
草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1) 针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_______
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
高二化学实验题简单题查看答案及解析
-
(12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L),设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表:
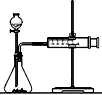
实验步骤
现象
结论
①分别取等体积的2 mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg。
反应快慢:
Mg>Fe>Cu
反应物的性质越活泼,反应速率越快。
(1)甲同学的实验目的是__________________________________________;要得出正确的实验结论,还需控制的主要实验条件是___________________________________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。完成该实验应选用的实验药品是______________________;应该测定的实验数据是_____________________________。
实验二:某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:____________________________________________________________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:____________________________________________________________________。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片纯度、质量、表面积均相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中。
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化。
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中______________________,实验b中________________________,则说明原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
高二化学实验题极难题查看答案及解析