-
草酸合铁(Ⅲ)酸钾晶体{Ka[Fe(C2O4)b]·cH2O}易溶于水,难溶于乙醇,110 ℃可完全失去结晶水,是制备某些铁触媒的主要原料。实验室通过下列方法制备Ka[Fe(C2O4)b]·cH2O并测定其组成:
Ⅰ.草酸合铁酸钾晶体的制备
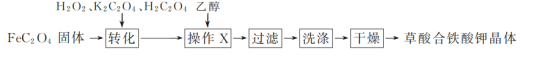
(1)“转化”过程中若条件控制不当,会发生H2O2氧化H2C2O4的副反应,写出该副反应的化学方程式:_________________________。
(2)“操作X”中加入乙醇的目的是_______________________。
Ⅱ. 草酸合铁酸钾组成的测定
步骤1:准确称取两份质量均为0.4910 g的草酸合铁酸钾样品。
步骤2:一份在N2氛围下保持110℃加热至恒重,称得残留固体质量为0.4370 g。
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱,发生反应:aRCl+[Fe(C2O4)b]a-=Ra[Fe(C2O4)b]+aCl-,用蒸馏水冲洗交换柱,收集交换出的Cl-,以K2CrO4为指示剂,用0.1500 mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液20.00 mL。
(3)若步骤3中未用蒸馏水冲洗交换柱,则测得的样品中K+的物质的量________(填“偏大”“偏小”或“不变”)。
(4)通过计算确定草酸合铁酸钾样品的化学式(写出计算过程)。 ________
-
K3[Fe(C2O4)3]· 3H2O(三草酸合铁酸钾晶体)为翠绿色晶体, 溶于水, 难溶于乙醇, 110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。 实验室利用(NH4)2Fe(SO4)2· 6H2O (硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
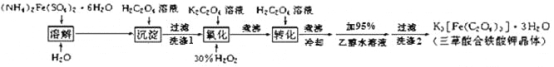
已知:沉淀FeC2O4 · 2H2O 既难溶于水又难溶于强酸
6FeC2O4 + 3H2O2 + 6K2C2O4 = 4K3[Fe(C2O4)3] + 2Fe(OH)3↓
2Fe(OH)3 + 3H2C2O4 + 3K2C2O4 = 2K3[Fe(C2O4)3] + 6H2O
(1)检验硫酸亚铁铵是否变质的试剂是_____;溶解时加几滴稀硫酸的目的是______。
(2)硫酸亚铁铵溶液与 H2C2O4溶液反应生成 FeC2O4 · 2H2O 沉淀,写出该反应方程式_______________;沉淀过滤后,洗涤 1 的操作方法是_______________________________。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2溶液,不断搅拌。此过程需保持温度在 40 ℃ 左右,可能的原因是_______。加入30%过氧化氢溶液完全反应后,煮沸的目的是______________。
(4)洗涤 2 中所用洗涤试剂最合适的是_______(填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
(5)为了不浪费药品,95%乙醇水溶液进行回收的方法是________,所用的主要玻璃仪器有__________(任写两种)等。
-
(15 分)K3[Fe(C2O4)3]· 3H2O(三草酸合铁酸钾晶体)为翠绿色晶体, 溶于水, 难溶于乙醇, 110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。 实验室利用(NH4)2Fe(SO4)2· 6H2O (硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
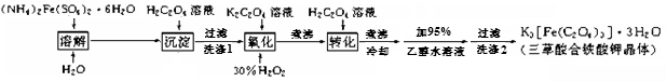
已知:沉淀:FeC2O4 · 2H2O 既难溶于水又难溶于强酸
6FeC2O4 + 3H2O2 + 6K2C2O4 = 4K3[Fe(C2O4)3] + 2Fe(OH)3↓
2Fe(OH)3 + 3H2C2O4 + 3K2C2O4 = 2K3[Fe(C2O4)3] + 6H2O
(1)检验硫酸亚铁铵是否变质的试剂是 ;溶解时加几滴稀硫酸的目的是 。
(2)硫酸亚铁铵溶液与 H2C2O4 溶液反应生成 FeC2O4 · 2H2O 沉淀,写出该反应方程式 ;沉淀过滤后,洗涤 1 的操作方法是 。
(3)在沉淀中加入饱和 K2C2O4 溶液,并用 40 ℃ 左右水浴加热,再向其中慢慢滴加足量的 30% H2O2 溶液,不断搅拌。此过程需保持温度在 40 ℃ 左右,可能的原因是 。加入30%过氧化氢溶液完全反应后,煮沸的目的是 。
(4)洗涤 2 中所用洗涤试剂最合适的是 (填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl 溶液
(5)为了不浪费药品,95%乙醇水溶液进行回收的方法是 ,所用的主要玻璃仪器有 (任写两种)等。
-
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾晶体)为翠绿色晶体,溶于水,难溶于乙醇,110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。
实验室利用(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
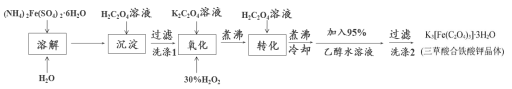
已知:沉淀: FeC2O4·2H2O既难溶于水又难溶于强酸
6FeC2O4+3H2O2+6K2C2O4 4K3[Fe(C2O4)3]+2Fe(OH)3↓
4K3[Fe(C2O4)3]+2Fe(OH)3↓
2Fe(OH)3+3H2C2O4+3K2C2O4 2K3[Fe(C2O4)3]+6H2O
2K3[Fe(C2O4)3]+6H2O
(1)检验硫酸亚铁铵是否变质的试剂是 ;溶解时加几滴稀硫酸的目的是 。
(2)沉淀过滤后,洗涤1的操作方法是 。
(3)在沉淀中加入饱和K2C2O4溶液,并用40 ℃ 左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40 ℃ 左右,可能的原因是 。加入30%过氧化氢溶液完全反应后,煮沸的目的是 。
(4)洗涤2中所用洗涤试剂最合适的是 (填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
-
三草酸合-铁(III)酸钾K3 [Fe(C2O4)3]·3H2O (Mr=491)为绿色晶体,易溶于水,难溶于乙醇等有机溶剂。110℃下可失去结晶水,230℃时即分解,是制备负载型活性铁催化剂的主要原料。以硫酸亚铁铵为原料制备三草酸合铁(III)酸钾晶体的流程如下所示:
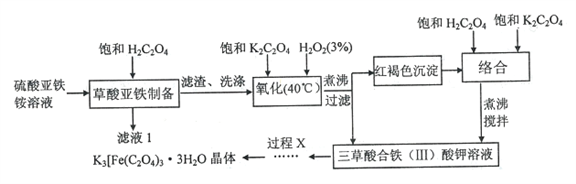
请回答下列问题:
(1)实验室中也可用Fe3+盐代替硫酸亚铁铵来制备该晶体,需先用碱液沉淀Fe3+,若用同浓度的NaOH溶液或氨水通过相同操作来沉淀,选择______能获得颗粒较大的Fe(OH)3。
(2)氧化过程中采用水浴加热,控制最佳温度为40℃,理由是_______,发生反应的化学方程式为_______。氧化完全后需将所得溶液煮沸,目的是__________________。
(3)关于过程X的下列说法中不正确的是________________。
A.可采用冷却和向溶液中加入乙醇的方法促使晶体析出
B.为了快速得到较干燥的固体,可以采用抽滤的方法
C.洗涤晶体时,可先用少量水洗,再用乙醇洗
D.可用加热烘干的方法得到较干燥的晶体
(4)为了分析产品纯度,进行如下操作:
准确称取产品0.9350g,配制成250mL溶液。每次移取25.00mL置于锥形瓶中,加入足量稀H2SO4酸化,将C2O42-转化为H2C2O4,用0.0100mol/LKMnO4溶液滴定至终点,现象是_______。平行测定三次,消耗KMnO4的体积分别为20.02mL,19.98mL,20.00mL,则所得粗产品的纯度为_________________。(已知:5 H2C2O4+2 MnO4-+6H+=10CO2↑+2Mn2++8H2O)
-
三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·3H2O}易溶于水,难溶于乙醇,可用于摄影和蓝色印刷。三草酸合铁酸钾晶体在110 ℃可完全失去结晶水,继续升高温度可发生分解反应。

(1)分解得到的气体产物用如下装置进行实验:
检查装置气密性后,先通一段时间的N2,其目的是________________;结束实验时,先熄灭酒精灯再通入N2至常温。实验过程中观察到B、F中澄清石灰水都变浑浊,E中有红色固体生成,则分解得到的气体产物是________。
(2)分解得到的固体产物含有K2CO3、FeO、Fe,加水溶解、过滤、洗涤、干燥,得到含铁样品。现设计下列两种实验方案对该样品进行铁元素含量测定:
(甲)a g样品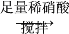 溶液
溶液
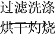 得固体b g
得固体b g
(乙)a g样品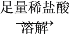 配制250 mL溶液
配制250 mL溶液 三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL。
三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL。
你认为以上________(填“甲”或“乙”)方案可确定样品的组成,测得铁元素的含量是________,不可确定样品组成的方案的理由是____________。
-
三草酸合铁酸钾是一种重要的光敏材料和有机反应的催化剂,化学式为K3[Fe(C2O4)3]·3H2O,为翠绿色晶体,溶于水,难溶于乙醇。110℃下失去三分子结晶水,230℃时分解。该配合物对光敏感,光照下即发生分解。
Ⅰ、三草酸合铁酸钾的制备
①溶【解析】
在托盘天平上称取4.0gFeSO4·7H2O晶体,放入250mL烧杯中,加入1 mol·L-1 H2SO4 1mL,再加入H2O 15mL,加热使其溶解。
②沉淀:在上述溶液中加入1 mol·L-1 H2C2O4 20mL,搅拌并加热煮沸,使形成FeC2O4·2H2O黄色沉淀,用倾斜法倒出清液,洗涤该沉淀3次以除去可溶性杂质。
③氧化:在上述沉淀中加入10 mL饱和K2C2O4溶液,水浴加热至40℃,滴加3%H2O2溶液20mL,不断搅拌溶液并维持温度在40℃左右,使Fe2+充分氧化为Fe3+。滴加完后,加热溶液至沸腾以除去过量的H2O2。
④生成配合物:保持上述沉淀近沸状态,趁热滴加1 mol·L-11H2C2O4使沉淀溶解至呈现翠绿色为止。冷却后,加入15mL 95%的乙醇水溶液,在暗处放置,结晶。减压过滤,抽干后用少量乙醇洗涤产品,继续抽干,称量,计算产率,并将晶体放在干燥器内避光保存。
Ⅱ、产物中C2O42-的质量分数的测定
称取0.20g产品于锥形瓶中微热溶解并加入2 mL稀硫酸,趁热用0.0200 mol·L-1 KMnO4标准溶液滴定至终点,重复操作2-3次,平均消耗KMnO4溶液的体积为25.00mL。计算产物中C2O42-的质量分数。 请回答下列问题:
(1)步骤①溶解时应加入少量的稀硫酸,目的是__________________________;
(2)步骤③用过氧化氢作氧化剂而不选择KMnO4的理由是_______________________;
(3)生成的FeC2O4·2H2O晶体上易沾附硫酸盐,如何证明晶体已洗涤干净______________;
(4)步骤③需保持恒温40℃,原因是__________________________;
(5)用乙醇洗涤的作用是______________________________________________________;
(6)滴定终点的现象是_____________________________________,通过计算,产物中C2O42-的质量分数为____________________。
-
三草酸合铁(III)酸钾K3[Fe
(C
2O4)3]•3H2O(其相对分子质量为491),为绿色晶体,易溶于水,难溶于酒精。110℃下可完全失去结晶水,230℃时分解。它还具有光敏性,光照下即发生分解,是制备活性铁催化剂的原料。某化学小组制备该晶体,并测定其中铁的含量,进行如下实验:
Ⅰ.三草酸合铁(Ⅲ)酸钾的制备;
①称取5g硫酸亚铁固体,放入到100mL的烧杯中,然后加15mL馏水和5~6滴稀硫酸,加热溶解后,再加入25mL饱和草酸溶液,搅拌加热至沸。停止加热,静置,待析出固体后,抽滤、洗涤、干燥,得到FeC2O4•2H2O;
②向草酸亚铁固体中加入饱和K2C2O4溶液10mL,40oC水浴加热,边搅拌边缓慢滴加20mL3%H2O2溶液,变为深棕色,检验Fe2+是否完全转化为Fe3+,若氧化不完全,再补加适量的H2O2溶液;
③将溶液加热至沸,然后加入20mL饱和草酸溶液,沉淀立即溶解,溶液转为绿色。趁热抽滤,滤液转入100mL烧杯中,加入95%乙醇25mL,混匀后冷却,可以看到烧杯底部有晶体析出。晶体完全析出后,抽滤,用乙醇-丙酮混合液洗涤,置于暗处晾干即可。
(1)写出步骤①中,生成FeC2O4•2H2O晶体的化学方程式___。检验FeC2O4•2H2O晶体是否洗涤干净的方法是___。
(2)步骤②中检验Fe2+是否完全转化的操作为___。
(3)步骤③用乙醇-丙酮混合液洗涤,而不是用蒸馏水洗涤的原因是___。
Ⅱ.铁含量的测定:
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化,MnO4-被还原成Mn2+,向反应后的溶液中逐渐加入锌粉,加热至黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤三:用0.0100mol/LKMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+。
步骤四:重复步骤二、步骤三操作,滴定消耗0.0100mol/LKMnO4溶液19.98mL。
(4)配制三草酸合铁酸钾溶液中用到的玻璃仪器有烧杯____,___,___。
(5)写出步骤三中发生反应的离子方程式____。
(6)实验测得该晶体中铁的质量分数为____(结果保留3位有效数字)。
-
(12分)某兴趣小组拟制备K3[Fe(C2O4)3]·3H2O晶体
Ⅰ.查阅资料
K3[Fe(C2O4)3]·3H2O是翠绿色晶体,易溶于水,难溶于乙醇,具有光敏性,光照分解。
110℃失去结晶水,230℃时分解。K3[Fe(C2O4)3]·3H2O的摩尔质量是491g/moL
Ⅱ.制备产品
实验步骤如下:
① 取27.8gFeSO4·7H2O和K2C2O4反应生成草酸亚铁
② 将草酸亚铁(FeC2O4)和适量K2C2O4的混合溶液置于40℃的恒温水浴中,逐滴加入 6% H2O2,边加边搅拌,使Fe2+充分被氧化。反应体系中生成K3[Fe(C2O4)3]的同时还有部分Fe(OH)3沉淀
③ 向②所得浊液中加入1mol/LH2C2O4溶液,使溶液变为翠绿色
④ 加热浓缩,冷却结晶,过滤,洗涤,干燥,称量产品的质量为ag
请回答下列问题:
(1)第②步需要控制水浴40℃,温度不能太高的主要目的: ,若第④步冷却时间较长,需将溶液置于冷暗处,原因是: 。
(2)第②步中,为检验Fe2+是否已完全被氧化,可选用 。试剂(填字母)
A.NaOH溶液 B.K3Fe(CN)6溶液 C.苯酚溶液 D.KSCN溶液
(3)请写出第③步中加入H2C2O4溶液将Fe(OH)3沉淀反应生成K3[Fe(C2O4)3]的化学反应方程式: 。
(4)步骤④中的实验操作需要下列仪器中的 (填仪器的编号).
①酒精灯 ②燃烧匙 ③烧杯 ④广口瓶 ⑤研钵 ⑥玻璃棒
(5)有同学为提高产率,避免第④步加热浓缩过程中K3[Fe(C2O4)3]的少量分解,依据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入 ,过滤,洗涤,干燥,称量。
-
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤一:称量5.40g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入适量锌粉使Fe3+全部转化为Fe2+,同时有气泡产生,过滤,洗涤,将过滤及洗涤所得溶液A收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定溶液A至终点,消耗KMnO4溶液21.98ml,反应中MnO4-被还原成Mn2+ 。
重复步骤二、步骤三操作,消耗0.010mol/L KMnO4溶液22.02ml。
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作依次是:称量、溶解、冷却、转移、洗涤、________、摇匀。
②“步骤一”所得溶液的颜色为________。
③写出“步骤二”中加锌粉产生气泡的离子方程式________;
写出“步骤二”中Fe3+转化为Fe2+的离子方程式________。
④“步骤三”KMnO4溶液应装在________式滴定管中;检查该滴定管不漏水,用水洗净后,装入KMnO4标准溶液前,要对该滴定管进行的操作是________ ________ ________;
判断滴定至终点依据的现象是________ ________。
⑤实验测得该晶体中铁的质量分数为________。






 溶液
溶液 得固体b g
得固体b g 配制250 mL溶液
配制250 mL溶液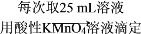 三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL。
三次平均消耗0.1 mol·L-1酸性KMnO4溶液V mL。