-
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(前四周期的元素),对比中学常见元素周期表,思考扇形元素周期表的填充对吕,并回答下列问题:
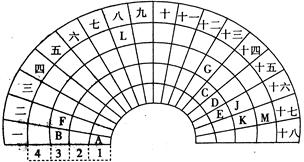
(1)E代表的元素处于常见周期表的位置是 。G的离子结构示意图 。
(2)CE2的电子式是 ,用电子式表示FM2的形成过程。
(3)元素A和M形成的化合物的水溶液与元素K的单质反应的离子方程式为: 。反应后,向溶液中加入CK4溶剂,震荡后现象为 。
(4)B、F、L三种元素最高价氧化物对应的水化物碱性最强的是 (填化学式);比较元素E、K的非金属性强弱,E的非金属性 于K(填“强”或“弱”)。并用化学方程式证明上述结论 。
高一化学填空题中等难度题查看答案及解析
-
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1-36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
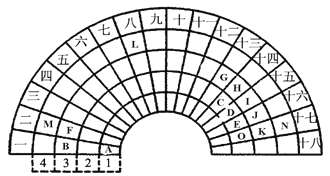
(1) D代表的元素处于常见元素周期表的位置是第 _____ 周期________ 族。
(2)元素F、G、I、K、M的原子半径由大到小的顺序是___________________(用元素符号表示)。
(3)B、F、G三种元素三种元素最高价氧化物对应水化物碱性最强的碱是_________(填化学式)。
高一化学填空题中等难度题查看答案及解析
-
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
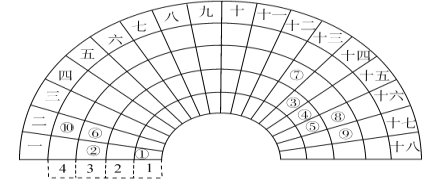
(1)若①~⑩分别代表十种元素,则⑩代表的元素处于常见周期表的位置是_______________________;
(2)⑥⑦为生活中两种常见的金属,其最高价氧化物对应水化物的碱性:⑥____⑦(填>、<或=);比较元素⑧⑨对应的常见单质氧化性的强弱,并用化学方程式证明:____________________________________;
(3)①③⑤三种元素形成的18电子结构化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②最高价氧化物对应的水化物作为电解质的燃料电池的负极反应式:___________________________;
(4)用电子式表示④的一种10电子结构氢化物的形成过程:_________________________。
高一化学推断题中等难度题查看答案及解析
-
(7分)
元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。
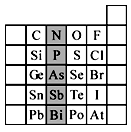
(1)阴影部分元素N在元素周期表中的位置为________周期________族 。 根据元素周期律,预测:酸性强弱 H3AsO4 ________H3PO4。(用“>”或“<”表示)
(2)元素Se的最高正价和最低负价的代数和为____________; 在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度________ 。(选填“更大”、“更小”或“相同”);
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是_____________。
(4)下列说法不正确的是________。
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
高一化学填空题中等难度题查看答案及解析
-
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
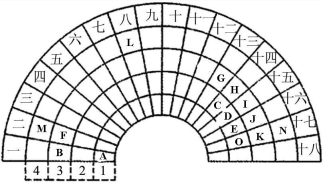
(1)L代表的元素处于常见周期表的位置是 ,该单质与A2E反应的方程式为: 。
(2)元素F、G、I、K、M的原子半径由大到小的顺序是 ,其对应离子的离子半径由大到小的顺序是 (用元素或离子符号表示)。
(3)用电子式表示MO2: 、用电子式表示CJ2的形成过程:
(4)F、G、M三种元素最高价氧化物对应的水化物碱性最强的是 (填化学式);比较元素C和J的非金属性强弱,C的非金属性 于J(填“强”或“弱”),并用化学方程式证明上述结论 。
(5)元素B和N形成的化合物的水溶液与元素K的单质反应的离子方程式为: ,反应后,向溶液中加入C、K形成的化合物溶液,现象为 。
(6)A与E和A与J均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为 。
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
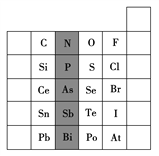
(1)阴影部分元素N在元素周期表中的位置为____周期第____族。根据元素周期律,预测酸性强弱:H3AsO4____H3PO4(填“>”或“<”)。
(2)S的最高化合价和最低化合价的代数和为____,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度____(填“更大”“更小”或“相同”)。
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是____。
(4)下列说法错误的是____(填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③干冰升华、液态水转变为气态水都要克服分子内的共价键
④HF、HCl、HBr、HI的热稳定性依次减弱
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
(1)阴影部分元素N在元素周期表中的位置为第______周期第______族.
根据元素周期律,预测:酸性强弱 H3AsO4______H3PO4.(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度______.(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是______.
(4)下列说法正确的是______
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.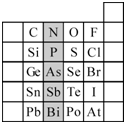
高一化学解答题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
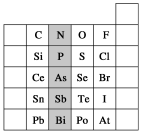
(1)阴影部分元素N在元素周期表中的位置为________周期________族。根据元素周期律,预测酸性强弱:H3AsO4________H3PO4(填“>”或“<”)。
(2)元素S的最高化合价和最低化合价的代数和为________,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度________(填“更大”、“更小”或“相同”)。
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是__________________。
(4)下列说法错误的是________。
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态水都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
高一化学填空题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
(1)阴影部分元素N在元素周期表中的位置为第______周期第______族.
根据元素周期律,预测:酸性强弱 H3AsO4______H3PO4.(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为______,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度______.(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是______.
(4)下列说法正确的是______
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱.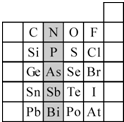
高一化学解答题中等难度题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质,如图是元素 周期表的一部分:
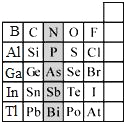
(1)阴影部分元素N在元素周期表中的位置为第_______周期第_______族。根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4__________H3PO4(填 “>”“<”或“=”)。
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_______族。
(3)元素甲是第三周期金属元素中原子半径最小的元素,该元素的离子与过量氨水反应的离子方程式为:_____。
(4)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用,已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为______。
A.硫 B.砷 C.硒 D.硅
高一化学填空题中等难度题查看答案及解析