在酸性条件下,黄铁矿( FeS2)催化氧化的反应方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+,实现该反应的物质间转化如图所示。下列分析错误的是
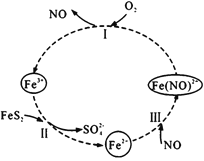
A.反应I的离子方程式为4Fe(NO)2++O2+4H+= 4Fe3++4NO+2H2O
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ш是氧化还原反应
D.黄铁矿催化氧化中NO作催化剂
高二化学单选题中等难度题
在酸性条件下,黄铁矿( FeS2)催化氧化的反应方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+,实现该反应的物质间转化如图所示。下列分析错误的是

A.反应I的离子方程式为4Fe(NO)2++O2+4H+= 4Fe3++4NO+2H2O
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ш是氧化还原反应
D.黄铁矿催化氧化中NO作催化剂
高二化学单选题中等难度题
在酸性条件下,黄铁矿( FeS2)催化氧化的反应方程式为2FeS2+7O2+2H2O=2Fe2++4SO42-+4H+,实现该反应的物质间转化如图所示。下列分析错误的是

A.反应I的离子方程式为4Fe(NO)2++O2+4H+= 4Fe3++4NO+2H2O
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ш是氧化还原反应
D.黄铁矿催化氧化中NO作催化剂
高二化学单选题中等难度题查看答案及解析
不能正确表示下列变化的离子方程式是
A.二氧化硫与酸性高锰酸钾溶液反应:5SO2+2H2O+2MnO4-===2Mn2++5SO42-+4H+
B.FeCl3溶液腐蚀铜板:2Fe3++Cu===2Fe2++Cu2+
C.苯酚钠溶液中通入少量CO2:2+CO2+H2O====2
+CO32-
D.酸性碘化钾溶液中滴加适量双氧水:2I−+2H++H2O2===I2+2H2O
高二化学单选题中等难度题查看答案及解析
下列离子方程式错误的是
A.铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42-
B.酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2 +6H+═2Mn2++5O2↑+8H2O
C.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
D.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓
高二化学选择题简单题查看答案及解析
下列离子方程式正确的是
A.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
B.二氧化硫与酸性高锰酸钾溶液反应:5SO2+2H2O+2MnO4-=2Mn2++5SO42-+4H+
C. Na2S2O3溶液与稀H2SO4反应的离子方程式:S2O32-+6H+=2S↓+3H2O
D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe=2Fe3++3Cu
高二化学单选题中等难度题查看答案及解析
在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是( )
A.2Fe3++SO2+2H2O===2Fe2++SO42-+4H+
B.2Fe2++Cl2===2Fe3++2Cl-
C.2Br-+4H++SO42-===SO2+Br2+2H2O
D.I2+SO2+2H2O===4H++SO42-+2I-
高二化学选择题简单题查看答案及解析
氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2 + 2H2O-2e-→SO42- + 4H+;(2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:Cl2+2e-→2Cl-。在(1)和(2)反应中均会生成产物X,则X的化学式为
A.NaClO B.ClO2 C.HClO D.NaClO4
高二化学选择题简单题查看答案及解析
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
SO2+2Fe3++ 2H2O=SO42-+2Fe2++4H+;
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
则:()
A. 还原性Cr3+>Fe2+>SO2
B. 氧化性Cr2O72->SO2>Fe3+
C. Cr2O72-能将 Na2SO3 氧化成 Na2SO4
D. 两个反应中Fe2(SO4)3均作还原剂
高二化学单选题中等难度题查看答案及解析
为探究酸性条件下KI溶液被空气氧化的快慢(已知反应4I-+O2+4H+=2I2+2H2O),设计下列方案。其中不可行的是
| 选项 | 实验Ⅰ | 实验Ⅱ | ||
| 温度 | 试剂加入顺序 | 温度 | 试剂加入顺序 | |
| A | 20℃ | 淀粉、稀硫酸、KI | 20℃ | 淀粉、KI、稀硫酸 |
| B | 25℃ | KI、稀硫酸、淀粉 | 35℃ | 稀硫酸、KI、淀粉 |
| C | 30℃ | 淀粉、KI、稀硫酸 | 35℃ | 淀粉、KI、稀硫酸 |
| D | 35℃ | KI、淀粉、稀硫酸 | 30℃ | KI、淀粉、稀硫酸 |
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
(10分)许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同条件下发生的还原反应如下:
①酸性:MnO4-+5e-+8H+→Mn2++4H2O;
②中性:MnO4-+3e-+2H2O→MnO2+4OH-
③碱性:MnO4-+e-→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e-→Mn2++2H2O
(1)MnO2与稀盐酸不能制取氯气,其原因是___________________________________。
(2)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是_______。(选填编号)
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(3)写出将SO2通入KMnO4溶液中所发生反应的离子方程式,并配平:
________________________________________________________________________。
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,已知产物中K2SO4和S的物质的量之比为3∶2。完成并配平该反应的化学方程式:
□KMnO4+□K2S+□__________→□K2MnO4+□K2SO4+□S↓+□__________,反应若生成5.44 g硫单质,反应过程中转移电子的物质的量为__________________。
高二化学填空题困难题查看答案及解析
下列离子方程式书写正确的是( )
A.在100 mL浓度为1 mol•L﹣1的 Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42﹣+4H+
B.在100 mL浓度为2 mol•L﹣1的FeI2的溶液中通入标准状况下5.6 L的Cl2:4Fe2++6I﹣+5Cl2═4Fe3++3I2+10Cl﹣
C.向NaHCO3溶液中加入过量的澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣
D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O
高二化学选择题简单题查看答案及解析