飞秒(1fs=10-15s)化学广泛应用于化学研究。大多双分子反应难于确定反应历程,Zewail通过研究HI与CO2反应巧妙的解决了这个问题,其反应过程中的片断: (1ps=1000fs)。下列说法不正确的是
(1ps=1000fs)。下列说法不正确的是
A.反应过程中CO2未全部断键而HI全部断键
B.HOCO是HI与CO2双分子反应的过渡态产物
C.观察到HOCO解离需用1ps,说明HI与CO2反应极快
D.该反应的起点是HI的解离,终点是OH自由基与I自由基的结合
高三化学单选题中等难度题
飞秒(1fs=10-15s)化学广泛应用于化学研究。大多双分子反应难于确定反应历程,Zewail通过研究HI与CO2反应巧妙的解决了这个问题,其反应过程中的片断: (1ps=1000fs)。下列说法不正确的是
(1ps=1000fs)。下列说法不正确的是
A.反应过程中CO2未全部断键而HI全部断键
B.HOCO是HI与CO2双分子反应的过渡态产物
C.观察到HOCO解离需用1ps,说明HI与CO2反应极快
D.该反应的起点是HI的解离,终点是OH自由基与I自由基的结合
高三化学单选题中等难度题
飞秒(1fs=10-15s)化学广泛应用于化学研究。大多双分子反应难于确定反应历程,Zewail通过研究HI与CO2反应巧妙的解决了这个问题,其反应过程中的片断: (1ps=1000fs)。下列说法不正确的是
(1ps=1000fs)。下列说法不正确的是
A.反应过程中CO2未全部断键而HI全部断键
B.HOCO是HI与CO2双分子反应的过渡态产物
C.观察到HOCO解离需用1ps,说明HI与CO2反应极快
D.该反应的起点是HI的解离,终点是OH自由基与I自由基的结合
高三化学单选题中等难度题查看答案及解析
“飞秒(10-15s)化学”使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为利用该技术不能观察的是( )
A.原子中原子核的内部结构
B.化学反应中原子的运动
C.化学反应中生成物分子的形成
D.化学反应中反应物分子的分解
高三化学选择题简单题查看答案及解析
1999年度诺贝尔化学奖获得者艾哈迈德·泽维尔,开创了“飞秒(10-15s)化学”的新领域,使用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为该技术不可能观察到的是 ( )
A.化学变化中反应物分子的分解 B.原子核内部微粒的运动
C.化学变化中生成物分子的形成 D.化学反应中原子的运动
高三化学选择题简单题查看答案及解析
大多数天然元素存在几种稳定的同位素。许多同位素有重要的用途,例如是作为确定原子量标准的原子;
、
是制造氢弹的材料;
是制造原子弹的材料和核反应堆的原料。同位素示踪法广泛应用于科学研究、工农业生产和医疗技术方面,例如用
标记化合物确证了酯化反应的历程,
用于甲状腺吸碘机能的实验等。下列说法中正确的是
A. 、
互为同位素
B.分子是保持物质化学性质的唯一微粒
C.同种元素的各种同位素原子的质量不同,但化学性质几乎相同
D.题干中涉及了五种具体的核素
高三化学选择题简单题查看答案及解析
(16分)碳和碳的化合物在生产生活实际中应用广泛。运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7 ,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式________;
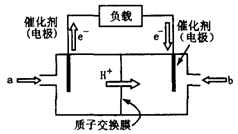
(2)上图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示意图。电池总反应为2CH3OH+3O22CO2+4H2O。该装置放电时________(填“a”或“b”)为电池的负极,其电极反应式为________;
(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置。
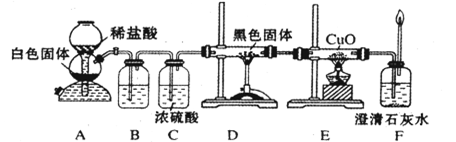
已知:C + H2OCO+H2 CO + H2O
CO2 + H2 C + CO2
2CO
试回答下列问题:
① 装置B中最适宜的试剂是________,必须用装置C吸收气体中的水蒸气的理由是;
② 根据该实验中的________现象,可证明CO具有还原性;
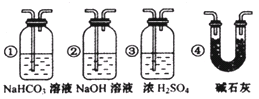
③ 若要根据装置F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置________与________之间(填字母标号)连接下图中的________装置(选填序号)。
高三化学实验题中等难度题查看答案及解析
诺贝尔奖获得者艾哈迈德·泽维尔研究了氰化碘的分解反应2ICN====I2+(CN)2,他发现此反应在200飞秒(1飞秒=10-15秒)内完成,氰被称为类卤素,则下列有关ICN的叙述正确的是( )
A.ICN晶体是原子晶体
B.ICN能与NaOH反应
C.ICN是共价化合物
D.ICN在常温常压下为气体
高三化学选择题简单题查看答案及解析
尼龙材料是一种性能优良的工程塑料,目前广泛应用于汽车领域,具有优异的力学性能。以A(C6H10)原料通过氧化反应制备G,再通过缩聚反应合成尼龙,合成路线如下:
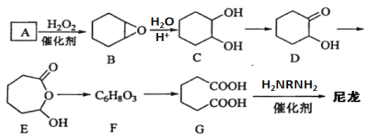
回答下列问题:
(1)A的化学名称为_________________;
(2)B到C的反应类型为_______________;
(3)D中含有的官能团名称是____________;
(4)E的分子式为_____________;
(5)由G合成尼龙的化学方程式为________________________________;
(6)写出一种与C互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积之比为3:1)_____________。
(7)1,4-二溴环己烯()是多数有机合成一种重要的中间体,设计由B为起始原料制备1,4-二溴环己烯的合成路线____________________。
高三化学综合题中等难度题查看答案及解析
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。试回答下列问题:
(1)已知:高炉炼铁过程中会发生如下反应:
①FeO(s)+CO(g)===Fe(s)+CO2(g) ΔH1
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3
则反应Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)的ΔH的表达式为_______________________________(用含ΔH1、ΔH2、ΔH3的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下表:
| 温度/℃ | 250 | 600 | 1000 | 2000 |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600 ℃时固体物质的主要成分为_____________(填化学式);若该温度下,测得固体混合物中m(Fe)∶m(O)=35∶4,则FeO被CO还原为Fe的百分率为______________(设其他固体杂质中不含Fe、O元素)。
(3)铁的某些化合物可用作CO与H2反应的催化剂。已知某种铁的化合物可用来催化反应:CO(g) + 3H2(g) CH4(g) + H2O(g) ΔH <0 。
在T ℃、a MPa时,将2 mol CO和6 mol H2充入某容积可变的密闭容器中,实验测得CO的物质的量在反应体系中所占百分比x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.21 | 0.20 | 0.10 | 0.10 |
① T ℃ a MPa时,此反应的平衡常数K = ____________(保留1位小数)。达到平衡时CO的转化率为___________。

②上图表示该反应CO的平衡转化率与温度、压强的关系。
图中温度T1、T2、T3由低到高的顺序是________________。图中显示其它条件固定时,增加压强会导致平衡向___________(填“左”或“右”)移动。
高三化学填空题困难题查看答案及解析
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。请回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)Fe(s)+CO2(g) K1 ΔH1=a kJ·mol−1
3Fe2O3(s)+CO(g)2Fe3O4(s)+CO2(g) K2 ΔH2=b kJ·mol−1
Fe3O4(s)+CO(g)3FeO(s)+CO2(g) K3 ΔH3=c kJ·mol−1
①Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g) ΔH=_____kJ·mol−1(用含a、b、c的代数式表示)。
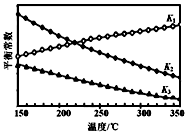
②上述反应对应的平衡常数K1、K2、K3随温度变化的曲线如图所示。则a_________b,(填“>”、“<”或“=”),理由是_________________。
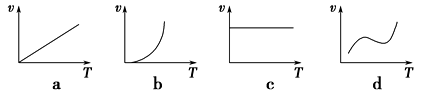
(2)铁的氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。
(3)铁等金属可用作CO与H2反应的催化剂:CO(g)+3H2(g)CH4(g)+H2O(g)
ΔH<0。在T℃,将l mol CO和3 mol H2加入2 L的密闭容器中。实验测得n(CO)随时间的变化如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| n(CO)/mol | 1.0 | 0.70 | 0.45 | 0.25 | 0.10 | 0.10 |
①下列能判断该反应达到平衡的标志是______(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②在0~20 min内v (H2)=______;在T℃时该反应的平衡常数K=_________。
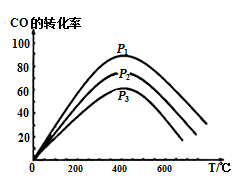
③下图表示该反应中CO的转化率与温度、压强的关系。图中压强P1、P2、P3由高到低的顺序是_________。
高三化学填空题困难题查看答案及解析
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+ CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+1/3 CO(g)═ 2/3 Fe3O4(s)+ 1/3 CO2(g)△H2
Fe3O4(s)+ CO(g)═3Fe(s)+CO2(g)△H3
Fe2O3(s)+ CO(g)═2Fe(s)+3CO2(g)△H4
则△H4 的表达式为_____(用含△H1、△H2、△H3 的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为_____,该温度下若测得固体混合物中 m(Fe):m(O)=35:2, 则 FeO 被 CO 还原为 Fe 的百分率为_________(设其它固体杂质中不含 Fe、O 元素)。
(3)铁等金属可用作 CO 与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g) = CH4(g) +H2O(g)△H<0.在 T℃,106Pa 时将 l mol CO 和 3mol H2 加入体积可变的密闭容器 中.实验测得 CO 的体积分数 x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断 CO(g)+3H2(g)⇌ CH4(g)+H2O(g)达到平衡的是_____(填序号)。
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v 正(CO)=3v 逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时 CO 的转化率为___________;在 T℃106Pa 时该反应的压强平衡常数 Kp(用平衡分 压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为_____。
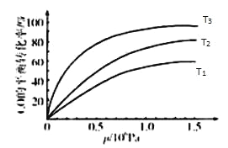
③图表示该反应 CO 的平衡转化率与温度、压强的关系.图中温度 T1、T2、T3 由高到低的顺序是_____,理由是_____________.
高三化学综合题中等难度题查看答案及解析