-
己二酸是重要的有机合成中间体,是重要的化工原料。己二酸的物理常数如表所示:
| 物质 | 色态 | 相对分子质量 | 熔点/℃ | 溶解度(性) |
| g/100mL水 | 乙醇 |
| 己二酸 | 白色晶体 | 146 | 152 | 15℃ | 25℃ | 100℃ | 易溶 |
| 1.4 | 2.3 | 160 |
Ⅰ.制备己二酸的一种反应机理如下:
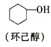 +HNO3(浓)
+HNO3(浓) HOOC(CH2)4COOH+NO2↑+H2O(未配平)
HOOC(CH2)4COOH+NO2↑+H2O(未配平)
制备己二酸的装置如图所示(夹持、加热装置省略)。
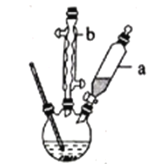
(1)向三颈烧瓶中加入2 mL浓HNO3,再缓慢滴加1 mL环己醇,保持80 ℃持续反应2 h。仪器b的名称是______________,能否用于蒸馏冷凝: ____________(填“能”或“否”)。反应结束冷却至室温后,在冰水浴中冷却,分离出己二酸粗品,用冰水浴的目的是__________
(2)图中装置的缺陷为____________________。
Ⅱ.用浓HNO3做氧化剂的合成方法中,浓HNO3会严重腐蚀设备。科学家改进了合成已二酸的方法,改进后的反应机理如下:

 HOOC(CH2)4COOH
HOOC(CH2)4COOH
(环己烯,难溶于水,易溶于乙醇),使用的装置如图所示(夹持、加热装置省略)。
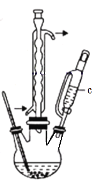
(3)仪器c与a相比较,优点在于___________。
(4)检验己二酸粗产品中含有少量环己烯时的方法_________。
(5)实验结束后,准确称取实验产品0.1500 g于250 mL锥形瓶中,加入50 mL热的蒸馏水,搅拌溶解,滴加几滴酚酞。用0.1000 mol•L-1 NaOH溶液滴定。重复上述操作两次,消耗NaOH的平均体积为20.00 mL。
①滴定终点的现象为__________。
②产品的纯度为______________(保留3位有效数字)。
-
乙酰苯胺是一种具有退热镇痛作用的药物,可用苯胺和冰醋酸为原料来制备乙酰苯胺。
①化学原理为: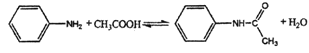 (已知:苯胺易被氧化)
(已知:苯胺易被氧化)
②相关物质的物理常数
| 物质 | 相对分子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度(g) |
| 水 | 乙醇 |
| 苯胺 | 93 | 无色液体 | 6 | 184 | 3.42(20℃) | 任意比混溶 |
| 冰醋酸 | 60 | 无色液体 | 17 | 118 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 白色片状固体 | 114 | 304 | 0.56(20℃)、3.45(50℃)、5.20(100℃) | 36.9(20℃) |
③制各乙酰苯胺的装置如图所示:韦氏分馏柱作用与原理类似于冷凝管。

④制备方法和过程:

(1)仪器a的名称_______。
(2)制备过程中加入锌粒的作用:其一是________、其二是防止暴沸。
(3)从化学平衡的角度分析,步骤1要控制分馏柱上端的温度在105℃左右的原因_____。
(4)步骤2中将反应液倒入冷水中的目的是______。
(5)步骤3中洗涤剂最好选择________。
A.冷水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(6)步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→_____→冷却结晶→过滤→洗涤→干燥。
(7)本实验所得到的乙酰苯胺产率是________。
-
有机合成在制药工业上有着极其重要的地位。现用硝基苯制取苯胺,再用苯胺制得无 色晶体乙酰苯胺(具有退热镇痛作用的药物)。
①化学反应原理为:

②相关物质的物理常数
| 物质 | 相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解度(g) |
| 水 | 乙醇 |
| 苯胺 | 93 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
| 乙酸 | 60 | 17 | 117.9 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 114 | 304 | 0.56(20℃) 3.45(50℃) 5.20(100℃) | 36.9(20℃) |
| | | | | |
③制备乙酰苯胺的装置及过程如下图所示:
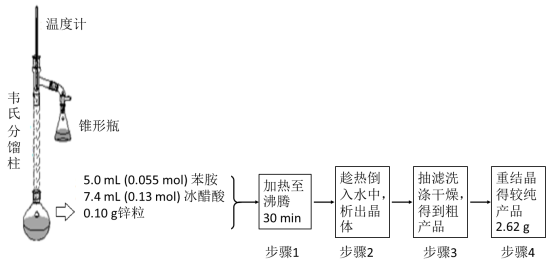
已知:Ⅰ苯胺易被氧化;Ⅱ韦氏分馏柱作用与原理类似于冷凝管
请回答以下问题:
(1)加入锌粒的目的是___________;韦氏分馏柱作用的是_________;
(2)步骤1中保持柱顶温度约为105℃,则锥形瓶中收集到的馏分主要是_____________;
(3)步骤2中将反应液倒入水中的目的是___________;
(4)步骤3中洗涤剂最好选择______________;
A.冷水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(5)步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→________→__________→抽滤→洗涤→干燥;
(6)上述制备过程的产率是____________。(结果保留4位有效数字)。
-
3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 | 
| 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 | 
| 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | 
| 33 ~36 | 
| 易溶于甲醇、乙醚,微溶于水 |
(1)1mol间苯三酚完全燃烧需要______molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是的__________。
②萃取用到的分液漏斗使用前需____________并洗 净,分液时有机层在分液漏斗的______填(“上”或“下”)层。
净,分液时有机层在分液漏斗的______填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是_________________________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____________(填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)反应可能出现的副产物的结构简式为___________________。
-
环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下:
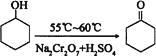
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm—3、20 ℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
现以20mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯。其主要步骤有(未排序):
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分离提纯步骤的正确顺序是 。
(2)b中水层用乙醚萃取的目的是 。
(3)以下关于萃取分液操作的叙述中,不正确的是 。
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图( )用力振荡
)用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分漏斗静置液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞,待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是 。蒸馏除乙醚的操作中,采用的加热方式为 。
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是 。
(6)恢复至室温时,分离得到纯产品体积为12mL,则环己酮的产率约是 (保留两位有效数字)。
-
乙二酸(HOOC—COOH)也称草酸,是一种重要的化工原料和化工产品。利用石油化工产品中的烷烃可以生成草酸,生产流程如下:

已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79。
请回答下列问题:
(1)A的结构简式是_______________ ;D的名称__________________。
(2)写出有关的化学方程式:
B→C:________________________________________________________。
D→E:________________________________________________________。
(3)A生成B的反应类型是__________;C生成D的反应类型是___________。
-
乙二酸(HOOC—COOH)也称草酸,是一种重要的化工原料和化工产品。利用石油化工产品中的烷烃可以生成草酸,生产流程如下:

已知上述框图中有机物B的相对分子质量比有机物A的相对分子质量大79。
请回答下列问题:
(1)A的结构简式是_______________ ;D的名称__________________。
(2)写出有关的化学方程式:
B→C:________________________________________________________。
D→E:________________________________________________________。
(3)A生成B的反应类型是__________;C生成D的反应类型是___________。
-
有机化工中3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 | 
| 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 | 
| 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | 
| 33 ~36 | 
| 易溶于甲醇、乙醚,微溶于水 |
(1)1mol间苯三酚完全燃烧需要_____molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是________。
②萃取用到的分液漏斗分液时有机层在分液漏斗的____填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是__________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_________(填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)写出反应中可能出现的副产物结构简式______________(只要写一种即可)。
-
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:( )

| 物质 | 沸点/℃ | 熔点/℃ | 溶解性 |
| 甲醇 | 64. 7 | ﹣97.8 | 易溶于水 |
| 3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
下列说法正确的是( )
A. 分离出甲醇的操作是结晶 B. 间苯三酚与苯酚互为同系物
C. 上述合成反应属于取代反应 D. 洗涤时可以用饱和Na2CO3溶液除氯化氢
-
[实验化学]
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 | 
| 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 | 
| 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | 
| 33 ~36 | 
| 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的_________。
②萃取用到的分液漏斗使用前需_______并洗净,分液时有机层在分液漏斗的_____填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是______________;用饱和食盐水洗涤的目的是______________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____(填字母)。
a.蒸馏除去乙醚 b..重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先_______,再______。
 +HNO3(浓)
+HNO3(浓)HOOC(CH2)4COOH+NO2↑+H2O(未配平)

HOOC(CH2)4COOH

 (已知:苯胺易被氧化)
(已知:苯胺易被氧化)



 )用力振荡
)用力振荡



