-
铋酸钠(NaBiO3)广泛应用于制药业。其粉末呈浅黄色,不溶于冷水,遇沸水或酸则迅速分解。某同学设计如下实验,利用白色且难溶于水的Bi(OH)3在NaOH溶液中与Cl2反应制备NaBiO3,并探究其应用与纯度测定。请按要求回答下列问题:
(1)已知:Bi是N同主族元素,周期序数相差4,则Bi的原子序数为__。
Ⅰ.NaBiO3的制备,实验装置如图(加热和夹持仪器已略去)
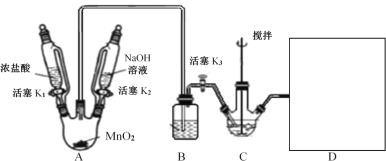
(2)A装置制备的气体是__;B装置的作用是__;补全图中D装置图(并标注试剂名称)___。
(3)C中反应的离子方程式为__。当观察到现象为___时,可以初步判断C中反应已经完成。
(4)反应完成后,处理装置A烧瓶中残留气体需进行的操作:__;为从装置C中获得尽可能多的产品,需进行的操作:__、过滤、洗涤、干燥。
Ⅱ.铋酸钠的应用,检测Mn2+
(5)向含有Mn2+的溶液中加入铋酸钠,再加入硫酸酸化,溶液变为紫红色,此反应中铋酸钠的作用是__;同学甲再向其中滴加MnSO4浓溶液,振荡,观察到紫红色褪去,有黑色固体(MnO2)生成,产生此现象的离子反应方程式为__。
Ⅲ.产品纯度的测定
(6)取上述NaBiO3(Mr=280)产品ag,加入适量稀硫酸和MnSO4稀溶液使其完全转化为Bi3+,再用bmo1·L-1的H2C2O4标准溶液滴定,当溶液紫红色恰好褪去时(假设Mn元素完全转化为Mn2+),消耗VmL标准溶液。该产品的纯度为__(用含a、b、V的代数式表示)。
-
铋酸钠(NaBiO3)是分析化学中的重要试剂,不溶于冷水,遇沸水或酸则迅速分解。某化学兴趣小组设计如图实验装置制取铋酸钠。装置丙中盛有Bi(OH)3(难溶于水)与NaOH溶液混合物。下列说法错误的是
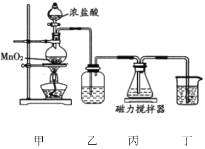
A.装置乙中盛装的试剂是饱和食盐水
B.装置丙中发生反应的离子方程式是:Bi(OH)3+3OH-+Na++Cl2=NaBiO3+2Cl-+3H2O
C.从装置丙中获得产品的操作为:在冰水中冷却结晶、过滤、洗涤、干燥
D.为除去所得固体中混有的Bi(OH)3,可用稀盐酸洗涤
-
铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
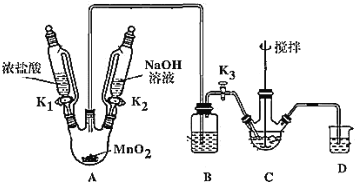
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(1)装MnO2的仪器名称是_____________,B装置用于除去HCl,盛放的试剂是________________;
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为_____;
(3)当观察到_____(填现象)时,可以初步判断 C 中反应已经完成;
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气,除去Cl2的操作是_______。
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是____________,过滤、洗涤、干燥;
Ⅱ.产品纯度的测定
(6)取上述NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用 c mo1/L的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4---CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗V mL标准溶液。该产品的纯度为 ______________(用含 w、c、V的代数式表示)。
-
连二亚硫酸钠(Na2S2O4)又称保险粉,是白色砂状或淡黄色粉末固体,己知连二业硫酸钠在碱性条件下较稳定,易被空气氧化,不溶于甲醇,遇水迅速分解,某同学设计利用如下图所示的实验装置制备一定量的连二亚硫酸钠,装置C中的试剂为甲酸钠(HCOONa)、NaOH 的甲醇溶液,回答下列问题:
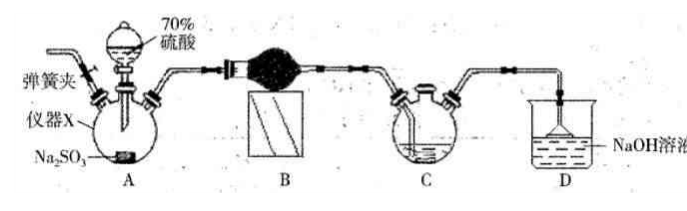
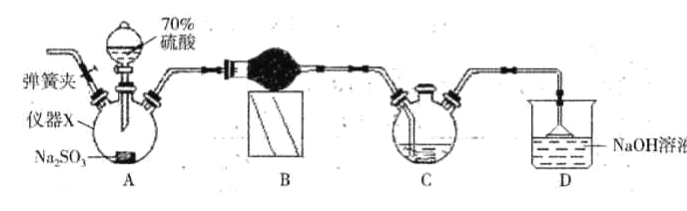
(1)仪器X的名称是_____。装置B中的球形干燥管中盛装的试剂是_______。
(2)装置D的作用是___________。实验时需要将C中温度控制在70-75℃,最好的控制方法是__________。
(3)实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是______。实验过程中装置C 中除有气体产生外,还能观察到的实验现象为____________。
(4)有同学通过仔细思考后认为,还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是______。为得到较纯的连二亚硫酸钠,需要对在过滤时得到的连二亚硫酸钠进行洗涤,洗涤的方法是_________。
(5)若实验中所用Na2SO3的质量为12.6g (硫酸是过量的),最终得到m g干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为_____________。
-
连二亚硫酸钠(Na2S2O4)又称保险粉,是白色砂状或淡黄色粉末固体,己知连二业硫酸钠在碱性条件下较稳定,易被空气氧化,不溶于甲醇,遇水迅速分解,某同学设计利用如下图所示的实验装置制备一定量的连二亚硫酸钠,装置C中的试剂为甲酸钠(HCOONa)、NaOH 的甲醇溶液,回答下列问题:
(1)仪器X的名称是_____。装置B中的球形干燥管中盛装的试剂是_______。
(2)装置D的作用是___________。实验时需要将C中温度控制在70-75℃,最好的控制方法是__________。
(3)实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是______。实验过程中装置C 中除有气体产生外,还能观察到的实验现象为____________。
(4)有同学通过仔细思考后认为,还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是______。为得到较纯的连二亚硫酸钠,需要对在过滤时得到的连二亚硫酸钠进行洗涤,洗涤的方法是_________。
(5)若实验中所用Na2SO3的质量为12.6g (硫酸是过量的),最终得到m g干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为_____________。
-
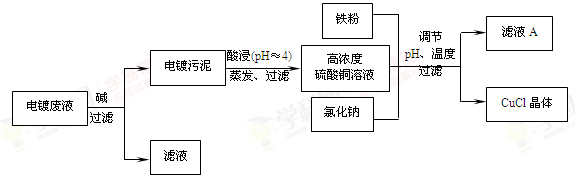
(16分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程如下:
请回答下列问题:
(1)电镀污泥的主要成分是 (写化学式)。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
。
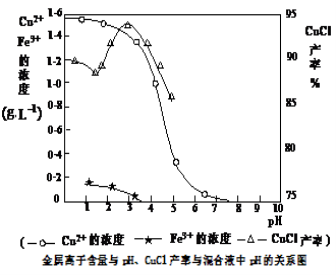
(3)析出CuCl晶体时的最佳pH在 左右。
(4)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是 。
(5)从滤液A中可回收的主要物质是 (写化学式)。
(6)以碳棒为电极电解CuCl2溶液可得到CuCl。写出电解CuCl2溶液后的阴极上发生的反应为
-
(15分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
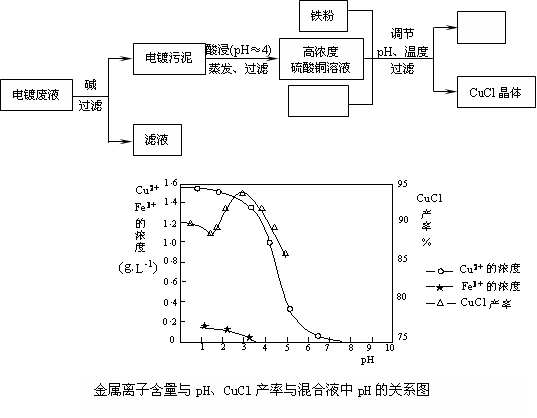
请回答下列问题:
(1)电镀污泥的主要成分是________(写化学式);
(2)酸浸时发生反应的离子方程式是________;
(3)析出CuCl晶体时的最佳pH在________左右;
(4)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
________;
(5)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是________。
-
溴化亚铜可用作工业催化剂,是一种白色粉末,微溶于冷水,不溶于乙醇等有机溶剂,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:

步骤1.在如上图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去水中的________________(写化学式)。
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为__________________;
②控制反应在60℃进行,实验中可采取的措施是____________________;
③说明反应已完成的现象是_____________________ 。
(3)步骤2过滤需要避光的原因是_____________________。
(4)步骤3中洗涤剂需“溶有SO2”的原因是____________________。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。
请补充实验步骤[须用到SO2(贮存在钢瓶中)、20%NaOH溶液]:
①_________________。
②___________________。
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④过滤,用乙醇洗涤2~3次。⑤放真空干燥箱中干燥。
-
溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:
步骤1.在如图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。

步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤。
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去其中水中的______________(写化学式)。
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为_______________;
②控制反应在60℃进行,实验中可采取的措施是_____________;
③说明反应已完成的现象是__________________。
(3)步骤2过滤需要避光的原因是_______________。
(4)步骤3中洗涤剂需“溶有SO2”的原因是_____________________最后溶剂改用乙醚的目的是________________________________。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。请补充实验步骤(须用到SO2(贮存在钢瓶中)、20%NaOH溶液、乙醇)
①_______________________________________________。
②__________________________________________________。
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④__________________________________________________。
⑤放真空干燥箱中干燥。
-
NaBiO3可作为测定锰的氧化剂,Bi2O3在电子行业有着广泛应用,可利用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)来制备,工艺流程如下:

已知:NaBiO3难溶于水。
回答下列问题
(1)溶液Ⅰ中主要成分为BiCl3、FeCl2,则滤渣Ⅰ的主要成分是________(写化学式)。
(2)海绵铋与盐酸、H2O2反应的化学方程式是__________
(3)向溶液Ⅲ中加入NaOH和NaClO发生反应的离于方程式是______,从反应后的混合体系中获得纯净NaBiO3,操作Ⅱ包括_________。
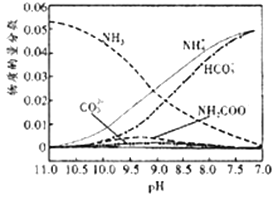
(4)一定温度下,向氨水中通入CO2,得到 (NH4)2CO3、NH4HCO3等物质,溶液中各种微粒的物质的量分数与pH的关系如图所示。随着CO2的通入,溶液中c(OH-)/c(NH3·H2O)将______(填“增大”“减小”或“不变”)。pH=9时,溶液中c(NH4+)+c(H+)=______(用离子浓度表示)。
(5)取所得NaBiO3样品2.0g,加入稀硫酸和MnSO4溶液使其完全溶解,然后用新配制的0.5mol/LFeSO4溶液滴定生成的MnO4-,滴定完成后消耗22.00mLFeSO4溶液。则该样晶中NaBiO3纯度为_________。












