-
反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平衡常数如下表所示。下列说法正确的是
温度
(K)
化学平衡常数
反应Ⅰ: 4NH3 + 5O2 → 4NO + 6H2O
反应Ⅱ: 4NH3 + 3O2 → 2N2 + 6H2O
反应Ⅲ: 2NO + O2 → 2NO2
500
1.1×1026
7.1×1034
1.3×102
700
2.1×1019
2.6×1025
1.0
A.使用选择性催化反应Ⅰ的催化剂可增大氧化炉中NO的含量
B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ
C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ
D.氧化炉出气在进入氧化塔前应进一步提高温度
高三化学单选题中等难度题查看答案及解析
-
(14分)工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
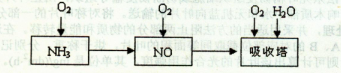
(1)已知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式________。当温度升高时,化学平衡常数K值________(填“增大”、“减小”、“无影响”)。
(2)硝酸厂尾气常用的处理方法是:催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7 kJ/mol
H2O(1)=H2O(g) △H=+44.0 kJ/mol
则8g H2恰好将NO2转化成N2和H2O(1)时△H=________。
(3)氨气是制取硝酸的重要原料,合成氨反应的化学方程式如下:N2+3H2
2NH3,该反应在固定容积的密闭容器中进行。
①下列各项标志着该反应达到化学平衡状态的是________(填字母)。
A.容器内N2、H2、NH3的浓度之比为l:3:2
B.
C.容器内压强保持不变
D.混合气体的密度保持不变
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2 L固定容积的密闭容器中,5 min后反应达平衡时,n(N2)=1.2 mol,n(H2)=1.2 mol, n(NH3)=0.8 mol,则反应速率v(N2)=________,平衡常数=________(保留两位小数)。若保持容器的温度和容积不变,将上述平衡体系中的混合气体的浓度增大1倍,则平衡________(填向左、向右或不移动)移动。
高三化学选择题中等难度题查看答案及解析
-
[化学—选修化学与技术](15分)
工业上常用氨氧化法生产硝酸,其生产过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
⑴氨催化氧化反应在一定温度下(水为气体)为正反应放热的可逆反应,写出该反应的化学方程式________和平衡常数表达式K=________,若升高温度,则K的值________(填“增大”“减小”或“不变”)。
⑵为了提高NH3的转化率,可以采取________。
a.减小压强b.增大反应物浓度c.使用催化剂d.降低温度e.及时分离出NH3
⑶原料气中空气必须过量,其主要原因是________。
⑷将铂铑合金做成薄丝网的主要原因是________。
⑸水吸收二氧化氮生成硝酸为放热反应,其化学方程式为________,
为了提高水对二氧化氮的吸收率,可采取的措施为________(答2项)。
高三化学填空题简单题查看答案及解析
-
亚硝酸钠是一种工业盐,虽然和食盐很像,但有毒,不能食用。以下为亚硝酸钠的工业生产流程:

(1)首先在反应塔中通SO2和淋入硝酸,控制反应生成的NO与NO2物质的量之比恰好1:1,则分解塔中发生反应的化学方程式为: 。试从产物产率的角度分析该反应中硝酸的浓度不宜过大或过小的原因是 。
(2)吸收塔中所发生化学反应方程式为: 。
(3)为测定亚硝酸钠的含量,称取4.500 g样品溶于水配成250 mL溶液,取20.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:

①锥形瓶中发生反应的离子方程式为 。
②第一组实验数据出现异常,造成这种异常的原因可能是_________(填代号)。
A.酸式滴定管用蒸馏水洗净后用标准液润洗
B.滴定终点时仰视读数
C.锥形瓶洗净后未干燥
③根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
高三化学实验题简单题查看答案及解析
-
工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
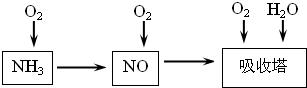
(1)已知反应一经发生,铂铑合金网就会处于红热状态.写出氨催化氧化的化学方程式:______△4NO+6H2O高三化学解答题中等难度题查看答案及解析
-
硝酸是重要的化工原料,工业上用氨催化氧化法生产硝酸,反应如下:
①氧化炉:4NH3+5O2=4NO+6H2O
②吸收塔:4NO+3O2+2H2O=4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80。完成下列计算:
(1)1mol NH3完全转化为NO至少需要空气______mol。工业上先将氨气和空气混合好,在氧化炉反应后直接通入吸收塔中用冷水吸收,为了确保吸收效果,第②步反应要求氧气至少过量20%,计算起始时空气与氨气的体积比至少为______
(2)硝酸工业产生的氮氧化物尾气(NO和NO2),可用烧碱吸收,反应如下:
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO3+NaNO2+H2O
现有含0.5mol氮氧化物的尾气,用8mol/L的NaOH溶液完全吸收,吸收后的溶液中c(OH﹣):c(NO2﹣):c(NO3﹣)=5:4:1。所用NaOH溶液的体积为______mL。若将尾气中NO与NO2的平均组成记为NOx,则x=______
(3)工业上用硝酸与氨气反应制取硝酸铵:HNO3+NH3=NH4NO3,反应时NH3的吸收率为97%,硝酸的利用率为98%。在用氨气制取硝酸时,氨气的利用率为90%。计算生产80吨的硝酸铵共需氨气__吨?(保留1位小数)
高三化学解答题困难题查看答案及解析
-
工业上用接触法制取硫酸过程中,硫铁矿在沸腾炉中燃烧的化学方程式是________,该反应中氧化剂是______,还原剂是______,被氧化的元素是______,被还原的元素是______。
高三化学填空题简单题查看答案及解析
-
工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
O2
(1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(2)硝酸厂尾气常用的处理方法是催化还原法:催化剂存在时用H2将NO2还原为N2 。已知:
2H2(g)+O2(g)=2H2O(g) △H= a kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H= b kJ·mol-1
H2O(1)=H2O(g) △H= c kJ·mol-1
则反应2NO2(g)+4H2(g)=N2(g)+4H2O(1)的△H=_________。(用a、b、c表示)
(3)①合成氨反应的化学方程式为N2+3H2
2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的相对分子质量保持不变
E.1mol N≡N键断裂,同时1mol H—H键断裂
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L的密闭容器中,5min反应达平衡,n(N2)=1mol,n(H2)=1mol,n(NH3)=2mol,则反应速率v(N2)=________________,H2的平衡转化率=_________________;若保持容器的温度不变,在10min时将容器的容积压缩为lL,请在答题卡坐标图中,画出从反应开始至15min时c(NH3)随时间变化曲线示意图。
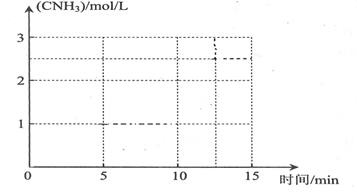
高三化学计算题中等难度题查看答案及解析
-
明末宋应星的著书《天工开物》中记载了我国古代炼锌的方法,用炉甘石(主要成分是ZnCO3)和木炭混合加热分两步反应得到锌,写出其中氧化还原反应的化学方程式_____________。
现代工业上利用锌焙砂提炼金属锌的流程如下图所示(已知:①锌焙砂的主要成分是ZnO、ZnFe2O4,还含有少量FeO、CuO、NiO杂质;②金属活动性顺序:Zn>Ni>Cu),请回答下列问题:
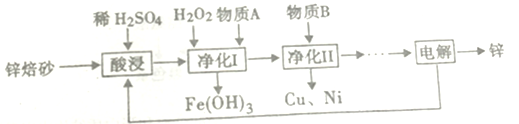
(2)化合物ZnFe2O4中Fe的化合价为_________,酸浸时,ZnFe2O4发生反应的化学方程式为________。
(3)净化I操作分两步:首先用H2O2处理酸浸液,然后用物质A调节溶液的PH使Fe3+转化为Fe(OH)3沉淀过滤后除去。
①写出用H2O2处理酸浸液时发生反应的离子方程式______________。
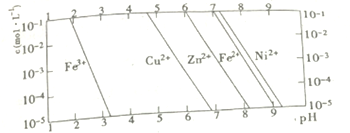
②下图中的斜线是溶液中金属阳离子浓度(纵标)随pH值(横标)变化时的沉淀溶解平衡线,若加入物质A只使Fe3+沉淀完全,则物质A可能是_____________(填出一种可能的化学式),调节后溶液的pH应控制在______________范围内(假设杂质离子浓度均不大于0.1mol· L-1 )。
③此流程中没有用调节pH来除去Cu2+的原因是_____________。
(4)净化II欲分离出Cu、Ni,加入的B物质的化学式_____________。
(5) 本流程中可以循环利用的化合物有_______________。
高三化学简答题困难题查看答案及解析
-
如图1所示是工业生产硝酸的流程:

合成塔中内置铁触媒,氧化炉中内置Pt-Rh合金网.请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨.2007年化学家格哈德•埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如图2所示.、
、
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______.
(2)合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g),写出该反应的化学平衡常数表达式K=______.在一定温度和压强下,将H2 和N2 按3:1(体积之比)混合后进入合成塔,反应达到平衡时,平衡混合气中NH3 的体积分数为15%,此时H2 的转化率为______.
(3)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1 266.8kJ/mol
N2(g)+O2(g)=2NO(g)△H=+1 80.5kJ/mol,氨催化氧化的热化学方程式为______.
(4)吸收塔中通入空气的目的是______.高三化学解答题中等难度题查看答案及解析