对于气相反应,用某组分(B)的平衡压强[p(B)]代替物质的量浓度(cB)也可表示平衡常数(记作Kp)。已知反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g),在t℃时的平衡常数 Kp=a,则下列说法正确的是
A.Kp=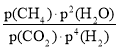
B.升高温度,若Kp 增大,则该反应为吸热反应
C.该反应达到平衡状态后,增大压强,平衡向左移动,Kp减小
D.t℃时,反应 CH4(g)+H2O(g)⇌
CH4(g)+H2O(g)⇌ CO2(g)+2H2 (g)的平衡常数Kp=
CO2(g)+2H2 (g)的平衡常数Kp= a
a
高一化学单选题简单题
对于气相反应,用某组分(B)的平衡压强[p(B)]代替物质的量浓度(cB)也可表示平衡常数(记作Kp)。已知反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g),在t℃时的平衡常数 Kp=a,则下列说法正确的是
A.Kp=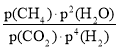
B.升高温度,若Kp 增大,则该反应为吸热反应
C.该反应达到平衡状态后,增大压强,平衡向左移动,Kp减小
D.t℃时,反应 CH4(g)+H2O(g)⇌
CH4(g)+H2O(g)⇌ CO2(g)+2H2 (g)的平衡常数Kp=
CO2(g)+2H2 (g)的平衡常数Kp= a
a
高一化学单选题简单题
对于气相反应,用某组分(B)的平衡压强[p(B)]代替物质的量浓度(cB)也可表示平衡常数(记作Kp)。已知反应CH4(g)+2H2O(g)⇌CO2(g)+4H2(g),在t℃时的平衡常数 Kp=a,则下列说法正确的是
A.Kp=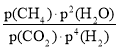
B.升高温度,若Kp 增大,则该反应为吸热反应
C.该反应达到平衡状态后,增大压强,平衡向左移动,Kp减小
D.t℃时,反应 CH4(g)+H2O(g)⇌
CH4(g)+H2O(g)⇌ CO2(g)+2H2 (g)的平衡常数Kp=
CO2(g)+2H2 (g)的平衡常数Kp= a
a
高一化学单选题简单题查看答案及解析
氮的化合物在生产生活中广泛存在。
(1)用焦炭还原NO的反应为:2NO(g)+C(s)⇌N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400 ℃、400 ℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO) (甲容器) /mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO) (乙容器) /mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO) (丙容器) /mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为______(填“放热”或“吸热”)反应。平衡常数的表达式为K=______
②乙容器在200 min达到平衡状态,则0~200 min内用NO的浓度变化表示的平均反应速率v(NO)=_。
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s)⇌N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
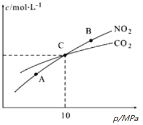
①A、B两点的浓度平衡常数关系:Kc(A)___Kc(B)(填“<”或“>”或“=”)。A、B、C三点中NO2的转化率最高的是_____(填“A”或“B”或“C”)点。
②计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)对于2NO(g)+2CO(g)⇌N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1 mol NO和0.3mol CO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是_____(填字母代号)
A. c(CO)=c(CO2) B. 容器中混合气体密度不变
C. v(N2)正=2v(NO)逆 D. 容器中混合气体的平均摩尔质量不变
②下图为容器内的压强(P)与起始压强(Po)的比值(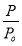 )随时间(t)的变化曲线,曲线中的两个点的坐标分别为(5,0.925)和(10,0.90)。平衡时NO的转化率为________
)随时间(t)的变化曲线,曲线中的两个点的坐标分别为(5,0.925)和(10,0.90)。平衡时NO的转化率为________

高一化学原理综合题困难题查看答案及解析
一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
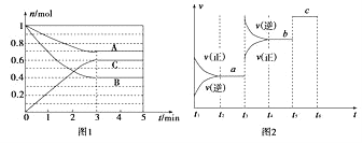
(1)该反应的化学方程式为___________。
(2)该反应的反应速率v随时间t的关系如上图2所示:
①根据上图判断,在t3时刻改变的外界条件是______。
②a、b、c三点中,C的体积分数最大的是________。
③各阶段的平衡常数如下表所示:
| t2~t3 | t4~t5 | t5~t6 |
| K1 | K2 | K3 |
K1、K2、K3之间的大小关系为________(用“>”、“<”或“=”连接)。
Ⅱ.在密闭容器中充入一定量的H2S,发生反应2H2S(g) 2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。

(1)△H_________ (填“>”“<”或“ = ”)0。
(2)图中压强(p1、p2、p3)的大小顺序为_______。
(3)图中M点的平衡常数Kp =____MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
高一化学原理综合题困难题查看答案及解析
大量实验事实表明,对于可逆反应,在一定温度下,无论反应物的起始浓度如何,反应达到平衡状态后,将各物质的物质的量浓度代入表达式:
(
表示物质C的物质的量浓度的p次方。)得到的结果是一个定值。我们把这个常数叫做该反应的化学平衡常数。这个式子叫化学平衡常数表达式。依据你的理解下列可逆反应平衡常数表达式错误的是( )
| 化学方程式 | 平衡常数表达式 | |
| A | | |
| B | | |
| C | | |
| D | | |
A.A B.B C.C D.D
高一化学单选题中等难度题查看答案及解析
一定温度下,在一恒容密闭容器中,发生反应:N2+3H22NH3,下列能说明反应已达到平衡状态的是( )
①体系的压强不变 ②体系的密度不变 ③各组分的物质的量浓度不变 ④各组分的质量分数不变 ⑤反应速率υ(N2):υ(H2)=1:3 ⑥混合气体的总物质的量不变⑦混合气体的平均相对分子质量不变 ⑧一个N≡N键断裂的同时,有2个N—H键的断裂 ⑨c(N2):c(H2):c(NH3)=1:3:2
A. ②③⑥⑦⑨ B. ②③⑤⑧⑨
C. ①③④⑥⑦ D. ①④⑤⑧⑨
高一化学单选题中等难度题查看答案及解析
对于可逆反应M+NQ达到平衡时,下列说法中正确的是( )
A.M、N、Q三种物质的浓度一定相等 B.M、N全部变成了Q
C.反应混合物各组分的浓度不再变化 D.压强不再变化
高一化学选择题简单题查看答案及解析
甲醇是重要的有机化工原料,在能源紧张的今天,甲醇的需求也在增大。甲醇的一种合成方法是:CO(g)+2H2(g)⇌CH3OH(g) ΔH<0
(1)①在恒温恒容的密闭容器中,能判断上述反应达到平衡状态的依据是___________(填字母)。
a.CH3OH的浓度不再发生变化
b.生成CH3OH的速率与消耗CO的速率相等
c.氢气的体积分数保持不变
d.混合气体的密度不变
②反应达到平衡后,改变反应的某一个条件,下列变化能说明平衡一定向逆反应方向移动的是____(填字母)。
a.正反应速率先增大后减小
b.逆反应速率先增大后减小
c.化学平衡常数K值减小
d.氢气的平衡转化率减小
(2)某温度下,将1.0molCO与2.0molH2充入2L的恒容密闭容器中发生反应,在第5min时达到平衡状态,此时甲醇的物质的量分数为10%。若在第10min、20min时分别改变反应条件,甲醇的浓度在不同条件下的变化如图所示。从反应开始到5min内,生成甲醇的速率为_________,H2的平衡转化率α=_____%。比较甲醇在7~8min、12~13min和25~27min内平均反应速率[平均反应速率分别以υ(7~8)、υ(12~13)、υ(25~27)表示]的大小_____。

(3)恒压条件下,将1.0molCO与2.0molH2充入2L的恒压密闭容器中发生反应,实验测得CO的平衡转化率与压强、温度的关系如图所示:
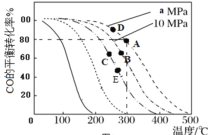
①由图像可知,a_____(填“>”“<”或“=”)10。300℃、aMPa时用分压表示的平衡常数Kp=_____(分压=总压×物质的量分数,用含a的式子表示)。
②在B点对反应容器降温的同时缩小容器体积,重新达到的平衡状态可能是图中A~E点中的_____点。
高一化学原理综合题困难题查看答案及解析
氮的氧化物是造成大气污染的主要物质。
(1)用活性炭还原NO的有关反应为:C(s)+2NO(g)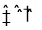 N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及10 min和20 min各物质平衡浓度如表所示:
N2(g)+CO2(g)。向恒容密闭容器中加入一定量的活性炭和NO,T℃时,各物质起始浓度及10 min和20 min各物质平衡浓度如表所示:
| 浓度mol/L 时间min | NO | N2 | CO2 |
| 0 | 10 | 0 | 0 |
| 10 | 5 | 2.5 | 2.5 |
| 20 | 2 | 4 | 0.25 |
①在10min时,若只改变某一条件使平衡发生移动,20min时重新达到平衡,则改变的条件是____。
②在20min时,保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原来的两倍,此时反应v正___v逆(填“>”“<”或“=”)。
(2)工业上由N2、H2来制备NH3。不同温度下,向三个相同的容器中投入相同的反应物进行反应,测得不同温度时平衡混合物中NH3的物质的量分数随压强增大而变化如图所示。
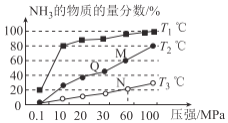
①M点的v正_______Q点的v正(填“>”“<”或“=”)。
②图中三条曲线对应的温度分别为T1、T2、T3,其中温度最高的是____。
③恒温恒容条件下,能说明反应N2(g)+3H2(g)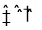 2NH3(g)达到平衡状态的是____(填选项字母)
2NH3(g)达到平衡状态的是____(填选项字母)
A. 2v(N2)=v(NH3) B.c2(NH3)/[c(N2)c3(H2)]保持不变
C.反应器中的压强不再发生变化 D.3 molH-H键断裂的同时,有2molN-H键断裂
(3)NO2存在如下平衡:2NO2(g)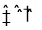 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系: v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系: v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。
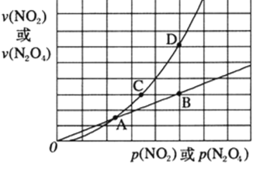
一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=____;在上图标出点中,指出能表示反应达到平衡状态的点是______。
高一化学原理综合题困难题查看答案及解析
(1)25 ℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
| 热化学方程式 | 平衡常数 | |
| ① | 2NO2(g)+NaCl(s) | K1 |
| ② | 4NO2(g)+2NaCl(s) | K2 |
| ③ | 2NO(g)+Cl2(g) | K3 |
则该温度下,ΔH3=_______________kJ∙mol-1;K3=_____________(用K1和K2表示)。
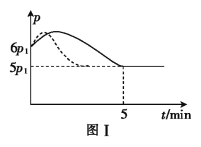
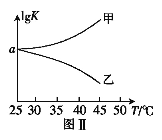
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则ΔH3 ___(填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是_____________;在5 min时,再充入0.08 mol NO和0.04 molCl2,则混合气体的平均相对分子质量将_____________(填“增大”、“减小”或“不变”)。图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(lgK)与温度的变化关系图,其中正确的曲线是______(填“甲”或“乙”),a值为__________。25 ℃时测得反应③在某时刻,NO(g)、Cl2(g)、NOCl(g)的浓度分别为0.8、0.1、0.3,则此时v正_________v逆(填“>”“<”或“=”)
(3)在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生CO2(g)+3H2(g) CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
高一化学填空题困难题查看答案及解析
煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关重要。请回答下列问题:
(1)煤的气化。原理是C(s)+2H2(g) CH4(g) ΔH。
CH4(g) ΔH。
在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
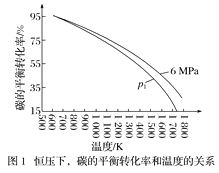
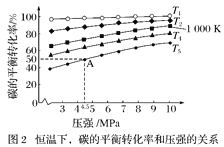
①有关图1、图2的说法正确的有___(填字母)。
a.p1<6MPa b.T1<1000K
c.ΔH<0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=__(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO+H2)与N2的体积之比为3.1~3.2,发生的反应有C(s)+H2O(g) CO(g)+H2(g),C(s)+
CO(g)+H2(g),C(s)+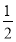 O2(g)
O2(g) CO(g)。从能量角度考虑,通入空气的目的是___。
CO(g)。从能量角度考虑,通入空气的目的是___。
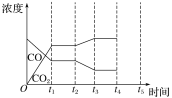
②如图是反应CO(g)+H2O(g) H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
高一化学原理综合题中等难度题查看答案及解析