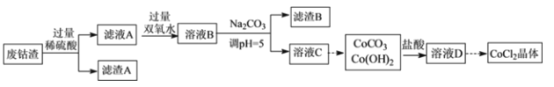
-
铁黄是一种重要的颜料,化学式为Fe2O3•xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如图:

(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是________、________。
(2)试剂a最好选用______(供选择使用的有:铝粉、空气、浓HNO3);其作用是________。
(3)上述步骤中需用到氨气.下列装置可用于实验室制氨气的是______(填序号)。
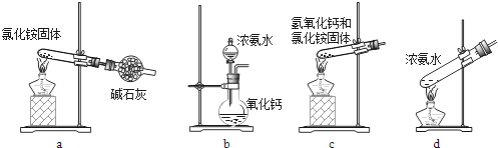
(4)检验溶液Z中含有NH4+的方法是________。
(5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。
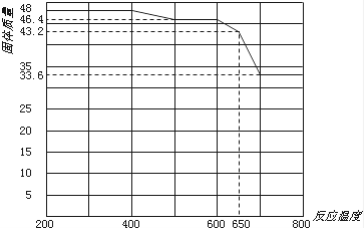
根据图像推断650℃时Fe2O3还原产物的化学式为________,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论)________。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。
-
利用硫酸渣(主要成分为Fe2O3和少量的SiO2、FeO)可以制备高纯度的氧化铁,制备流程如图:
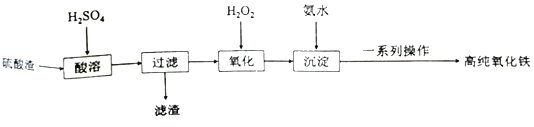
(1)滤渣的主要成分是___。
(2)“氧化”时发生反应的离子方程式为___。
(3)检验沉淀是否完全的方法为___。
(4)一系列操作包括:过滤、沉涤、干燥、___。
(5)用高温分解FeSO4也可以制备较纯的Fe2O3,写出反应的化学方程式___。
(6)上述硫酸渣含铁28%,现需高纯氧化铁64吨,理论上需用硫酸渣多少吨?___(写出计算过程)
-
铝土矿的主要成分是Al2O3、 Fe2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
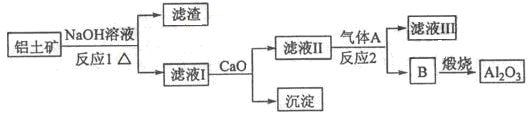
回答下列问题:
(1)写出反应1的化学方程式
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,
(3)工业生产中通入的气体A 应过量,理由是 ;
则反应2生成B的离子方程式为 ;
-
以黄铁矿为原料制备硫酸会产生大量的废渣,合理利用废渣可以减少环境污染,变废为宝。工业上,可利用废渣(含Fe2+、Fe3+的硫酸盐及少量 CaO和MgO)制备高档颜料铁红(Fe2O3) 和回收(NH4)2SO4,具体生产流程如下。
已知:铵黄铁矾的化学式为(NH4)2Fe6(SO4)4(OH)12。

(1)在废渣溶解操作时,应选用________溶解(填字母)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2)为了提高废渣溶解时的浸取效率,可采用的措施有哪些?___________________(写出一点即可)。
(3)物质A 是一种氧化剂,工业上一般选用空气,其理由是___________。氧化过程中发生反应的离子方程式为_________________。
(4)根据下图有关数据,你认为工业上氧化操作时应控制的最佳温度和pH是:______。

(5) 铵黄铁矾中 可能混有的 杂质有 Fe(OH)3、____________。 铵黄铁矾与氨水反应的离子方程式为______________。
-
工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。下图是从铝土矿中提纯Al2O3的简单示意图。其中涉及到的一个反应是:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。

(1)图示中(1)的实验操作是________;图示中(2)加入的试剂__________。
(2)试写出下列物质(或溶液中的溶质)的化学式:
B__________________;C__________________;H________________;F______________。
(3)写出化学方程式:
①_____________________________________。
③_____________________________________。
④_________________________________。
-
(8分).某科研小组用高岭土(主要成分是Al2O3·2SiO2·2H2O,并含少量CaO、Fe2O3)研制新型净水剂(铝的化合物)。试验流程如下:
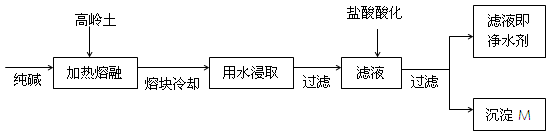
请回答下列问题:
(1)已知Al2O3 、SiO2与纯碱的反应相似。用化学方程式表示熔融时高岭土主要成分与纯碱发生反应的化学方程式、
________。
(2)在熔融高岭土与纯碱试样时,最好选用下列哪种仪器________(填写编号)
A.铁坩埚 B.瓷坩埚 C.氧化铝坩埚 D.玻璃坩埚
(3)写出上述过程中,最后得到的沉淀M的化学式________。
-
以黄铁矿为原料制硫酸会产生大量的废渣,合理利用废渣可以减少环境污染,变废为宝。工业上利用废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:

(1)在废渣溶解操作时,应选用________溶解(填字母)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2) 为了提高废渣的浸取率,可采用的措施有哪些?_______________(至少写出两点)。

(3)物质A是一种氧化剂,工业上最好选用________(供选择使用的有:空气、Cl2、MnO2),其理由是_______________。氧化过程中发生反应的离子方程式为_________________。
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件(从温度、pH和氧化时间三方面说明)是:______________________________________________________。
(5) 铵黄铁矾中可能混有的杂质有Fe(OH)3、________。
(6) 铵黄铁矾的化学式可表示为(NH4)xFey(SO4)z(OH)w,其化学式可通过下列实验测定:
① 称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00 mL溶液A。
② 量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32 g。
③ 量取25.00 mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体448mL,同时有红褐色沉淀生成。
④ 将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80 g。
通过计算,可确定铵黄铁矾的化学式为___________________________。(已知铵黄铁矾的摩尔质量为960g•mol-1,计算过程中不考虑固体损失和气体溶解。
-
实验室里常用的干燥剂有: ①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)作指示剂],④五氧化二磷,⑤ 无水氯化钙,⑥浓硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1)上述物质中,属于纯净物的是_____(填序号)。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为___、____、_____、_______(填序号)。
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(CoC12)呈蓝色,吸水后变为粉红色的CoCl2•6H2O,该变化过程属于_____ (填“物理变化”或“化学变化”)。
(4)下列气体中,能用固体氢氧化钠干燥的是_________
A.CO2 B.HCl C.NO2 D.NH3 E.NO
(5)生石灰常用作食品干燥剂,久置后易失去干燥能力,其原因为_____(用化学方程式表示)。
-
实验室里常用的干燥剂有:①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)作指示剂],④五氧化二磷,⑤无水氯化钙,⑥浓硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1)上述物质中,属于纯净物的是__________。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为______、________、________、______。(填序号)
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2•6H2O,该变化过程属于____________(填“物理变化”或“化学变化”)。
(4)下列气体中,能用固体氢氧化钠干燥的是( )
A.CO2 B.HCl C.NO2 D.NH3 E.NO
(5)生石灰常用作食品干燥剂,久置后易失去干燥能力,其原因为_________________ (用化学方程式表示)
(6)上述干燥剂中,仅有浓硫酸为液体干燥剂,下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸为液体干燥剂,干燥效率高,能用于干燥所有的气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
-
实验室里常用的干燥剂有:①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)作指示剂],④五氧化二磷,⑤无水氯化钙,⑥浓硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1)上述物质中,属于纯净物的是__________。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为______、________、________、______。(填序号)
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2•6H2O,该变化过程属于____________(填“物理变化”或“化学变化”)。
(4)下列气体中,能用固体氢氧化钠干燥的是( )
A.CO2 B.HCl C.NO2 D.NH3 E.NO
(5)生石灰常用作食品干燥剂,久置后易失去干燥能力,其原因为_________________ (用化学方程式表示)
(6)上述干燥剂中,仅有浓硫酸为液体干燥剂,下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸为液体干燥剂,干燥效率高,能用于干燥所有的气体
D.浓硫酸在常温下能够使铁、铝等金属钝化