-
CH4与CO2重整生成H2和CO的过程中主要发生下列反应
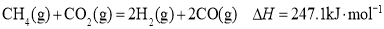
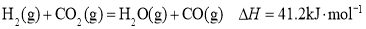
在恒压、反应物起始物质的量比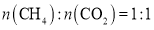 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是

A.升高温度、增大压强均有利于提高CH4的平衡转化率
B.曲线B表示CH4的平衡转化率随温度的变化
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH4):n(CO2)=1:1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
-
已知CH4与CO2在一定条件下能发生反应,CH4(g)+CO2(g) 2CO(g)+2H2(g)△H=+247.0 kJ·mol-1。在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在温度为753K下发生反应,CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)△H=+247.0 kJ·mol-1。在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在温度为753K下发生反应,CO2的平衡转化率如下表所示:
| 容器 | 起始物质的量(n)mol | CO2的平衡转化率 |
| CH4 | CO2 | CO | H2 |
| A | 1 | 1 | 0 | 0 | 50% |
| B | 1 | 1 | 2 | 2 | |
(1)若容器A中反应从开始到平衡所用的时间为t min,则t min内该反应的平均反应速率为:v(CO2)=___________(用含t的表达式表示)。
(2)温度为753K时该反应的平衡常数K=________;容器B中的反应起始时将_________移动(填“正向”、“逆向”或“不”)。
(3)反应达到平衡时,其他条件不变,升高温度,此时v正________v逆(填“>”、“=”或“<”)。
(4)当容器A、B中的反应均达到平衡时,容器中n(CO)满足的关系:2n(CO)A_____n(CO)B(填“>”、“=”或“<”)。
-
向密闭容器中充入物质的量浓度均为 0.1 mol/L的CH4和 CO2,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
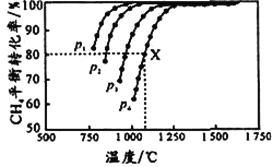
A. 平衡时CO与H2的物质的量比为1:1
B. p1、p2、p3、p4由大到小的顺序为p1<p2<p3<p4
C. 1100℃,p4条件下,该反应10 min时达到平衡点X,则ν(CO2) = 0.008 mol•L-1•min-1
D. 随着温度升高,该反应的平衡常数减小
-
CH4-CO2催化重整反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。该原理不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)已知:C(s)+2H2(g)=CH4(g)△H=-75kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-394kJ•mol-1
C(s)+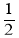 O2(g)=CO(g)△H=-111kJ•mol-1
O2(g)=CO(g)△H=-111kJ•mol-1
①催化重整反应的△H=______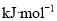 。
。
②L(L1、L2)、X可分别代表压强或温度。如图表示L一定时,CH4-CO2催化重整反应中CH4(g)的平衡转化率随X 的变化关系。
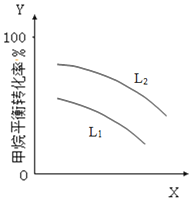
X代表的物理量是______;判断L1、L2的大小关系L1______L2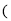 填“
填“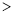 ”、“
”、“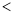 ”或“
”或“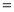 ”
”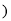 ,并简述理由:______。
,并简述理由:______。
(2)某温度下,在体积为2L 的容器中加入2mol CH4、1molCO2以及催化剂进行重整反应,经过2min 达到平衡状态时测得CO2的转化率是50%。
①反应达到平衡状态的标志是______ 填字母
填字母 。
。
A.单位时间内生成n mol的CH4的同时,生成n mol 的H2
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.反应体系中气体的总物质的量不变
D.容器中的混合气体密度不再发生变化
②平均化学反应速率v(CH4)______ mol•L-1•min-1;其平衡常数为______mol2•L-2;若其它条件不变增大压强,则合成反应的化学平衡常数______ 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变” 。
。
③达到平衡后,其它条件不变时向反应容器中充入CO2和CO 各1mol,则化学平衡______移动 填“正反应方向”、“逆反应方向”或“不”
填“正反应方向”、“逆反应方向”或“不”
-
数十年来,化学工作者对氮的氧化物、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)
N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) 2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________;
II.利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放
已知重整过程中部分反应的热化方程式为:
①CH4(g)=C(s)+2H2(g)ΔH>0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
③CO(g)+H2(g)=C(s)+H2O(g)ΔH<0
固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。
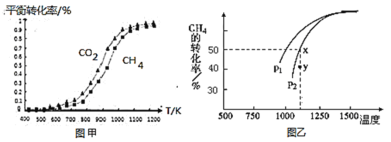
在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g)+CH4(g) 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,已知P2=aPa求x点对应温度下反应的平衡常数Kp=__________________。
2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,已知P2=aPa求x点对应温度下反应的平衡常数Kp=__________________。
III.根据2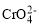 +2H+
+2H+
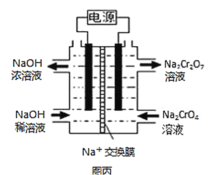
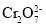 +H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的____________极,电解制备过程的总反应的离子方程式为____________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为____________。若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为____________。
+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的____________极,电解制备过程的总反应的离子方程式为____________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为____________。若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为____________。
-
氮的固定是指将氮元素由游离态转化为化合态的过程.据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:2N2(g)+6H2O(l)⇌4NH3(g)+3O2ΔH=+1530.0kJ/mol。目前工业合成氨的原理是:N2(g)+3H2(g)⇌2NH3(g)ΔH=-93.0kJ/mol。
回答下列问题:
(1)写出表示氢气燃烧热的热化学方程式________。
(2)在恒温恒容密闭容器中进行的工业合成氨反应,下列能表示达到平衡状态的是________(填序号)。
A.混合气体的压强不再发生变化
B.混合气体的平均相对分子质量不再发生变化
C.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
D.单位时间内断开3a个H-H键的同时形成6a个N-H键
E.反应容器中NH3的物质的量不再发生变化
(3)在一定温度下,向容积不变(始终为10L)的密闭容器中加入2molN2、8molH2及固体催化剂,10min后反应达到平衡状态,容器内气体压强变为起始的80%,10min内用氮气的浓度表示的化学反应速率为________,平衡时氮气的转化率为________。则该温度下反应的平衡常数K=________(计算结果可用分数表示)。
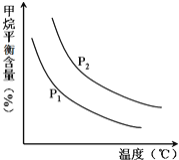
(4)原料气H2可通过反应CH4(g)+H2O(l)⇌CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①下图中,两条曲线表示压强的关系是:P1________P2(填“>”、“=”或“<”).
②该反应为________反应(填“吸热”或“放热”).
-
化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3,FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
(1)用FeO作载氧剂,部分反应的lgKp与温度的关系如图所示。[已知:平衡常数Kp是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]
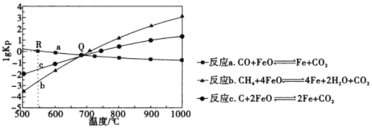
①图中涉及的反应中,属于放热反应的是反应________(填字母 a , b 或 c) 。
②R 点对应温度下,向某恒容密闭容器中通入 1. 5mol CO, 并加入足量的 FeO, 只发生反应a:CO(g) + FeO(s)⇌CO2 (g)+ Fe(s), 则CO的平衡转化率为_________。
(2)在T℃下,向某恒容密闭容器中加入 2mol CH4 ( g ) 和 8mol FeO ( s ) 进行反应 b:CH4 (g) + 4FeO(s)⇌4Fe(s)+ 2H2O( g) +CO2 ( g) 。反应起始时压强为 P0,达到平衡状态时 ,容器的气体压强是起始压强的 2 倍。
①反应达平衡时 ,容器内气体的总物质的量为______mol;
②T℃下,该反应的Kp =________。
③若起始时向该容器中加入 0. 5mol CH4 (g), 2mol FeO(s), 3mol H2O(g), 1. 5mol CO2 (g), 此时反应向______(填“正反应”或“逆反应”)方向进行。
(3)一种微胶囊吸收剂 ,将煤燃烧排放的 CO2 以安全、高效的方式处理掉,胶囊内部充有 Na2CO3 溶液,其原理如下图所示。
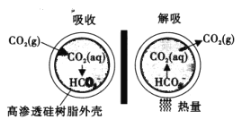
①这种微胶囊吸收 CO2 的原理是_________(用离子方程式表示)。
②将解吸后的CO2 催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) △H1 =-1323kJ• mol-1
2H2(g)+O2(g)=2H2O(g) △H2= -483. 6kJ• mol-1
则该过程的反应热为: 2CO2 (g) +6H2 (g)=C2H4(g) + 4 H2O ( g) △H3 =_______。
-
在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应生成Z,平衡后测得X,Y的转化率与起始时两物质的物质的量之比
 的关系如图所示,据此判断下列说法正确的是 ( )
的关系如图所示,据此判断下列说法正确的是 ( )

A.上述反应的化学方程式为:X+Y⇌3Z
B.该条件下,X、Y和Z一定为气体
C.该反应一定为氧化还原反应
D.反应速率 (X):
(X): (Y)=3:1
(Y)=3:1
-
已知CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g), ΔH=+247kJ·mol−1,则有利于提高CH4平衡转化率的条件是( )
A. 高温低压 B. 低温高压 C. 高温高压 D. 低温低压
-
二甲醚(CH3OCH3)常作为甲基化试剂用于生产硫酸二甲酯,CO2催化加氢合成二甲醚的过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH2=-122.5kJ·mol-1
回答下列问题:
(1)2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g) ΔH=______,欲提高该反应中CH3OCH3(g)的平衡产率,理论上应采取的措施是______(填标号)。
A.低压高温 B.高压低温 C.高压高温 D.低压低温
(2)一定温度下,在恒容密闭器容中发生反应Ⅱ,下列能判断反应达到平衡状态的有______(填标号)。
A.v正(CO2)=2v逆(CH3OCH3)
B.气体的压强不再变化
C单位时间每消耗2molCO2,同时产生1molCH3OCH3
D.H2与H2O的物质的量之比为2:1
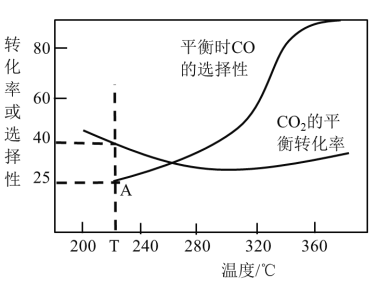
(3)在恒压、CO2和H2的起始量一定条件下,CO2平衡转化率和平衡时CO的选择性(CO的选择性=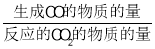 ×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
(4)一定温度下,向容积为2L的恒容密闭器容中充入CO(g)和H2O(g),发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)。CO和H2O的平衡转化率(a)与起始充入的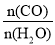 的关系如图所示:
的关系如图所示:
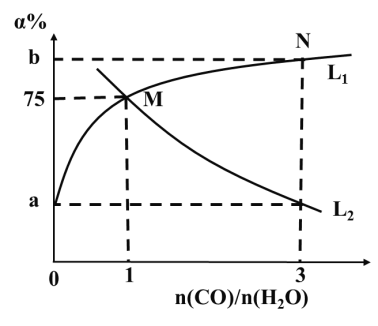
①a:b=______。
②图中表示CO变化趋势的曲线为______(填“L1”或“L2”);该温度下,反应的平衡常数K=______。
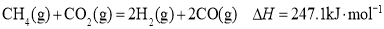
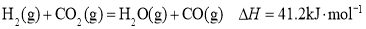
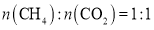 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
 2CO(g)+2H2(g)△H=+247.0 kJ·mol-1。在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在温度为753K下发生反应,CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)△H=+247.0 kJ·mol-1。在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在温度为753K下发生反应,CO2的平衡转化率如下表所示:
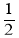 O2(g)=CO(g)△H=-111kJ•mol-1
O2(g)=CO(g)△H=-111kJ•mol-1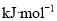 。
。
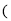 填“
填“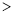 ”、“
”、“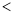 ”或“
”或“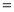 ”
”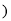 ,并简述理由:______。
,并简述理由:______。 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,已知P2=aPa求x点对应温度下反应的平衡常数Kp=__________________。
2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,已知P2=aPa求x点对应温度下反应的平衡常数Kp=__________________。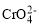 +2H+
+2H+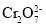 +H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的____________极,电解制备过程的总反应的离子方程式为____________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为____________。若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为____________。
+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的____________极,电解制备过程的总反应的离子方程式为____________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为____________。若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为____________。
 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:



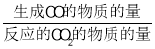 ×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
×100%)随温度的变化如图。T℃时,起始投入2molCO2、6molH2,达到平衡时,反应I理论上消耗H2的物质的量为______;合成二甲醚时较适宜的温度为260℃,其原因是______。
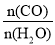 的关系如图所示:
的关系如图所示: