氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂为_________,还原产物为_________(均填化学式)
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为_________,转移电子的数目是_________
③用双线桥表示转移电子的数目_________。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为_________,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式_________
(3)次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,其电离方程式是:H3PO2⇌H++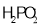 ,具有较强还原性,回答下列问题:
,具有较强还原性,回答下列问题:
①H3PO2中,磷元素的化合价为_________
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:_________
A.PH3 B.H3PO3 C.P D.H3PO4
③NaH2PO2是正盐还是酸式盐?_________,其溶液显_________性(填弱酸性、中性、或者弱碱性)
高二化学原理综合题中等难度题