我国科研工作者构建了一种在反应过程中能同时活化水和甲醇的双功能结构催化剂,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程(TS表示过渡态)。
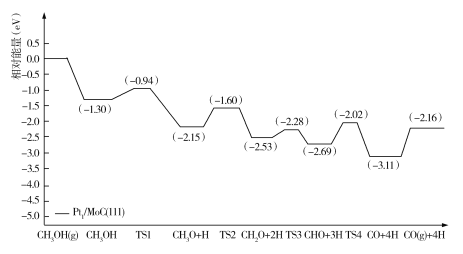
下列说法错误的是
A.CH3OH的脱氢反应是分步进行的
B.甲醇脱氢反应历程的最大能垒(活化能)是1.30 eV
C.甲醇脱氢反应中断裂的化学键有C—H键和O—H键
D.该催化剂的研发为醇类重整产氢的工业应用提供了思路
高三化学单选题中等难度题
我国科研工作者构建了一种在反应过程中能同时活化水和甲醇的双功能结构催化剂,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程(TS表示过渡态)。

下列说法错误的是
A.CH3OH的脱氢反应是分步进行的
B.甲醇脱氢反应历程的最大能垒(活化能)是1.30 eV
C.甲醇脱氢反应中断裂的化学键有C—H键和O—H键
D.该催化剂的研发为醇类重整产氢的工业应用提供了思路
高三化学单选题中等难度题
我国科研工作者构建了一种在反应过程中能同时活化水和甲醇的双功能结构催化剂,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程(TS表示过渡态)。

下列说法错误的是
A.CH3OH的脱氢反应是分步进行的
B.甲醇脱氢反应历程的最大能垒(活化能)是1.30 eV
C.甲醇脱氢反应中断裂的化学键有C—H键和O—H键
D.该催化剂的研发为醇类重整产氢的工业应用提供了思路
高三化学单选题中等难度题查看答案及解析
一种双功能结构催化剂能同时活化水和甲醇,用以解决氢气的高效存储和安全运输。下图是甲醇脱氢转化的反应历程(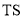 表示过渡态)
表示过渡态)
下列说法正确的是( )
A.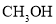 的脱氢反应是分步进行的
的脱氢反应是分步进行的
B.甲醇脱氢反应历程的最大能垒(活化能)是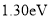
C.甲醇脱氢反应中断裂了极性键和非极性键
D.该催化剂的研发为醇类重整产氢的工业应用提供了新思路
高三化学多选题中等难度题查看答案及解析
甲醇耐高温、易存储热值高、节能环保,可做燃料,又是重要的化工原料。科学家用太阳能分解水生成的氢气在催化剂作用下与反应生成甲醇。已知:
、
和
的燃烧热∆H分别为
、
和
。请回答下列问题:
(1)用太阳能分解水消耗的能量是________
。
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________。
(3)催化加氢合成甲醇(反应Ⅱ)中伴随着反应Ⅰ的发生:
反应Ⅰ:
反应Ⅱ:
在恒压、和
的起始量一定的条件下,
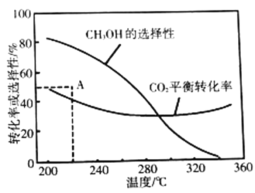
平衡转化率和平衡时
的选择性随温度的变化如图。其中:
的选择性

①温度高于300℃,平衡转化率随温度升高而上升的原因是_________。
②220℃时,在催化剂作用下与
反应一段时间后,测得
的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高
选择性的措施有_________________(写出两点)。
(4)在体积为的密闭容器中充入
和
发生反应Ⅱ,到平衡时氢气的转化率为25%,求该反应的平衡常数K=________。(结果保留二位有效数字)
(5)研究证实,也可在硫酸溶液中用惰性电极电解生成甲醇,生成甲醇的电极反应式为__________,另一极电解产物是________________。
高三化学综合题中等难度题查看答案及解析
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H原子将CO2高效还原为重要工业原料之一的甲醇,反应机理如下图。下列有关说法不正确的是
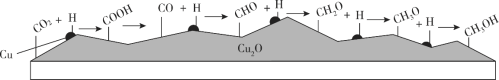
A. CO2生成甲醇是通过多步还原反应实现的
B. 催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
C. 该催化过程中只涉及化学键的形成,未涉及化学键的断裂
D. 有可能通过调控反应条件获得甲醛等有机物
高三化学单选题中等难度题查看答案及解析
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H原子将CO2高效还原为重要工业原料之一的甲醇,反应机理如下图。下列有关说法不正确的是
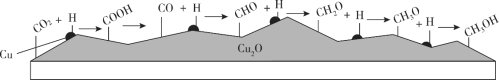
A. CO2生成甲醇是通过多步还原反应实现的
B. 催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
C. 该催化过程中只涉及化学键的形成,未涉及化学键的断裂
D. 有可能通过调控反应条件获得甲醛等有机物
高三化学单选题中等难度题查看答案及解析
我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )
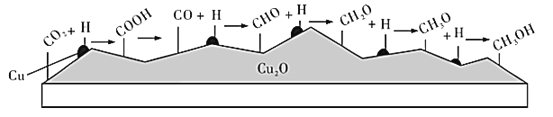
A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
高三化学单选题中等难度题查看答案及解析
中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。请回答下列问题:
(1)基态铁原子的价层电子轨道表达式为______。
(2)硅、碳位于同一主族,用“”“
”或“
”填空:
| 性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
| 项目 |
|
|
|
|
(3)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有______ (任写一种);1 mol[Fe(CN)6 ]3-中含______molσ键。
(4)已知:反应,碳原子的杂化类型转化过程为______;
从共价键重叠方式看,分子中
键类型为;
的键角比
的键角______
填“大”或“小”
。
(5)铁晶体有两种晶胞,如图1、图2所示。

图1中晶胞中铁的配位数为______;图2中铁晶胞堆积方式为______。
(6)碳化硅晶胞如图3所示,已知碳化硅晶体的密度为dg⋅cm-3,NA表示阿伏加德罗常数的值,则碳化硅中硅碳键的键长为______ pm。
高三化学填空题简单题查看答案及解析
中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。请回答下列问题:
(1)基态铁原子的价层电子轨道表达式为______。
(2)硅、碳位于同一主族,用“”“
”或“
”填空:
| 性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
| 项目 |
|
|
|
|
(3)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有______ (任写一种);1 mol[Fe(CN)6 ]3-中含______molσ键。
(4)已知:反应,碳原子的杂化类型转化过程为______;
从共价键重叠方式看,分子中
键类型为;
的键角比
的键角______
填“大”或“小”
。
(5)铁晶体有两种晶胞,如图1、图2所示。
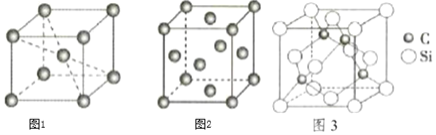
图1中晶胞中铁的配位数为______;图2中铁晶胞堆积方式为______。
(6)碳化硅晶胞如图3所示,已知碳化硅晶体的密度为dg⋅cm-3,NA表示阿伏加德罗常数的值,则碳化硅中硅碳键的键长为______ pm。
高三化学填空题简单题查看答案及解析
参考下列图表和有关要求回答问题:
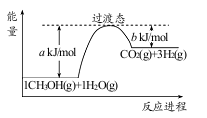
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2。右图是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是_____ (填“增大”、“减小”、“不变”),反应热△H的变化是_____(填“增大”、“减小”、“不变”)。请写反应进程出CH3OH(g)和H2O(g)反应的热化学方程式_____。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:
CH3OH(g)+1/2O2(g)CO2(g)+2H2(g) △H=c kJ/mol
又知H2O(g)H2O(l) △H=d kJ/mol。
则甲醇燃烧生成液态水的热化学方程式为_____。
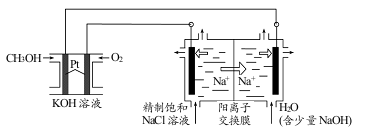
(3)以CH3OH燃料电池为电源电解法制取ClO2。二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH=_____,负极反应式为_____。
②图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2。阳极产生 ClO2的反应式为_____。
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_____mol。
高三化学填空题困难题查看答案及解析
将大气中的氮气活化合成氨是维持地球上生命所必需的转化过程,最近我国成功研制出高效电催化固氮催化剂Mo2N,它的研制成功能有效提高氮肥生产效率。
回答下列问题:
(1)钼(Mo)位于第五周期,与铬同副族,则Mo的价电子排布式为______________。
(2)基态氮原子核外电子空间运动状态有____种,氮元素所在周期中第一电离能最大的前三种元素依次是____(按由大到小的顺序写)。
(3)氮元素能形成一系列的化合物,如NH3、HN3(结构式为)、H2NCH2COOH等。NH3的分子构型为________,HN3结构式中间两个氮原子的杂化轨道类型为________,1个HN3分子中含______个π键;H2NCH2COOH(熔点为182 ℃)、CH3CH2COOH(熔点为−22 ℃)的相对分子质量几乎相同,但熔点相差很大,从物质结构的角度分析,导致该现象的主要原因是______。
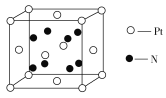
(4)氮与铂元素形成的某种化合物晶胞如图所示,则该化合物的化学式为______,若该晶胞的边长为d pm,则晶体的密度为____ g/cm3。
高三化学综合题中等难度题查看答案及解析