-
氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理,对于消除环境污染有重要意义。回答下列问题:
(1)已知2NO(g)+O2(g) -2NO2(g)△H的反应历程分两步:
-2NO2(g)△H的反应历程分两步:
①2NO(g) N2O2(g)(快) △H1<0,v1正=k1正c2(NO),v1逆=k1逆c2(N2O2)
N2O2(g)(快) △H1<0,v1正=k1正c2(NO),v1逆=k1逆c2(N2O2)
②N2O2(g)+ O2(g)  2NO2(g)(慢) △H2<0,v2正=k2正c2(N2O2)•c(O2),v2逆=k2逆c2(NO2)
2NO2(g)(慢) △H2<0,v2正=k2正c2(N2O2)•c(O2),v2逆=k2逆c2(NO2)
比较反应①的活化能E1与反应②的活化能E2的大小: E1__ E2 (填“>”、“<”或“=”) 其判断理由是__________;2NO(g)+O2(g) 2NO2(g) 的平衡常数K与上述反应速率常数k1正、k1逆、k2正、 k2逆的关系式为_______;已知反应速率常数k随温度升高而增大,若升高温度后k2正、 k2逆分别增大a倍和b倍,则a____b (填“>”、“<”或“=”);一定条件下,2NO (g)+O2(g)
2NO2(g) 的平衡常数K与上述反应速率常数k1正、k1逆、k2正、 k2逆的关系式为_______;已知反应速率常数k随温度升高而增大,若升高温度后k2正、 k2逆分别增大a倍和b倍,则a____b (填“>”、“<”或“=”);一定条件下,2NO (g)+O2(g)  2NO2 (g)达平衡后,升高到某温度,再达平衡后v2正较原平衡减小,根据上述速率方程分析,合理的解释是_________________。
2NO2 (g)达平衡后,升高到某温度,再达平衡后v2正较原平衡减小,根据上述速率方程分析,合理的解释是_________________。
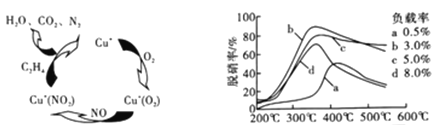
(2)①以乙烯(C2H4)作为还原剂脱硝(NO),其脱硝机理如左下图所示,若反应中n(NO):n(O2) =2:1,则总反应的化学方程式为_______________;脱硝率与温度、负载率(分子筛中催化剂的质量分数) 的关系如右下图,为达到最佳脱硝效果,应采用的条件是________________。
②用NO可直接催化NO分解生成N2、O2,将其反应机理补充完整(Vo代表氧空穴):
2Ni2++2Vo+2NO→2Ni3++2O-+N2 2O-→+O2-+1/2O2+V。______________
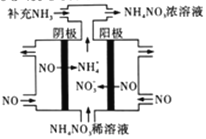
(3)电解NO可制备NH4NO3,其工作原理如右图所示,阴极的电极反应式为______________。
-
氮的氧化物和氮的氢化物的任意排放均会对环境造成污染,因此关于其转化的研究对于消除环境污染有着重要意义。
(1)已知T℃时,有如下反应:
反应I:4NH3(g) + 6NO(g) 5N2 ( g) + 6H2O(g) △H = -1804 kJ•mol-1
5N2 ( g) + 6H2O(g) △H = -1804 kJ•mol-1
反应II:N2(g) +2O2(g)  2NO2(g) △H = +67.8 kJ•mol-1
2NO2(g) △H = +67.8 kJ•mol-1
反应III:2NO(g) + O2 (g)  2 NO2 (g) △H =-116.2 kJ•mol-1
2 NO2 (g) △H =-116.2 kJ•mol-1
试写出T℃ 时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式 ______。
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(mol•L-1) 如下表所示:
| 时间( min) | NO | O2 | NO2 |
| 0 | a | 0.30 | 0.10 |
| 10 | 0.14 | 0.27 | b |
| 20 | 0.10 | c | 0.20 |
| 30 | d | 0.24 | 0.22 |
| 40 | 0.08 | e | f |
①温度不变,反应达平衡后容器中的压强与最初加入气体时的压强之比为_______。
②反应的前 20 min 的平均反应速率v(NO)=________mol•L-1·min-1。
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,c(O2)_____0.48mol•L-1(填“>”“<”或“ =”)。
(3)某化学兴趣小组利用电解原理设计实验消除NH3 与 NO对环境的影响, 并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:
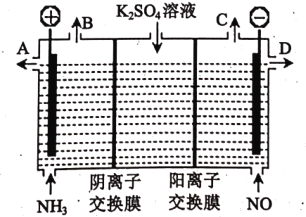
①从出口B、C产生的气体相同,该气体是_____:从出口 D 得到的溶液是____。
②电解槽左池中发生的电极反应式为________ 。
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成____________mol KOH。
-
氮氧化物是环境污染物,研究氮氧化物转化有重要的意义。回答下列问题:
(1)催化转化器可使汽车尾气反应而转化:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH
已知:2C(s)+O2(g)=2CO(g) ΔH1=akJ·mol-1;
C(s)+O2(g)=CO2(g) ΔH2=bkJ·mol-1;
N2(g)+O2(g)=2NO(g) ΔH3=ckJ·mol-1
ΔH=__kJ·mol-1(用含a、b、c的代数式表示);
(2)T℃时,将等物质的量的NO和CO充入容积为1L的密闭容器中发生尾气转化反应,容器中NO物质的量随时间变化如图所示。
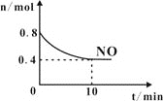
①T℃时,该化学反应的平衡常数K=___。
②下列事实能判断汽车尾气转化反应达到到化学平衡状态的是___;
A.体系中NO的转化率和CO的转化率相等 B.气体的密度不再变化
C.NO消耗速率等于N2消耗速率的2倍 D.混合气体平均相对分子质量不再变化
③已知汽车尾气转化反应的ΔH<0。10min后,改变下列示意图横坐标对应的反应条件,纵坐标对应的量变化关系不正确的是___。(填序号)
a.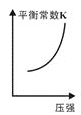 b.
b.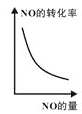 c.
c. d.
d.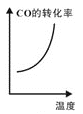
(3)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g) 2I(g)(快反应)
2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
下列表述不正确的是___(填标号)。
A.IO为反应的中间产物
B.第二步活化能比第三步小
C.第二步对总反应速率起决定作用
D.N2O分解反应中,k值与是否含碘蒸气无关
(4)碱吸收、碳还原是目前工业生产中处理氮氧化物的常用方法。
①碱吸收的常见产物为NaNO2。常温下,pH=8的NaNO2溶液中c(Na+)-c(NO2-)=___mol·L-1(用精确值表示);
②碳还原法是在高温条件下将NO与NO2混合气体与焦炭反应,生成CO2和N2,且物质的量之比为4:3,写出该方法的化学方程式___。
-
研究碳氧化合物、氮氧化合物、硫氧化合物等大气污染物的处理对缓解环境污染、能源危机具有重要意义。
(1)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g)△H<0。其他条件相同,在甲、乙两种催化剂作用下,相同时间时NO转化率与温度的关系如图。
4N2(g)+6H2O(g)△H<0。其他条件相同,在甲、乙两种催化剂作用下,相同时间时NO转化率与温度的关系如图。
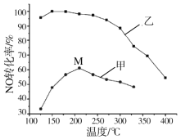
①工业上选择催化剂__________(填“甲”或“乙”)。
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是__________。(写一条即可)。
(2)某研究小组对反应NO2+SO2 SO3+NO△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。
SO3+NO△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。
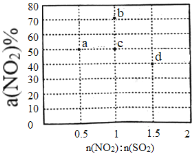
①如果将图中b点的平衡状态改变为c点的平衡状态,应采取的措施是________________。
②图中a、d两点对应的实验温度分别为T1和T2,则T1_______T2(填“>”、“=”或“<”)。
(3)在酸性电解质溶液中,以惰性材料作电极,将CO2转化为丙烯的原理如图所示。
①太阳能电池的正极为_____(填“a”或“b”)。
②生成丙烯的电极反应式是_____________________________。
③当生成标准状况下2.24L丙烯时,右侧溶液中质量减少____g。

-
氮及其化合物在工农业生产、生活中有着重要应用。
(1)烟气中的氮氧化物(NOx)可与甲烷在一定条件下反应转化为无害成分,从而消除污染。已知
| 反应 | 反应热(△H/kJ·mol-1) | 平衡常数(K) |
| CH4(g)+2O2(g)═CO2(g)+2H2O(l) | a | K1 |
| N2(g)+O2(g)═2NO(g) | b | K2 |
则 CH4 脱硝的热化学方程式为 CH4 (g) + 4NO (g)⇌CO2 (g) + 2N2 (g) + 2H2O ΔH=_________kJ/mol(用 a、b 表示);平衡常数 K3=_________(用 K1、K2 表示)。
(2)用活性炭还原法可以消除NO 的污染,发生的反应为C(s)+2NO(g)⇌N2(g)+CO2(g)。1molNO 和足量的活性炭在T℃、容积恒定为2L的密闭容器中反应,经过5min反应达到平衡,测得NO的物质的量为0.4mol。
①从反应开始到5min,用氮气表示的平均反应速率为_________。达到平衡后,向容器中再通入0.1molNO气体和0.3molCO2气体,则此平衡将_________(填“正向移动”“不移动”或“逆向移动”)。
②能判断该反应一定达到化学平衡状态的依据是_________(填标号)。
a.NO和N2的体积比保持不变
b.单位时间内生成2nmolNO的同时消耗nmolCO2
c.恒温恒容条件下,反应体系的压强不再发生改变
d.恒容条件下,混合气体的平均相对分子质量不变
(3)某实验小组模拟4CO(g)+2NO2(g) ⇌4CO2(g)+N2(g) ΔH=-1200kJ·mol-1净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙(填“>、=、<或不确定”)
| 甲 | 乙 |
| 0.2molNO2 | 0.1molNO2 |
| 0.4molCO | 0.2molCO |
-
研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:NO NO2
NO2 N2
N2
已知:NO(g)+O3(g)===NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
2NO(g)+O2(g)===2NO2(g) ΔH=-116.2 kJ·mol-1
则反应Ⅰ的热化学方程式为___________________________________________________________。
(2)有人设想将CO按下列反应除去:2CO(g)===2C(s)+O2(g) ΔH>0,请你分析该设想能否实现?________(填“能”或“否”),依据是_________________________________________。
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。已知常温时,甲酸的电离平衡常数Ka=1.70×10-4。
①甲酸钠的水溶液呈碱性,请用离子方程式表示其原因________________________________________。
②向20 mL 0.1 mol·L-1的甲酸钠溶液中滴加10 mL 0.1 mol·L-1的盐酸,混合液呈________(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序为_________________________________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.100 0 mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
| 温度 | 固体活性炭/mol | NO/mol | A/mol | B/mol |
| 200 ℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
| 335 ℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为________(填“吸热”或“放热”)反应。
②200 ℃时,平衡后向恒容容器中再充入0.1 mol NO,再次平衡后,NO的百分含量将________(填“增大”“减小”或“不变”)。
③计算反应在335 ℃时的平衡常数为________。
-
氮氧化物具有不同程度的毒性,利用构成电池方法既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,发生反应 6NO2+ 8NH3= 7N2+12H2O,装置如图所示。下列关于该电池的说法正确的是
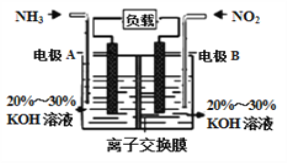
A. 为使电池持续放电,离子交换膜需选用阴离子交换膜
B. 电子从右侧电极经过负载后流向左侧电极
C. 电极A极反应式为2NH3 - 6e-=N2 +6H+
D. 当有4.48LNO2被处理时,转移电子物质的量为 0.8mol
-
C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)目前工业上有一种方法是用CO,和H2在230℃,催化剂条件下转化生成甲醇蒸汽和水蒸气。
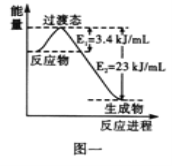
图一表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图。写出该反应的热化学方程式_____________。
(2) “亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO4溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图二所示。
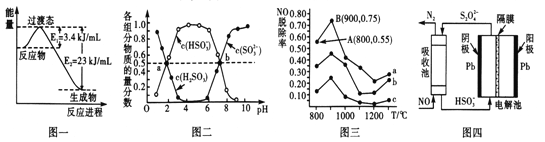
请写出a点时n(HSO3-):n(H2SO3)=______,b点时溶液pH=7,则n(NH4+):n(HSO3-)=___。
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO 5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图三所示:
5N2+ 6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:l、3:l、1:3时,得到NO脱除率曲线如图三所示:
① 请写出N2的电子式________。
② 曲线c对应NH3与NO的物质的量之比是______。
③ 曲线a中NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_____mg/(m3·s)。
(4)间接电化学法可除NO。其原理如图四所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性):_________________。
-
“绿水青山就是金山银山”,现今“环境保护”意识深入人心。氮的氧化物是大气主要污染物,研究氮氧化物间的相互转化及脱除,让空气更加清洁是环境科学的重要课题。
(1)已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步 2NO(g) N2O2(g) (快速平衡)
N2O2(g) (快速平衡)
第二步 N2O2(g)+O2(g)=2NO2(g) (慢反应)
①用O2表示的速率方程为v(O2)=k1·c2(NO)·c(O2);NO2表示的速率方程为v(NO2)=k2·c2(NO)·c(O2),k1与k2分别表示速率常数(与温度有关),则 _________。
_________。
②下列关于反应2NO(g)+O2(g)=2NO2(g)的说法正确的是_________(填序号)。
A.增大压强,反应速率常数一定增大
B.第一步反应的活化能大于第二步反应的活化能
C.反应的总活化能小于第一步和第二步反应的活化能之和
(2)已知:反应N2(g)+O2(g) 2NO(g) ΔH=+180.0 kJ·mol-1,CO的燃烧热ΔH=-283.5 kJ·mol-1,某脱硝反应的平衡常数表达式为
2NO(g) ΔH=+180.0 kJ·mol-1,CO的燃烧热ΔH=-283.5 kJ·mol-1,某脱硝反应的平衡常数表达式为 ,则该反应的热化学方程式为_________________________。
,则该反应的热化学方程式为_________________________。
(3)用活性炭还原法也可以处理氮氧化物,某研究小组在2 L的恒容密闭容器中加入3 mol活性炭和2 mol NO2,发生反应2C(s)+2NO2(g) N2(g)+2CO2(g),60 min后,体系达到平衡状态,此时气体的压强变为原来的1.3倍,请回答下列问题。
N2(g)+2CO2(g),60 min后,体系达到平衡状态,此时气体的压强变为原来的1.3倍,请回答下列问题。
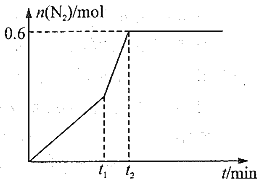
①该反应在0~60 min的平均反应速率v(N2)=_________。
②相同条件下进行上述反应,若在t1时刻,只改变一种条件,所得N2的物质的量随时间的变化如图所示,则,t1时刻改变的条件是_________(填选项编号A.加压 B.加入催化剂 C.升温 D.降温 E.通入NO2),t2_________60 min(填“大于”、“小于”或“等于”)
③已知:升高温度,该反应的平衡常数减小,则该反应正向是_________反应。(填“吸热”或“放热”)保持温度不变,改为恒压容器发生该反应,达平衡后,NO2的转化率_________(填“增大”、“减小”或“不变”,下同),K值_________。
-
C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)目前工业上有一种方法是用CO2和H2在230℃,催化剂条件下转化生成甲醇蒸汽和水蒸气。图一表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图。写出该反应的热化学方程式__________________________________________________。
(2)NH3催化还原可以消除氮的氧化物的污染。
①相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g)⇋5N2(g)+6H2O(g)反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是___________

A.催化剂的催化效率:a>b>c
B.X点时,NH3的化学反应速率为0.5mol·L-1·min-1
C.达到平衡时,使用催化剂c时NO的转换率最小
D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡
②恒温恒容下,向容积为1.0L的密闭容器中充入1.8molNH3和2.4molNO,在一定条件下发生反应,达到平衡时平衡体系的压强为反应前压强的22/21倍,则化学平衡常数K=__________mol/L(保留两位有效数字)。若上述反应改在恒温恒压条件下进行,则反应达到平衡时NH3的体积分数__________(填变大、变小或不变)
(3)在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)⇋zC(g),平衡时测得A的浓度为0.3mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.18mol/L,则A的转化率__________(填变大、变小或不变),C的体积分数__________(填变大、变小或不变)
 5N2 ( g) + 6H2O(g) △H = -1804 kJ•mol-1
5N2 ( g) + 6H2O(g) △H = -1804 kJ•mol-1 2NO2(g) △H = +67.8 kJ•mol-1
2NO2(g) △H = +67.8 kJ•mol-1 2 NO2 (g) △H =-116.2 kJ•mol-1
2 NO2 (g) △H =-116.2 kJ•mol-1



 b.
b. c.
c.







