-
氢能被视为最具发展潜力的清洁能源,开发新型储氢材料是氢能利用的重要研究方向。请回答下列问题:
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
(1)基态B原子的价电子排布式为_____,B、C、N、O第一电离能由大到小的顺序为_____,CH4、NH3、CO2的键角按照由大到小的顺序排列为_____。
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
(1)印度尼赫鲁先进科学研究中心的Datta和Pati等人借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。
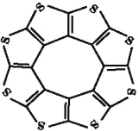
①S的基态原子中能量最高的电子,其原子轨道呈_____形。
②C16S8与H2微粒间的作用力是_____。
③C16S8分子中C原子和S原子的杂化轨道类型分别为_____。
-
氢能被视为21世纪最具发展潜力的清洁能源,其开发利用是科学家们研究的重要课题。试回答下列问题:
(1)与化石燃料相比,氢气作为燃料的优点是_________(至少答出两点)。
(2)与氢气直接燃烧相比较,设计成镍氢电池可以大大提高能量的转换率,在镍氢电池充电过程中储氢合金(M)吸氢转化为MH2,总反应为:xNi(OH)2+M xNiOOH+MHx,试写出放电过程中负极
xNiOOH+MHx,试写出放电过程中负极
反应式____________。
(3)施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,已知NaBH4与水反应后所得溶液显碱性,溶液中各离子浓度大小关系为__________,用离子方程式表示出溶液显碱性的原因_______________。
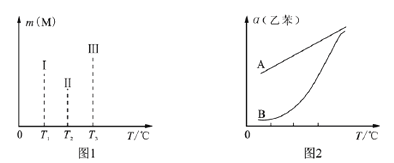
(4)在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中,分别放入ag的储氢合金(M)和bmol氢气发生如下反应:2M(s)+xH2(g) 2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___________,当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是______。
2MHx(s) ΔH<0,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___________,当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是______。
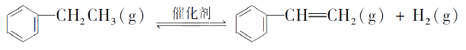
(5)储氢还可以借助有机物,如利用乙苯与苯乙烯之间的可逆反应来实现脱氢和加氢;
①在恒容密闭容器中,控制不同温度进行乙苯的脱氢实验。以乙苯起始浓度均为c mol/L测定乙苯的转化率,结果如图2所示。图中A为乙苯的平衡转化率与温度关系曲线,B曲线表示不同温度下反应经过相同时间且为达到化学平衡时乙苯的转化率。试说明随温度的升高,曲线B向曲线A逼近的原因__________。
②维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转换率为a,则在该温度下反应的平衡常数K=__________(用a等符号表示)。
-
开发新型储氢材料是氢能源利用的重要研究方向之一。请回答以下问题:
(1)Ti(BH4)3是一种储氢材料, 可由TiCl4和LiBH4反应制得。
①基态Ti3+的电子排布式为____________________;LiBH4中Li、B、H 元素的电负性由大到小的排列顺序为_________________。
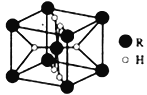
②另有一种含钛元素的新型材料,其理论结构模型如图所示,图中虚线框内碳原子的杂化轨道类型为____________。
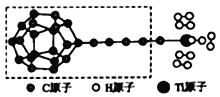
(2)氨硼烷(NH3BH3)是优良的储氢材料,少量氨硼烷可以由硼烷(B2H6)和NH3合成。
①NH3BH3中是否存在配位键__________(填“是”或“否”);与NH3BH3互为等电子体的分子的化学式为__________。
②B、C、N 与O元素的第一电离能由大到小的顺序为___________________。
③氨硼烷在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则立方氮化硼晶体可用作___________(选填下列字母序号)。
a.切削工具 b.钻探钻头 c.导电材料 d.耐磨材料
(3)一种有储氢功能的铜合金晶体具有面心立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。
①若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式为________________;
②铜与其它许多金属及其化合物都可以发生焰色反应,其原因是_______________。
(4)金属氢化物也是具有良好发展前景的储氢材料。某储氢材料是短周期金属元素R的氢化物。R的部分电离能如下表所示:
| I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
①该金属元素是___________(填元素符号)..
②若氢化物的晶胞结构如图所示(有4 个H原子位于面上,其余H原子位于晶胞内),已知该晶体的密度为ρg·cm-3,则该晶胞的体积为__________cm3[用含ρ、NA的代数式表示(其中NA为阿伏加德罗常数的值)]。
-
氢能是极具发展潜力的清洁能源,氢气的开发和综合利用是目前全球重要的科研项目之一。回答下列问题:
(1)T℃时,向体积均为1L的甲、乙两个恒容容器中分别加入足量碳和0.1molH2O(g),发生反应:H2O(g)+C(s)⇌CO(g)+H2(g) △H>0。甲容器控制绝热条件,乙容器控制恒温条件,两容器中压强随时间的变化如图所示。
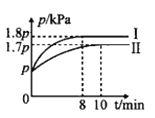
①图中代表甲容器的曲线为__(填“Ⅰ”或“Ⅱ”)。
②下列关于甲容器反应体系的说法错误的是__。
A.当水蒸气的体积分数不再发生变化,反应达到平衡状态
B.从密闭容器中分离出部分固体碳,H2的体积分数减小
C.缩小容器体积,平衡逆向移动,平衡常数减小
D.向平衡体系中充入少量水蒸气,再次平衡后,容器中c(CO)增大
③乙容器中,从反应开始到达平衡,v(H2O)=__mol•L-l•min-l;T℃下,该反应的平衡常数Kp=___(用含p的代数式表示)。
(2)对于反应aA(g)+bB(g)⇌cC(g)+dD(g),速率方程v═kcm(A)•cn(B),k为速率常数(只受温度影响),m+n为反应级数。已知H2(g)+CO2(g)⇌CO(g)+H2O(g),CO的瞬时生成速率=kcm(H2)•c(CO2)2。一定温度下,控制CO2起始浓度为0.25mol•L-1,改变H2起始浓度,进行以上反应的实验,得到CO的起始生成速率和H2起始浓度呈如图所示的直线关系。
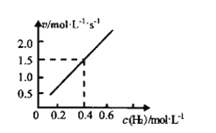
①该反应的反应级数为__。
②速率常数k=__。
③当H2的起始浓度为0.2mol•L-1,反应进行到某一时刻时,测得CO2的浓度为0.2mol•L-1,此时CO的生成瞬时速率v=__mol•L-l•s-1。
-
开发新型储氢材料是开发利用氢能的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为 ______,该电子层具有的原子轨道数为 _______。
②Li、B、H元素的电负性由大到小的排列顺序为 ___________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+ ___________(填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
| 
| 
| 
| 
| 
|
| 738 | 1451 | 7733 | 10540 | 13630 |
则M是 ______________ (填元素名称)。
-
新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是 ,B原子的杂化轨道类型是 .
Li、B、H元素的电负性由大到小排列顺序为 .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是 (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为 ,NaH的理论密度是 g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
-
新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是 ,B原子的杂化轨道类型是 .
Li、B、H元素的电负性由大到小排列顺序为 .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是 (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为 ,NaH的理论密度是 g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
-
新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为,该能层具有的原子轨道数为_________。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是,Li、B、H元素的电负性由大到小排列顺序为_________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+_________H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是_________(填元素符号)。
-
新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高电子层符号为__________,该电子层具有的原子轨道数为______.
②LiBH4由Li+和BH 构成,BH
构成,BH 的立体构型是______,B原子的杂化轨道类型是_______.
的立体构型是______,B原子的杂化轨道类型是_______.
③Li、B元素的电负性由小到大的顺序为_______________________.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+________H-(填“>”“=”或“<”).
②某储氢材料是短周期金属元素M的氢化物. M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1 451 | 7 733 | 10 540 | 13 630 |
M是________族元素.
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488 pm,Na+半径为102 pm,H-的半径为142pm,NaH的理论密度是________g·cm-3.(仅写表达式,不计算)
-
开发新型储氢材料是氢能利用的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有__个.
②LiBH4由Li+和BH4﹣构成,BH4﹣呈正四面体构型.LiBH4中不存在的作用力有__(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
③由BH4﹣结构可知Li,B,H元素的电负性由大到小排列顺序为__.
(2)金属氢化物是具有良好发展前景的储氢材料.
LiH中,离子半径:Li+__H﹣(填“>”、“=”或“<”).






