低温脱硫技术可用于处理废气中的氮氧化物。发生的化学反应为:
4NH3(g) + 6NO(g) 5N2(g) + 6H2O(g) ΔH<0
在恒容密闭容器中,下列有关说法正确的是:
A.平衡时,其他条件不变,降低温度可使该反应的平衡常数减小
B.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
D.单位时间内消耗NH3和H2O的物质的量比为2∶3时,反应达到平衡
高三化学选择题中等难度题
低温脱硫技术可用于处理废气中的氮氧化物。发生的化学反应为:
4NH3(g) + 6NO(g) 5N2(g) + 6H2O(g) ΔH<0
在恒容密闭容器中,下列有关说法正确的是:
A.平衡时,其他条件不变,降低温度可使该反应的平衡常数减小
B.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
D.单位时间内消耗NH3和H2O的物质的量比为2∶3时,反应达到平衡
高三化学选择题中等难度题
低温脱硫技术可用于处理废气中的氮氧化物。发生的化学反应为:
4NH3(g) + 6NO(g) 5N2(g) + 6H2O(g) ΔH<0
在恒容密闭容器中,下列有关说法正确的是:
A.平衡时,其他条件不变,降低温度可使该反应的平衡常数减小
B.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
D.单位时间内消耗NH3和H2O的物质的量比为2∶3时,反应达到平衡
高三化学选择题中等难度题查看答案及解析
低温脱硫技术可用于处理废气中的氮氧化物。发生的化学反应为:
4NH3(g) + 6NO(g) 5N2(g) + 6H2O(g) ΔH<0
在恒容密闭容器中,下列有关说法正确的是:
A.平衡时,其他条件不变,降低温度可使该反应的平衡常数减小
B.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
D.单位时间内消耗NH3和H2O的物质的量比为2∶3时,反应达到平衡
高三化学选择题中等难度题查看答案及解析
低温脱硫技术可用于处理废气中的氮氧化物。发生的化学反应为:
2NH3(g) + NO(g) 2N2(g) + 3H2O(g) ΔH<0
在恒容密闭容器中,下列有关说法正确的是
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
高三化学单选题中等难度题查看答案及解析
为有效提升空气质量,国家强制各燃煤企业要对燃媒烟气进行脱硫、脱硝处理后排放。回答下列问题:
(1)燃煤烟气“脱硝”中涉及到的部分反应如下:
a.4NH3(g)+6NO(g)5N2(g)+6H2O(g)△H1
b.4NH3(B)+5O2(g)4NO(g) +6H2O(g) △H2=-925 kJ·mol-1
c.N2(g)+O2(g)2NO(g) △H3=+175kJ·mol-1
则△H1=_________kJ·mol-1。
(2)向某恒容密闭容器中加入2molNH3、3molINO,在适当条件下发生(1)中反应a,反应过程中NO的平衡转化率随温度T、压强p的变化曲线如图1所示:

①p1_________p2(填 “>”“ <” 或“=”)。
②若在压强为p2、温度为600℃时,达到平衡时反应体系内化学能降低了300kJ,则NO的转化率为_________。
③600℃时,下列各项数据中能表明该反应已达到化学平衡状态的是_________(填标号)。
a.水与NO的生成速率相等 b.混合气体的密度保持不变
c.NH3、N2生成速率比为5∶4 d.容器的总压强保持不变
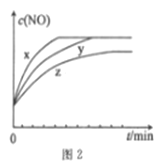
(3)将2molN2、3molH2O(g)、0.5molNO的混合气体置于x、y、z三个容积相同的恒容密闭容器中,控制适当的条件发生反应,反应过程中c(NO)随时间的变化如图2所示。
①在建立平衡的过程中,三个容器中反应速率的相对大小为______________。
②与y容器中反应相比,z容器中反应改变的条件及判断依据分别是____________________________。
(4)2000℃下,在一个2L的密闭容器里发生(1)中反应c,起始时氮气和氧气的浓度均为0.69 mol·L-1,达到平衡时NO的浓度为0.18 mol·L-1,期2000℃时该反应的平衡常数K=__________。
(5)将NO、NO2用NaOH溶液吸收也可消除氮氧化物污染,适当比例的NO、NO2通入NaOH溶液中可得到一种盐X,则该盐的化学式为_________。
高三化学综合题中等难度题查看答案及解析
用NH3催化还原氮的氧化物,可以消除氮的氧化物的污染。已知:
反应①:4NH3(g)+ 6NO(g)5N2(g) + 6H2O(l)
反应②:2NO(g) + O2(g) 2NO2(g)
(
< 0且
=2
)
反应③:4NH3(g) + 6NO2(g) 5N2(g)+ 3O2 + 6H2O(l)
反应①和反应②在不同温度时的平衡常数及其大小关心如下表:

(1)试推测反应③是______ 反应(填“吸热”或“放热”)。
(2)相同条件下反应①在2L的密闭容器中选用不同的催化剂,反应产生N2的物质的量随时间的变化如右图所示。
则:①计算0~4min时在A催化剂作用下,反应速率v(NO)=_______________
②下列说法正确的是:________________________
A.该反应的活化能大小顺序是:Ea(A)>Ea(B) >Ea(C)
B.增大压强能使反应速率加快的原因,是因为增加活化分子的百分数
C.单位时间内H-O键与N-H断裂的数目相等时,说明反应已达平衡状态
D.若在恒容绝热的密闭容器中进行,当温度不变时,说明反应已达平衡状态
(3)对于反应②,若在某温度下,在容积为2L的刚性密闭容器中起始加入2 molNO 和2 molO2,反应一段时间后,测的生成NO21.6mol,则该反应是否达到平衡状态?_________(填“是”或“不是”已知该温度下该反应的K约为147.3).达平衡后,在同一温度下向大小相同的另一刚性容器中加入1.2mol的NO2和1.5mol的O2,则还要加入NO______mol、O2_____mol,达平衡时各物质的浓度才能跟前平衡的相等。
高三化学简答题中等难度题查看答案及解析
用NH3催化还原氮的氧化物,可以消除氮的氧化物的污染。已知:
反应①:4NH3(g)+ 6NO(g)5N2(g) + 6H2O(l) △H1
反应②:2NO(g) + O2(g)2NO2(g) △H2(△H2<0且
)
反应③:4NH3(g) + 6NO2(g)5N2(g)+ 3O2 + 6H2O(l) △H3
反应①和反应②在不同温度时的平衡常数及其大小关心如下表:

(1)试推测反应③是______ 反应(填“吸热”或“放热”)
(2)相同条件下反应①在2L的密闭容器中选用不同的催化剂,反应产生N2的物质的量随时间的变化如图所示。

则:
①计算0~4min时在A催化剂作用下,反应速率v(NO)=__________。
②下列说法正确的是:__________________。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B) >Ea(C)
B.增大压强能使反应速率加快的原因,是因为增加活化分子的百分数
C.单位时间内H-O键与N-H断裂的数目相等时,说明反应已达平衡状态
D.若在恒容绝热的密闭容器中进行,当温度不变时,说明反应已达平衡状态
(3)对于反应②,若在某温度下,在容积为2L的刚性密闭容器中起始加入2 molNO和2 molO2,反应一段时间后,测的生成NO21.6mol,则该反应是否达到平衡状态?_______(填“是”或“不是”。已知该温度下该反应的K约为147.3)。达平衡后,在同一温度下向大小相同的另一刚性容器中加入1.2mol的NO2和0.9mol的O2,则还要加入NO______mol、O2_____mol,达平衡时各物质的浓度才能跟前平衡的相等。
高三化学简答题中等难度题查看答案及解析
已知:用NH3催化还原NOx时包含以下反应。
反应①:4NH3(g) + 6NO(g) 5N2(g) + 6H2O(l) ∆H1 = -1807.0kJ•mol-1
反应②:4NH3(g) + 6NO2(g) 5N2(g) + 3O2(g) + 6H2O(l) ∆H2 = ?
反应③:2NO(g) + O2(g) 2NO2(g) ∆H3 = -113.0kJ•mol-1
(1)反应②的∆H2 =_________________________。 反应①②在热力学上趋势大,其原因是___________________________________________________________________。
(2)为探究温度及不同催化剂对反应①的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得N2浓度变化情况如下图所示。

①反应①的平衡常数的表达式K=__________。在催化剂甲的作用下反应的平衡常数_______________在催化剂乙的作用下反应的平衡常数(填写“大于”,“小于”或“等于”)。
②N点后N2浓度减小的原因可能是_________________、 ________________。
(3)某温度下,在1L容器中对于反应①初始投入4molNH3和6molNO,当气体总物质的量为7.5mol时反应达到平衡,则NH3的转化率_______________% ,达平衡所用时间为5分钟,则用NO表示此反应平均反应速率为__________________。
高三化学综合题困难题查看答案及解析
利用低温技术可用于处理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:
 ,有关说法正确的是
,有关说法正确的是
A.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
B.平衡时,其他条件不变,增加的浓度,废气中NO的转化率减小
C.单位时间内生成和
的物质的量比为2:3时,反应达到平衡
平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
高三化学选择题中等难度题查看答案及解析
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O
在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
高三化学选择题简单题查看答案及解析
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O
在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
高三化学选择题简单题查看答案及解析