-
(16分) 在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。则:
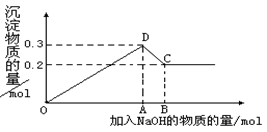
(1)写出代表各线段发生反应的离子方程式:
OD段________,_________________________________,
DC段_。
(2)原溶液中Mg2+、Al3+物质的量浓度之比为________。
(3)图中C点表示当加入________mol NaOH时,Al3+已经转化为 Mg2+已经转化为________。
(4)图中线段OA∶AB=________。
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。下列说法错误的( )
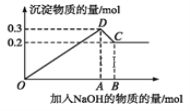
A.C点溶液中溶质为偏铝酸钠和氯化钠
B.原溶液中Mg2+、Al3+的物质的量浓度之比为 2∶1
C.C点加入0.8mol NaOH
D.图中线段OA∶AB=5∶1
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
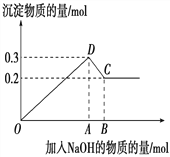
(1)写出代表下列线段发生的反应的离子方程式:
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量之比为_____________。
(3)图中B点时所加入溶液中含NaOH为________mol
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为________________________________。
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。

(1)写出下列线段内发生反应的离子方程式:
OD段_________________________,
CD段_________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为____________。
(3)图中C点横坐标为_______ 。
(4)图中线段OA∶AB=____________。
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
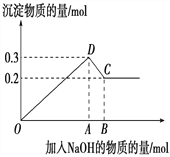
(1)写出代表下列线段发生的反应的离子方程式:
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量之比为_____________。
(3)图中B点时所加入溶液中含NaOH为________mol
(4)若向50 mL 2 mol·L-1的AlCl3溶液中加入100 mL KOH溶液,充分反应后得到3.12g沉淀。则KOH的物质的量浓度可能为________________________________。
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
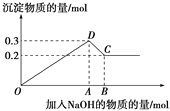
(1)写出代表各线段发生的反应的离子方程式:
OD段________________________________________________,
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为________。
(3)图中C点表示当加入______mol NaOH时,Al3+已经转化为_____,Mg2+已经转化为______。
(4)图中线段OA∶AB=________。
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。
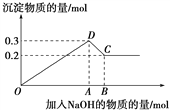
(1)写出代表各线段发生的反应的离子方程式:
OD段________________________________________________,
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为________。
(3)图中C点表示当加入______mol NaOH时,Al3+已经转化为_____,Mg2+已经转化为______。
(4)图中线段OA∶AB=________。
【答案】 Mg2++2OH-===Mg(OH)2↓、Al3++3OH-===Al(OH3)↓ Al(OH)3+OH-==AlO2-+2H2O 2∶1 0.8 AlO Mg(OH)2 7∶1
Mg(OH)2 7∶1
【解析】试题分析:(1)OD段镁离子和铝离子全部转化为沉淀,其离子方程式为Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓;DC段NaOH过量时氢氧化铝溶解,其离子方程式为:Al(OH)3+OH-═AlO2-+2H2O。
(2)由图象可知,0~A发生Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,A~B发生Al(OH)3+OH-═AlO2-+2H2O,C点对应的沉淀为Mg(OH)2,D点对应的沉淀为Mg(OH)2和Al(OH)3,则Mg(OH)2的物质的量为0.2mol,Al(OH)3的物质的量为0.3mol-0.2mol=0.1mol,由Mg(OH)2~Mg2+、Al(OH)3~Al3+,溶液的体积相同,浓度之比等于物质的量之比,所以原溶液中Mg2+、Al3+物质的量浓度之比为0.2mol:0.1mol=2:1。
(3)由Mg2++ 2OH-═Mg(OH)2↓
0.2mol 0.4mol
Al3++ 3OH- ═Al(OH)3↓
0.1mol 0.3mol
Al(OH)3+OH-═AlO2-+2H2O
0.1mol 0.1mol
则C点NaOH的物质的量为0.4mol+0.3mol+0.1mol=0.8mol,此时铝离子完全转化为AlO2-,镁离子完全转化为Mg(OH)2沉淀。
(4)0~A发生Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,A~B发生Al(OH)3+OH-═AlO2-+2H2O,则线段OA对应的NaOH的物质的量为0.4mol+0.3mol=0.7mol,线段AB对应的NaOH的物质的量为0.1mol,所以线段OA:AB=0.7mol:0.1mol=7:1。
考点:本题考查离子反应及其计算、图像的分析。
【题型】填空题
【结束】
25
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
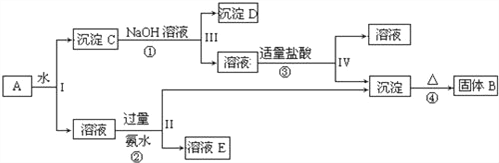
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
-
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示.则:
(1)原溶液中Mg2+、Al3+物质的量浓度之比为______.
(2)图中C点表示当加入______molNaOH时,Al3+已经转变为______,Mg2+已经转变为______.
(3)图中线段OA:AB=______.
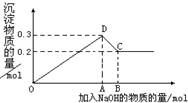
-
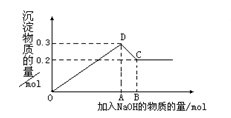
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如右图所示。则:
(1)原溶液中Mg2+、Al3+物质的量浓度之比为___________。
(2)图中C点表示当加入______molNaOH时,Al3+已经转变为_______,Mg2+已经转变为_________。
(3)图中线段OA∶AB=___________。
-
在MgCl2和AlCl3的混合液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。
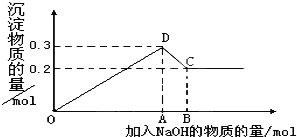
(1)写出下列线段内发生反应的方程式:
OD段__________________________________。
CD段__________________________________。
(2)图中C点表示加入________mol NaOH时。
(3)原溶液中来自MgCl2、AlCl3 的氯离子物质的量浓度之比为_____________。
(4)图中线段OB:OA=_________。

Mg(OH)2 7∶1









