将CoCl2溶解于盐酸中可以形成CoCl,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
B.升高温度,正反应速率增大,逆反应速率减小
C.该反应的平衡常数K=
D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色
高二化学选择题简单题
将CoCl2溶解于盐酸中可以形成CoCl,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
B.升高温度,正反应速率增大,逆反应速率减小
C.该反应的平衡常数K=
D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色
高二化学选择题简单题
将CoCl2溶解于盐酸中可以形成CoCl,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
B.升高温度,正反应速率增大,逆反应速率减小
C.该反应的平衡常数K=
D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色
高二化学选择题简单题查看答案及解析
将CoCl2溶解于盐酸中可以形成CoCl42—,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq)CoCl42—(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小
B.该反应的平衡常数
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小
高二化学选择题简单题查看答案及解析
将CoCl2溶解于盐酸中可以形成CoCl42-,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl42-(aq) ΔH>0
粉红色 蓝色
下列说法正确的是
A. 升高温度,正反应速率增大,逆反应速率减小
B. 该反应的平衡常数K=c(CoCl42-)/[c(Co2+)c4(Cl-)]
C. 将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D. 增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小
高二化学单选题中等难度题查看答案及解析
将CoCl2溶解于盐酸中可以形成,在溶液中存在下面的化学平衡:
下列说法正确的是
A.升高温度,正反应速率增大,逆反应速率减小
B.该反应的平衡常数K=[] / [ Co2+][ Cl-]4
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小
高二化学选择题中等难度题查看答案及解析
高二化学填空题中等难度题查看答案及解析
将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为Co2+(aq)+Cd(s)===Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如图的原电池,则下列说法一定错误的是( )
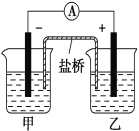
A. Cd作负极,Co作正极
B. 原电池工作时,电子从负极沿导线流向正极
C. 甲池中盛放的是CdCl2溶液,乙池中盛放的是CoCl2溶液
D. 盐桥中装有含氯化钾的琼脂,其作用是传递电子
高二化学单选题中等难度题查看答案及解析
把CoCl2溶于水后加氨水直接先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]Cl2,此时向溶液中通入空气,得到的产物中有一种其组成可以用CoCl2·5NH3表示,Co配位数是6,.把分离出的CoCl2·5NH3溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1 mol CoCl2·5NH3只生成1 molAgCl。下列说法正确的是( )
A. 产物中CoCl2·5NH3的配体NH3为分子和氯原子
B. 通入空气后得到的还原产物含有[Co(NH3)6]Cl2
C. [Co(NH3)6]Cl2中心离子的价电子排布式为3d4s2
D. [Co(NH3)6]Cl2中含有配位键,极性共价键,离子键
高二化学单选题困难题查看答案及解析
氯化钴溶液中存在下列平衡:CoCl42-(蓝色)Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
A.由蓝色变为粉红色 B.红色加深
C.由粉红色变为蓝色 D.蓝色加深
高二化学选择题中等难度题查看答案及解析
把CoCl2溶于水后加氨水直接先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]Cl2,此时向溶液中通入空气,得到的产物中有一种其组成可以用CoCl3•5NH3表示,Co配位数是6,把分离出的CoCl3•5NH3溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1mol CoCl3•5NH3只生成2molAgCl.下列说法错误的是( )
A. 产物中CoCl3•5NH3的配位体为氨分子和氯离子
B. 通入空气后得到的溶液含有[Co(NH3)5Cl]2+
C. [Co(NH3)6]Cl2中心离子的价电子排布式为3d54s2
D. [Co(NH3)6]Cl2中含有配位键,极性共价键,离子键
高二化学单选题中等难度题查看答案及解析
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。回答下列问题:
(1)装置中安全管的作用原理是___。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用___式滴定管,可使用的指示剂为___。
(3)样品中氨的质量分数表达式为___。
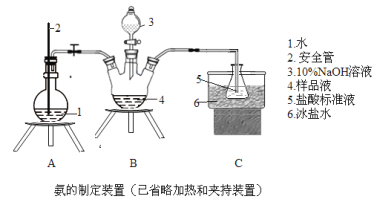
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___(填“偏高”或“偏低”)。
(5)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1,c(CrO42-)为___mol·L-1。
(已知:Ksp(Ag2CrO4)=1.12×10-12)
(6)X的化学为[Co(NH3)6]Cl3。制备X的反应化学方程式为___。
高二化学实验题中等难度题查看答案及解析