-
常温下有浓度均为0.1 mol 的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
(1)有人称溶液①是油污的“清道夫”,原因是_____________________(用离子方程式解释)
(2)这四种溶液中水的电离程度由大到小的顺序是(用序号填写)______________________
(3)向④中加入少量氯化铵固体,此时 的值___________(填“增大”“减小”或“不变”)。
的值___________(填“增大”“减小”或“不变”)。
(4)等体积混合③和④的溶液,此时溶液中[NH4+]+[NH3·H2O]=_____________mol·L-1(填数值);此时溶液中离子浓度的大小顺序是:__________________________;若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积_________④的体积(填“大于”小于”或“等于”)
(5)将10 mL溶液③加水稀释至100 mL,则此时溶液中由水电离出的c( H+)=___________ mol·L-1。
-
Ⅰ.常温下有浓度均为0.1 mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
(1)这四种溶液中水的电离程度由大到小的顺序是___________________(用序号填写)。
(2)等体积混合③和④的溶液中离子浓度的大小顺序是:__________________________。
(3)②溶液中存在的质子守恒关系:c(OH-)=___________________________。
(4)向④中加入少量氯化铵固体,溶液中c(H+)______(填“增大”、“减小”或“不变”)
(5)取10mL溶液③,加水稀释到100mL,则该溶液中由水电离出的c(H+)约为 ________ 。
Ⅱ.普通泡沫灭火器内的玻璃筒里盛有Al2(SO4)3溶液,铁筒中盛有NaHCO3溶液,当意外失火时,打开泡沫灭火器使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为:______________________________________,不能把Al2(SO4)3溶液盛放在铁筒中的主要原因是______________________________________________________。
Ⅲ.某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
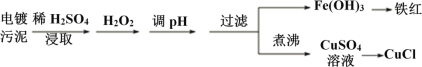
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是___________________,调pH的最适宜范围为__________。
(2)调pH过程中加入的试剂最好是___________(填标号)。
A. NaOH B. CuO C.NH3·H2O D.HCl
-
(10分)常温下有浓度均为0.05 mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O,回答相关问题:(1)上述溶液中,可发生水解的是 (填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液中,离子浓度大小的关系
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值 (“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积 ④的体积(“大于”、 “小于”或“等于”)
(5)取10 mL的③溶液,加水稀释到500 mL,则此溶液中由水电离出的c(H+)= mol/L
-
(10分)常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3・H2O(1)上述溶液中,可发生水解的是________(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度大到小的
顺序为________。
(3)向溶液④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值________(填增大、
减小、不变)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积④的体积(填
大于、小于、等于)。
(5)取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出的c(H+)=________。
-
常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是_________(序号)。
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液是________(化学式)。
(3)向④中加入少量NH4Cl固体,此时 的值__________(“增大”、“减小”或“不变” )。
的值__________(“增大”、“减小”或“不变” )。
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积_________④的体积(“大于”、“小于”或“等于” )。
-
(10分)常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3 ②NaHCO3
③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是________(填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液中,离子浓度大小的关系________
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值________(“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积________④的体积(“大于”、“小于”或“等于” )
(5)取10mL的③溶液,加水稀释到500mL,则此溶液中由水电离出的c(H+)=________mol/
-
(10分)常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是________(填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶
液中,离子浓度大小的关系________
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值________(“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积________④的体积(“大于”、“小于”或“等于” )
(5)取10mL的③溶液,加水稀释到500mL,则此溶液中由水电离出的c(H+) =________mol/L
-
(10分)常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是________(填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液中,离子浓度大小的关系________
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值________(“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积________④的体积(“大于”、“小于”或“等于” )
(5)取10mL的③溶液,加水稀释到500mL,则此溶液中由水电离出的c(H+)=________mol/L
-
常温下有浓度均为0.5 mol 的四种溶液:
的四种溶液:
①Na2CO3;②NaHCO3;③HCl;④NH3 H2O。
H2O。
(1)上述溶液中,可发生水解的是_____(填序号)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为_______。
(3)向溶液④中加入少量氯化铵固体,此时 的值_____(填“增大”“减小”或“不变”),c(OH-)变____(填“变大”“变小”或“不变”)
的值_____(填“增大”“减小”或“不变”),c(OH-)变____(填“变大”“变小”或“不变”)
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积____④的体积(填“大于”“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是___。
(5)取10 mL溶液③,加水稀释到500 mL,则该溶液中由水电离出的c(H+)=___。
-
(12分)常温下有浓度均为0.5 mol·L-1的四种溶液:①Na2CO3、②NaHCO3、③HCl、④NH3·H2O。
(1)上述溶液中,可发生水解的是_______(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为__________。
(3)向④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值________(填“增大”“减小”或“不变”)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是 ________ 。
(5)以10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
的值___________(填“增大”“减小”或“不变”)。
