-
(10分)碘在工农业生产和日常生活中有重要用途。
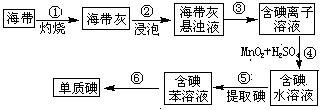
(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.冷凝管
步骤④发生反应的离子方程式为 。
若步骤⑤采用裂化汽油提取碘,后果是 。
(2)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为: IBr+H2O==HBr+HIO,下列有关IBr的叙述中错误的是: 。
A.固体溴化碘熔沸点较高
B.在许多反应中,溴化碘是强氧化剂
C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂
D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O
(3)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的碘以碘酸钾(KIO3)形式存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,请写出反应的离子方程式: 。
-
碘在工农业生产和日常生活中有重要用途。
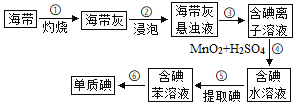
(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_____________(从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
步骤④发生反应的离子方程式为____________________________________。
(2)若步骤⑤采用裂化汽油提取碘,后果是__________________________。
(3)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为:IBr+H2O==HBr+HIO等,下列有关IBr的叙述中错误的是(____)。
A.固体溴化碘熔沸点较高
B.在许多反应中,溴化碘是强氧化剂
C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂
D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O
(4)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的碘以碘酸钾(KIO3)存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,下列说法正确的是(____)。
A.碘易溶于有机溶剂,可用酒精萃取碘水中的I2
B.检验加碘盐原理:IO3—+5I—+3H2O ===3I2+6OH—
C.在KIO3溶液中加入几滴淀粉溶液,溶液变蓝色
D.向某无色溶液中加入氯水和四氯化碳,振荡,静置,下层呈紫色,说明原溶液中有I—
-
碘在工农业生产和日常生活中有重要用途。
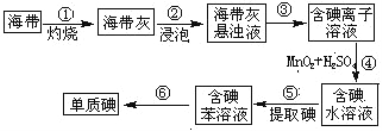
(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是____________________(从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
步骤④发生反应的离子方程式为______________________________________________。
若步骤⑤采用裂化汽油提取碘,后果是____________________________。
(2)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为:IBr+H2O==HBr+HIO,下列有关IBr的叙述中错误的是:________。
A.固体溴化碘熔沸点较高
B.在许多反应中,溴化碘是强氧化剂
C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂
D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O
(3)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的 碘以碘酸钾(KIO3)形式存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,下列说法正确的是___。
A.碘易溶于有机溶剂,可用酒精萃取碘水中的I2
B.检验加碘盐原理:IO3-+5I-+3H2O=3I2+6OH-
C.在KIO3溶液中加入几滴淀粉溶液,溶液变蓝色
D.向某无色溶液中加入氯水和四氯化碳,振荡,静置,下层呈紫色,说明原溶液中有I-
-
海带中含有丰富的碘。某研究性学习小组按下图所示实验流程提取海带中的碘。

回答下列问题:
(1)步骤①灼烧海带时,除三脚架外,还需要用到下列仪器中的________(填字母标号)。
A.烧杯
B.坩埚
C.蒸发皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是________。
(3)步骤④反应的离子方程式为____________________________。
(4)步骤⑤中,可以用苯来提取碘的理由是___________________,碘水溶液加入苯后,振荡、静止可观察到的实验现象为________。
(5)请设计实验检验提取碘后的水溶液中是否还有单质碘_______________。
-
(10分)海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
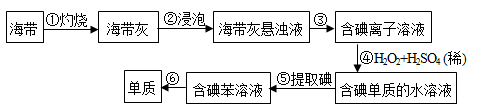
回答下列问题:
(1)步骤①灼烧海带时,除需要酒精灯、三脚架和坩埚钳外,还需要用到的实验仪器有 。
(2)步骤③的实验操作名称是 。
(3)步骤④反应的离子方程式是 。碘有极其重要的生理作用,缺乏碘会引起很多疾病。我国在居民食用盐中加入了一定量的含碘物质________以确保人体对碘的摄入量。
A.I2 B.KI C.KIO3 D.KIO4
(4)设计一种检验提取碘后的水溶液中是否还含单质碘的简单方法 。
-
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
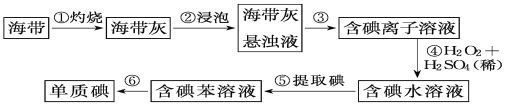
请填写下列空白:
(1)步骤①中灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___;___;___;___。
(2)步骤③的实验操作名称是__;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是__。
(3)步骤④反应的离子方程式是___。
(4)步骤⑤中,某同学选择用苯来提取碘的理由是___。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___。
-
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(图1):

(1)从上述步骤中可知,海带中含有的碘元素的主要存在形式是______.
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是______.
(3)步骤④中的转化还可以Cl2或双氧水,请分别写出反应的离子方程式:______、______.
(4)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出下列实验装置中(图2)的错误之处.
①______②______
进行上述蒸馏操作时,使用水浴的原因是______、______,最后晶态碘在______里聚集.
-
(10分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
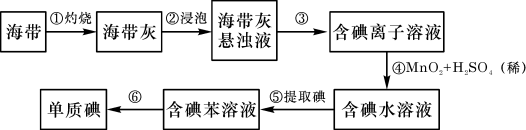
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是( )
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤⑤的仪器名称是 ;
(3)步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(4)若反应后有Mn2+步骤④反应的离子方程式是 。
(5)步骤⑤中,某学生选择用苯来提取碘的理由是 。
-
(14分)、海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
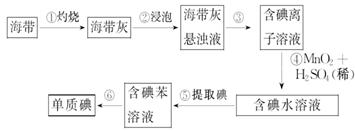
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是(从下列仪器中选出所需的仪器,用标号字母填写在横线处)。______________
A.烧杯 B.坩埚 C.表面皿 D.泥三角
E.酒精灯 F.干燥器 G.坩埚钳
(2)步骤③的实验操作名称是______________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是______________。
(3)在步骤④中MnO2 转变为Mn2+ 、I-转变为I2,请写出反应的离子方程式是___________________________________。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是___________________________________;_____________________________________________________________。
(5)、检验提取碘后的水溶液中是否还含有单质碘的试剂是:________________。
-
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
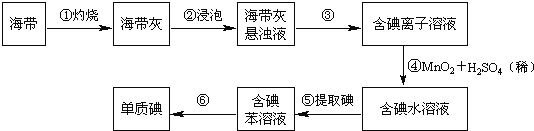
请填写下列空白:(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是(从下列仪器中选出所需的仪器,用标号字母填写在空白处)___________.
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_________.
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是________________________.
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法是:____________.









