-
以黄铁矿为原料生产硫酸的工艺流程图如下:
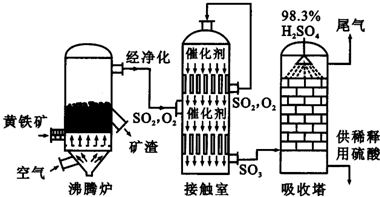
(1)将燃烧黄铁矿的化学方程式补充完整4______+11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
(2)接触室中发生反应的化学方程式是______△2SO3
-
以黄铁矿为原料生产硫酸的工艺流程图如下:
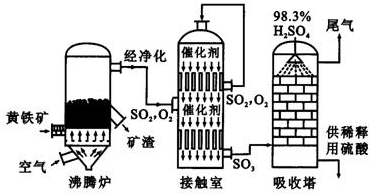
(1)将燃烧黄铁矿的化学方程式补充完整:4________+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)接触室中发生反应的化学方程式是________.
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)________.
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可制造水泥或制砖,含铁品位高的矿渣可炼铁
(4)每160g SO3气体与液态H2O化合放出260.6kJ的热量,该反应的热化学方程式是________.
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐.
①SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2的离子方程式是________.
②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量.铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变.计算:该铵盐中氮元素的质量分数是________%;若铵盐质量为15.00g,浓硫酸增加的质量为________.(计算结果保留两位小数)
-
以黄铁矿为原料生产硫酸的工艺流程图如下:

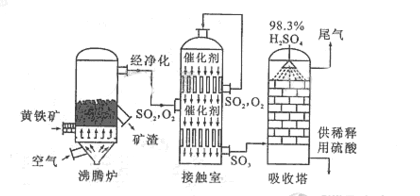
 (1)将燃烧黄铁矿的化学方程式补充完整
(1)将燃烧黄铁矿的化学方程式补充完整
4________+11
 (2)接触室中发生反应的化学方程式是。
(2)接触室中发生反应的化学方程式是。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)________。
 a. 为使黄铁矿充分燃烧,需将其粉碎
a. 为使黄铁矿充分燃烧,需将其粉碎
b. 过量空气能提高 的转化率
的转化率
 c. 使用催化剂能提高
c. 使用催化剂能提高 的反应速率和转化率
的反应速率和转化率
d. 沸腾炉排出的矿渣可供炼铁
 (4)每160g
(4)每160g 气体与
气体与 化合放出260.6kJ的热量,该反应的热化学方程是________。
化合放出260.6kJ的热量,该反应的热化学方程是________。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的 和铵盐。
和铵盐。
 ①
① 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 。
。 吸收
吸收 的离子方程式是________。
的离子方程式是________。
② 为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
 部分测定结果;
部分测定结果;
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
 计算:该铵盐中氮元素的质量分数是________%; 若铵盐质量为15.00g。 浓硫酸增加的质量为________。 (计算结果保留两位小数)
计算:该铵盐中氮元素的质量分数是________%; 若铵盐质量为15.00g。 浓硫酸增加的质量为________。 (计算结果保留两位小数)
-
以黄铁矿为原料生产硫酸的工艺流程图如下:

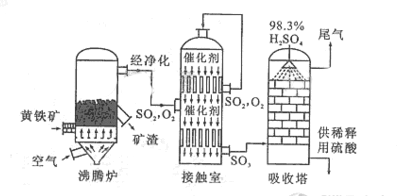
 (1)将燃烧黄铁矿的化学方程式补充完整
(1)将燃烧黄铁矿的化学方程式补充完整
4________+11
 (2)接触室中发生反应的化学方程式是。
(2)接触室中发生反应的化学方程式是。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)________。
 a. 为使黄铁矿充分燃烧,需将其粉碎
a. 为使黄铁矿充分燃烧,需将其粉碎
b. 过量空气能提高 的转化率
的转化率
 c. 使用催化剂能提高
c. 使用催化剂能提高 的反应速率和转化率
的反应速率和转化率
d. 沸腾炉排出的矿渣可供炼铁
 (4)每160g
(4)每160g 气体与
气体与 化合放出260.6kJ的热量,该反应的热化学方程是________。
化合放出260.6kJ的热量,该反应的热化学方程是________。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的 和铵盐。
和铵盐。
 ①
① 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的
既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 。
。 吸收
吸收 的离子方程式是________。
的离子方程式是________。
② 为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
 部分测定结果;
部分测定结果;
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
 计算:该铵盐中氮元素的质量分数是________%; 若铵盐质量为15.00g。 浓硫酸增加的质量为________。 (计算结果保留两位小数)
计算:该铵盐中氮元素的质量分数是________%; 若铵盐质量为15.00g。 浓硫酸增加的质量为________。 (计算结果保留两位小数)
-
以含硫铁矿石为原料生产硫酸的工艺流程图如下:
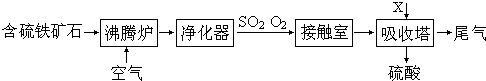
请回答下列问题:
(1)将燃烧含硫铁矿石的化学方程式补充完整:4______+11O2 2Fe2O3+8SO2.
2Fe2O3+8SO2.
充分煅烧含硫铁矿石Wg,反应完全后冷却至室温,称得固体物质的质量是mg,生成SO2为VL,则含硫铁矿石中硫元素的质量分数是(假设矿石中的杂质受热不分解,也不会与SO2反应)______.
A. B.
B. C.
C. D.
D.
(2)接触室中发生反应的化学方程式是______
-
(15分)以黄铁矿为原料生产硫酸的工艺流程图如下:
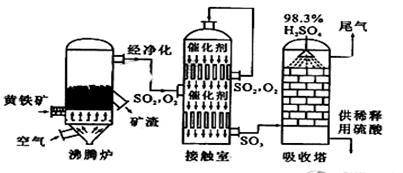
(1)写出燃烧黄铁矿的化学方程式________。
当有6mol SO2生成时,转移电子________mol。
(2)进入接触室的气体中含标准状态下1120m3SO2气体,达平衡后放出热量为4.728×106kJ,此时SO2转化率为96%。该反应的热化学方程式为________。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)________。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
e.吸收塔用水作吸收剂
(4)某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品充分灼烧,生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,再用0.02000 mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL。
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则样品中FeS2的质量分数是多少?(假设杂质不参加反应)
(5)该生产过程中产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是________。(填字母)
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液 D.氨水、酚酞
-
(18分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
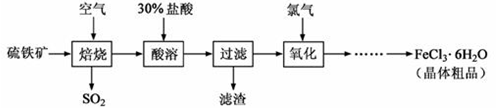
回答下列问题:
(1)将煅烧黄铁矿的化学方程式补充完整:________+________  Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 ________ 、 ________ ;
Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 ________ 、 ________ ;
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 ;
(3)通氯气氧化后时,发生的主要反应的离子方程式为 ;
(4)该过程产生的污染空气的气体有三种,尾气均可用强碱溶液吸收,这些反应的离子方程式为 ________ ;。
(5)从FeCl3溶液中得到FeCl3.6H2O晶体的操作为 ________ 。
-
【化学──选修2:化学与技术】
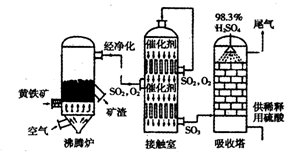
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:
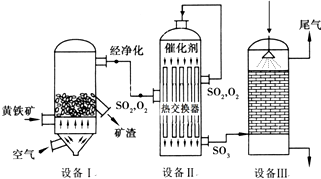
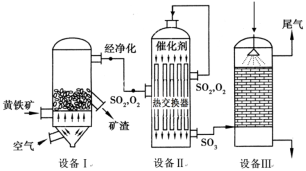 (1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。
(1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。
A.为使黄铁矿充分燃烧,需将其粉碎
B.过量空气能提高SO2的转化率
C.排出的矿渣可供炼铁
D.使用催化剂能提高SO2的化学反应速率和转化率
E.设备I生成的气体经净化的主要目的是防止催化剂中毒
F.热交换器的目的是使SO2的热量传递给SO3,有利于SO2的氧化和SO3的吸收
(2)设备Ⅰ的名称为 ,燃烧黄铁矿的化学方程式为 。
(3)设备Ⅱ为接触室,采用常压而不采用高压的原因是 。在生产中,为提高催化剂效率采取的措施有 。
(4)设备Ⅲ为吸收塔,从顶部喷淋 吸收SO3,得到 ,不用水吸收SO3是为了 。吸收塔中填充有许多瓷管,其作用是 。
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是 。
-
硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2+11O2  2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
2Fe2O3+8SO2;该反应中氧化剂和氧化产物的物质的量之比为______;标准状态下得到4.48升SO2时,一共转移了______mole-.
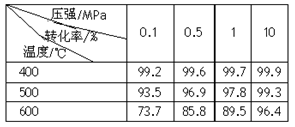
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:
压强/MPa
转化率/%
温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
根据上表回答,SO2转化到SO3的最佳反应条件是______.
A.400-500℃0.1MPa B.400℃10MPa
C.500℃10MPa D.400-500℃1MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:______.若在该条件下将2mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为______ (用含Q1、Q2代数式表示).
(4)市售浓硫酸的密度是1.84g/cm3、质量分数为98%,若用H2SO4•XH2O来表示这种浓硫酸,则X为______.
-
(14分) 硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2 + 11O2  2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
该反应中氧化剂和氧化产物之比为 ________;标准状态下得到4.48升SO2 时,一共转移了 ________mol e- 。(每空3分)
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的
最佳反应条件是________。(每空2分)
A.400-500℃ 0.1 MPa B.400℃ 10 MPa
C.500℃ 10 MPa D.400-500℃ 1 MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:________。若在该条件下将2 mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为________ (用含Q1、Q2代数式表示)。(每空2分)
(4)市售浓硫酸的密度是1.84 g / cm3、质量分数为98 % ,若用H2SO4· XH2O来表示这种浓硫酸,则X为________ 。(每空2分)
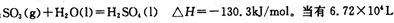 (已折算为标况下)SO3气体与H2O化合时放出的热量为________(保留两位有效数字)。
(已折算为标况下)SO3气体与H2O化合时放出的热量为________(保留两位有效数字)。








 (1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。
(1)依据工艺流程图判断下列说法不正确的是(选填序号字母)___________。