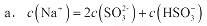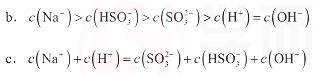-
直接排放含SO2的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关SO2性质的探究活动。

(1)装置A中反应的离子方程式为 。
(2)选用图1以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是 。
②丙同学设计的合理实验方案为:按照A→C →尾气处理(填字母)顺序连接装置。其中装置C的作用是 。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是 。

(3)利用如图2的装置A测残液中SO2的含量。量取10.00 mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL 0.1000 mol/L的KMnO4标准溶液吸收。充分反应后,再用0.2000 mol/L的KI溶液滴定过量的KMnO4,消耗KI溶液25.00 mL。
(已知:5SO2+2MnO4-+2H2O==2Mn2++5SO42-+4H+,10I-+2MnO4-+16H+==2Mn2++5I2+8H2O)
①该装置中仪器C的名称为 ,水通入C的进口为_____________。
②残液中SO2的含量为 mol·L-1。
-
直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。

(1)装置A中仪器a的名称为________。写出A中发生反应的离子方程式_________________________。若利用装置A 中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理_______________________________________。
(2)选用图中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是__________________________________。
②丙同学设计的合理实验方案为:按照A→C→______→F→尾气处理(填字母) 顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是____________________________。
③其中裝置C的作用是____________________________。
(3)为了测定装置A残液中SO2的含量,量取10.00mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL0.0500 mol·L-1的KMnO4溶液吸收。充分反应后,再用0.2000 mol·L-1的KI标准溶液滴定过量的KMnO4,消耗KI溶液20.00mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ 10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为____g·L-1。
②若滴定前读数时平视,滴定终点读数时俯视则测定结果________ (填“偏高”、“偏低”或“无影响”)。
【答案】 分液漏斗 CaSO3+2H+=Ca2++H2O+ SO2↑ SO2+2H2S=3S↓+2H2O 次氯酸在水溶液中能将SO2氧化,并非强酸制弱酸 B→E→D F中有沉淀后溶解,D不变色 除去挥发HCl 3.2 偏高
【解析】试题分析:(1)根据装置A分析仪器a的名称;A中亚硫酸钙与盐酸反应生成氯化钙、二氧化硫、水;SO2与H2S反应生成硫单质,能证明+4价的硫元素具有氧化性;(2)①次氯酸在水溶液中能将SO2氧化;②根据亚硫酸酸性大于碳酸、碳酸酸性大于次氯酸验证亚硫酸与次氯酸的酸性强弱;(3)①根据电子守恒计算SO2的含量;②若滴定前读数时平视,滴定终点读数时俯视,消耗KI溶液体积偏小;
解析:(1)装置A中仪器a的名称分液漏斗;A中亚硫酸钙与盐酸反应生成氯化钙、二氧化硫、水,反应的离子方程式是CaSO3+2H+=Ca2++H2O+ SO2↑;SO2与H2S反应生成硫单质,能证明+4价的硫元素具有氧化性,反应方程式是SO2+2H2S=3S↓+2H2O;次氯酸在水溶液中能将SO2氧化,并非强酸制弱酸。所以按A→C→F→尾气处理顺序连接装置,不能证明亚硫酸和次氯酸的酸性强弱;②根据亚硫酸酸性大于碳酸、碳酸酸性大于次氯酸验证亚硫酸与次氯酸的酸性强弱;A中生成的SO2气体通过饱和NaHSO3溶液除去HCl,再通过饱和NaHCO3溶液生成二氧化碳气体,证明亚硫酸酸性大于碳酸,再通过高锰酸钾溶液除去CO2中的SO2,用品红溶液检验SO2已经除尽,再把CO2通入漂白粉溶液中,若D中品红不褪色、F中先有沉淀后溶解,证明碳酸酸性大于次氯酸;所以按照A→C→B→E→D→F→尾气处理(填字母) 顺序连接装置。③其中饱和NaHCO3溶液的作用是除去挥发HCl。(3)①设10.00mL残液中SO2的质量是xg,根据电子守恒 ,x=0.032g,残液中SO2的含量为
,x=0.032g,残液中SO2的含量为 3.2g·L-1;②若滴定前读数时平视,滴定终点读数时俯视,消耗KI溶液体积偏小,根据上式可知测定结果偏高。
3.2g·L-1;②若滴定前读数时平视,滴定终点读数时俯视,消耗KI溶液体积偏小,根据上式可知测定结果偏高。
【题型】实验题
【结束】
9
海洋资源丰富,海水水资源的利用和海水化学资源(主要为NaCl和MgSO4及K、Br等元素)的利用具有非常广阔的前景。

回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Mg2+和Ca2+,要加入的试剂分别为__________________、__________________。
(2)写出步骤Ⅰ中反应的总化学方程式为___________________________________。
(3)简述步骤Ⅱ中能析出KClO3晶体而无其他晶体析出的原因是_____________________________。
(4)已知MgCl2溶液受热时易水解生成Mg(OH)Cl,写出该过程的化学方程式__________________。
(5)为得到无水MgCl2,步骤Ⅲ的操作应为_____________________________。
(6)步骤Ⅳ中,电解熔融MgCl2得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_____。
A.N2 B.H2 C. CO2 D.空气
(7)海水中溴含量为65mg·L-1。若1L海水中95%溴元素被氧化为Br2经热空气吹出,溴单质残留量3%。最后用SO2将90%Br2还原成Br-,所得溶液体积为50mL。此过程的目的为________________。所得溶液中溴离子浓度为海水中溴离子浓度的_____________倍(精确到0.1)。
-
直接排放含SO2的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关SO2性质的探究活动。
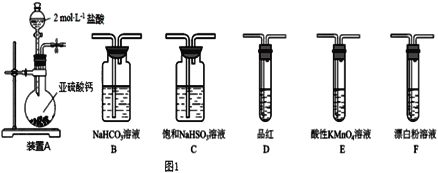
(1)装置A中反应的离子方程式为___________________________________。
(2)选用图1以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是__________________________。
②丙同学设计的合理实验方案为:按照A→C→________________________→尾气处理(填字母)顺序连接装置。其中装置C的作用是______________。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是___________________________________。
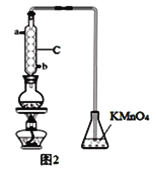
(3)利用图2的装置测量装置A中残液SO2的含量。量取10.00 mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL 0.1000 mol/L的KMnO4标准溶液吸收。充分反应后,再用0.2000 mol/L的KI溶液滴定过量的KMnO4,消耗KI溶液25.00 mL。(已知:10I -+2MnO4-+16H+==2Mn2++5I2+8H2O)
①图2锥形瓶中发生反应的离子方程式为______________________________。
②残液中SO2的含量为____________mol·L-1。
-
直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。

(1)装置 A 中仪器a的名称为 ____________。
(2)选用图6中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按 A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是_________________________。
②丙同学设计的合理实验方案为:按照 A→C→____ →E→_____ →F→尾气处理(填字母)顺序连接装置。 E装置的作用是________,证明亚硫酸的酸性强于次氯酸的实验现象是_______ 。
(3)为了测定装置A残液中SO2的含量,量取10.00mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00mL0.0500mol/L的酸性KMnO4溶液吸收。充分反应后,再用0.2 000mol/L的K I标准溶液滴定过量的 KMnO 4,消耗 KI溶液15.00mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
10I- +2MnO4-+16H+=2Mn 2+ +5I 2+8H2O
①残液中SO 2 的含量为_______ g·L-1。
②若滴定过程中不慎将 KI标准溶液滴出锥形瓶外少许,使测定结果______(填“偏高”、“偏低”或“无影响”)。
-
直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。

(1)装置A中仪器a的名称为__________。若利用装置A中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理________________。
(2)选用图4中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是_________________。
②丙同学设计的合理实验方案为:按照A→C→_________→F→尾气处理(填字母) 顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是_____________________。
③其中装置C的作用是__________。常温下,测得装置C中饱和NaHSO3溶液的pH≈5,则该溶液中所有离子的浓度由大到小的顺序为__________________。(已知0.1mol/L的H2SO3溶液pH >1)
(3)为了测定装置A残液中SO2的含量,量取10.00 mL残液于圆底烧瓶中,加热使SO2 全部蒸出,用20.00 mL0.0500 mol/L的KMnO4溶液吸收。充分反应后,再用0.2000mol/L的KI标准溶液滴定过量的KMnO4 ,消耗KI溶液15.00 mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为_______g·L-1。
②若滴定过程中不慎将KI标准溶液滴出锥形瓶外少许,使测定结果_______(填“偏高”、“偏低”或“无影响”)。
-
直接排放含SO2会形成酸雨,危害环境。某化学实验小组用如下装置进行有关SO2性质的探究活动。
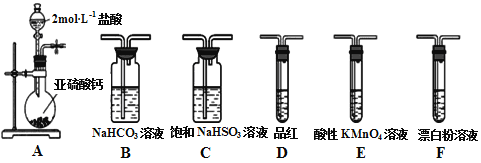
(1)装置A中反应的离子方程式为___________________________________。
(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是___________________。正确的连接顺序是:A→C→___________→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是__________________________。
(3)将二氧化硫通入以下装置可以制备Na2S2O3:

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ________________。
②写出装置A中发生反应的化学方程式___________________________________。
③Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(化学式量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=____mol·L-1。(已知:IO3-+5I-+6H+= 3I2+3H2O, 2S2O32-+I2=S4O62-+2I-)
-
直接排放含SO2会形成酸雨,危害环境。某化学实验小组用如下装置进行有关SO2性质的探究活动。

(1)装置A中反应的离子方程式为___________________________________。
(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是___________________。正确的连接顺序是:A→C→___________→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是__________________________。
(3)将二氧化硫通入以下装置可以制备Na2S2O3:

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ________________。
②写出装置A中发生反应的化学方程式___________________________________。
③Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(化学式量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=____mol·L-1。(已知:IO3-+5I-+6H+= 3I2+3H2O, 2S2O32-+I2=S4O62-+2I-)
-
直接排放含 的烟气会形成酸雨,危害环境.某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境.某化学实验小组进行如下有关 性质的探究活动.
性质的探究活动.
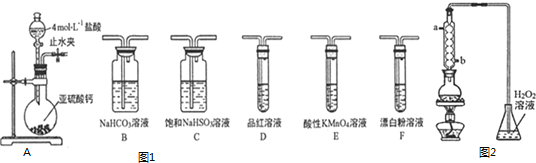
 写出利用如图1装置A中产生的气体证明
写出利用如图1装置A中产生的气体证明 价的硫元素具有氧化性的实验方案:______.
价的硫元素具有氧化性的实验方案:______.
 选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照 顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是______.
顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是______.
②丙同学设计的合理实验方案为: ______
______ ______
______ 尾气处理
尾气处理 填字母
填字母 其中装置C的作用昌______
其中装置C的作用昌______ 证明亚硫酸酸性强于次氯酸的实验现象是______.
证明亚硫酸酸性强于次氯酸的实验现象是______.
 利用如图2的装置可测定装置A残液中
利用如图2的装置可测定装置A残液中 的含量.量取
的含量.量取 残液于烧瓶中,加适量蒸馏水稀释,加热使
残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 标准溶液进行滴定,至终点时记录数据.重复滴定2次,平均消耗NaOH溶液的体积为
标准溶液进行滴定,至终点时记录数据.重复滴定2次,平均消耗NaOH溶液的体积为 .
.
①该装置中球形装冷凝管的冷凝水进口为______ 填“a”或“b”
填“a”或“b” .
.
②残液中 的含量为______
的含量为______ .
.
-
(10分)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示S形成硫酸酸雨的反应方程式 , 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________。
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣),n(HSO3﹣)变化关系如下表:
| n(SO3²﹣):,n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显 性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
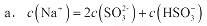
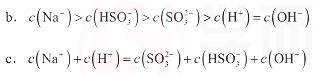
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
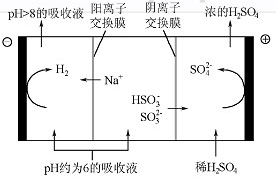
①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用。简述再生原理:
。
-
直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(1)用化学方程式表示S形成硫酸酸雨的反应方程式______,______.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是______.
(3)吸收液吸收SO2的过程中,pH随n(SO32-),n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显______性,用化学平衡原理解释:______.
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):______.
a、c(Na+)=2c(SO32-)+c(HSO3-)
b、c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
c、c(Na+)+c(H-)=c(SO32-)+c(HSO3-)+c(OH-)
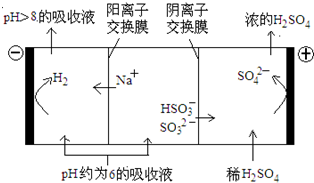
(4)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如图:
①HSO3-在阳极放电的电极反应式是______.
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理:______.



 ,x=0.032g,残液中SO2的含量为
,x=0.032g,残液中SO2的含量为