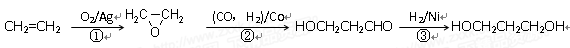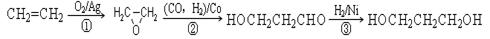-
工业上可利用“甲烷蒸气转化法生产氢气”,反应为:
CH4(g)+H2O(g)  CO(g)+3H2(g)
CO(g)+3H2(g)
已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷平衡含量(%)的影响如下图1:
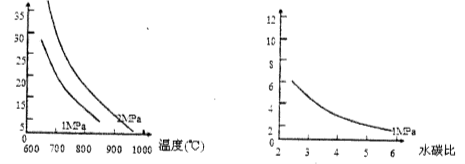
图1 (水碳比为3) 图2 (800℃)
(1)CH4(g)+H2O(g)  CO(g)+3H2(g)。的
CO(g)+3H2(g)。的 H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是 。
(3)其他条件不变,请在图2中画出压强为2MPa时,甲烷平衡含量(%)与水碳比之间关系曲线。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少?(写出计算过程,结果保留小数点后一位数字。)
-
以氢气、一氧化碳为主要成分,供化学合成的一种原料气体叫合成气。工业上通过“天然气蒸气转化”反应来得到合成气,其反应为:CH4+H2O(g) CO+3H2;△H>0。工业上通过采用合适的温度和压强、适宜的催化剂以及合适的CH4与H2O配比来获得最佳的生产效率。对于该转化反应的有关叙述正确的是( )
CO+3H2;△H>0。工业上通过采用合适的温度和压强、适宜的催化剂以及合适的CH4与H2O配比来获得最佳的生产效率。对于该转化反应的有关叙述正确的是( )
A.增大压强,有利于得到更多的合成气
B.反应温度越低,越有利于合成气的生产
C.工业生产中采用加入过量水蒸气来提高甲烷的利用率
D.工业生产中使用催化剂的目的在于提高甲烷的利用率
-
天然气(以甲烷计)在工业生产中用途广泛。
(1)Ⅰ.在制备合成氨原料气H2中的应用
(1)甲烷蒸气转化法制H2的主要转化反应如下:
CH4(g)+H2O(g) CO(g)+3H2(g)ΔH=+206.2kJ/mol
CO(g)+3H2(g)ΔH=+206.2kJ/mol
CH4(g)+2H2O(g) CO2(g)+4H2(g)ΔH=+165.0kJ/mol
CO2(g)+4H2(g)ΔH=+165.0kJ/mol
上述反应所得原料气中的CO能使合成氨催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是 。
(2)CO变换反应的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡变换率(已转化的一氧化碳量与变换前一氧化碳量之比)的关系如下图所示:
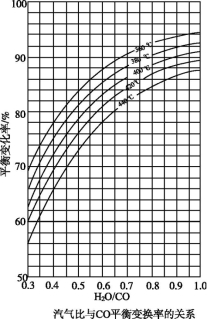
析图可知:
①相同温度时,CO平衡变换率与汽气比的关系是 。
②汽气比相同时,CO平衡变换率与温度的关系是 。
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),则CO变换反应的平衡常数表示式为Kp= 。随温 度的降低,该平衡常数 (填“增大”“减小”或“不变”)。
(2)Ⅱ.在熔融碳酸盐燃料电池中的应用以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池示意图如下:
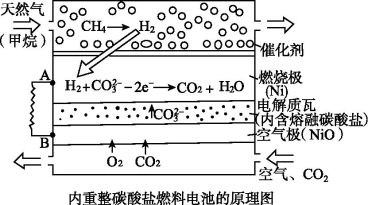
(1)外电路电子流动方向:由 流向 (填字母)。
(2)空气极发生反应的离子方程式是 。
(3)以此燃料电池为电源电解精炼铜,当电路有0.6 mol e-转移,有 g 精铜析出。
-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=-890.3kJ·mol-1
CO(g)+ O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H4=-41.0kJ•mol-1
则甲烷水蒸气重整反应的△H=__kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
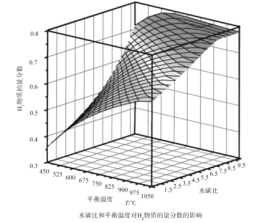
①H2的物质的量分数与水碳比(1~10)的关系是平衡温度一定时,__;其原因是__。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为__,其压强平衡常数为__;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率=__(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
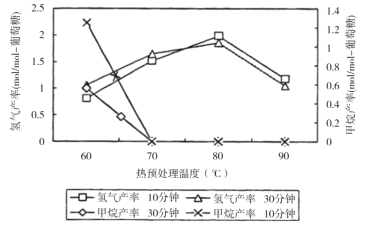
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为__;与甲烷水蒸气重整制氢相比其优点有__(至少写两点)。

-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=-890.3kJ·mol-1
CO(g)+ O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H4=-41.0kJ•mol-1
则甲烷水蒸气重整反应的△H=__kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
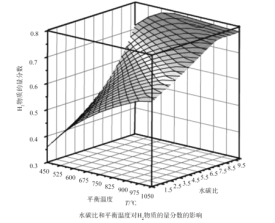
①H2的物质的量分数与水碳比(1~10)的关系是平衡温度一定时,__;其原因是__。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为__,其压强平衡常数为__;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率=__(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为__;与甲烷水蒸气重整制氢相比其优点有__(至少写两点)。
-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ·mol-1
CO(g)+0.5O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
H2(g)+0.5O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH4=-41.0kJ·mol-1
则甲烷水蒸气重整反应的ΔH=_____kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
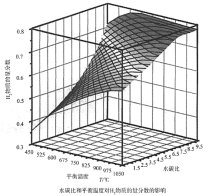
①温度一定时,H2的物质的量分数与水碳比(1~10)的关系是_____,产生该结论的原因是_____。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为_____,其压强平衡常数为_____;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率v=_____。
(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
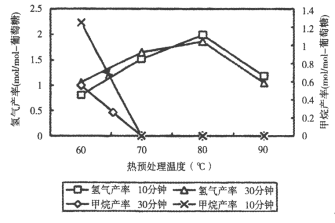
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为_____。
-
利用焦炭或天然气制取廉价的CO和H2,再用于有机合成是目前工业生产的重要途径.回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O═CO+3H2.部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热 |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1mol H2O (g)转变为1mol H2O(l)时放出44.0kJ热量.则CH4和水蒸气在高温下反应生成1mol H2的反应热为______.
(2)用CO和H2在一定条件下合成甲醇:CO+2H2⇌CH3OH.工业上采用稍高的压强(5MPa)和250℃,其可能原因是______.
| 反应温度/℃ | 平衡常数 | 反应温度/℃ | 平衡常数 |
| 667.30 | 200 | 1.909×10-2 |
| 100 | 12.92 | 300 | 2.42×10-4 |
(3)1,3-丙二醇是重要的化工原料,用乙烯合成1,3-丙二醇的路线如下:
CH2=CH2 HOCH2CH2CHO
HOCH2CH2CHO  HOCH2CH2CH2OH
HOCH2CH2CH2OH
某化工厂已购得乙烯11.2t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O  CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%.且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?______.
-
(12分)利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式________。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 mol H2,,此时N2的转化率为a。则平衡时NH3的浓度为________。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
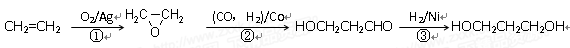
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭________吨、甲烷________吨,
才能满足生产需要。
-
 利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 molNH3,反应达平衡后测得平衡常数为K,此时CH4的转化率为a。则K和a的关系是K=。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
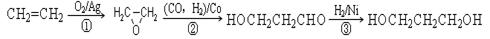
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
-
氢气是一种清洁、高效新能源,也是重要的化工原料。
(1)工业上利用甲烷制备氢气的反应为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
已知:
①H2(g)+1/2O2(g) H2O(g) △H1=-198kJ/mol
H2O(g) △H1=-198kJ/mol
②CO(g)+1/2O2(g) CO2(g) △H2=-283kJ/mol
CO2(g) △H2=-283kJ/mol
③CH4(g)+2O2(g) CO2(g)+2H2O(g) △H3=-846.3kJ/mol
CO2(g)+2H2O(g) △H3=-846.3kJ/mol
则CH4(g)+H2O(g) CO(g)+3H2(g) △H4=________。
CO(g)+3H2(g) △H4=________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g) CH3OH(g) △H=-116kJ/mo1
CH3OH(g) △H=-116kJ/mo1
①如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是_______,理由_________;Y1_____Y2(填“<”“=”或“>”)。
②在2L恒容密闭容器中充入2 mol CO和4 mol H2,在一定条件下经过10 min达到平衡状态c点处。则在该条件下,从开始至达到平衡状态v(CH3OH)=_______________,平衡常数Ka、Kb、Kc 的大小关系:___________。
③下列措施既能增大反应速率又能提高反应物的转化率的是_______。
A.使用催化剂 B.及时分离CH3OH C.升高温度 D.增大压强
(3)已知燃料电池的比能量与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为___________。
CO(g)+3H2(g)

CO(g)+3H2(g)。的
H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。






 CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题: