-
下列有关物质的性质或结构的说法正确的是 ( )
A.P是一种广泛应用于含磷化合物的结构分析和医疗诊断的核素,其原子核内含有15个中子
B.Na的原子半径比Cl的大,但Na+的半径比Cl-的小
C.Li、Na、K、Rb、Cs都属于碱金属元素,它们单质的还原性随原子序数的增大而减弱
D. Cl与I同属于ⅦA族元素,则两者最高价氧化物对应水化物的酸性:HClO4<HIO4
高三化学选择题中等难度题查看答案及解析
-
下列有关物质的性质或结构的说法正确的是( )
A.是一种广泛应用于含磷化合物的结构分析和医疗诊断的核素,其原子核内含有15个中子
B.Na的原子半径比Cl的大,但Na+的半径比Cl-的小
C.Li、Na、K、Rb、Cs都属于碱金属元素,它们单质的还原性随原子序数的增大而减弱
D.Cl与I同属于ⅦA族元素,则两者最高价氧化物对应水化物的酸性:HClO4<HIO4高三化学选择题中等难度题查看答案及解析
-
下列有关物质的性质或结构的说法正确的是
A.
是一种广泛应用于含磷化合物的结构分析和医疗诊断的核素,其原子核内含有15个中子
B.Na的原子半径比Cl的大,但Na+的半径比Cl-的小
C.Li、Na、K、Rb、Cs都属于碱金属元素,它们单质的还原性随原子序数的增大而减弱
D.Cl与I同属于ⅦA族元素,则两者最高价氧化物对应水化物的酸性:HClO4<HIO4
高三化学选择题简单题查看答案及解析
-
(12分)[物质结构与性质]
钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗以及石油化工等邻域。下面是用金红石(主要成分为TiO2)制备金属钛和钛酸钡的流程。
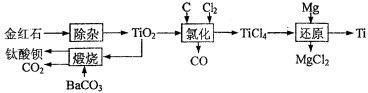
(1)Ti基态的电子排布式为 。
(2)TiCl4熔点为-24℃,沸点为136.4℃,室温下为无色液体,可溶于甲苯和氯代烃。
固态TiCl4属于 晶体。
(3)BaCO3为离子化合物。CO32-中C原子的杂化类型为 ,写出一种与CO32-互为等电子体的阴离子:
(填化学式)。
(4)钛酸钡的晶胞如图所示,其化学式为 。
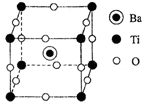
(5)用锌还原TiCl4的盐酸溶液,经后续处理可制得绿色的配合物[TiCl(H2O)5]Cl2•H2O。1mol该配合物中含有σ键的数目为 。
高三化学填空题困难题查看答案及解析
-
化学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的自然科学。下列不属于化学研究发展方向或说法不正确的是 ( )
A.高铁酸钾广泛用于废水的净化处理,因为它具有强还原性
B.最近合成117号元素的反应为:
,该变化不属于化学变化
C.“原子经济”和“零排放”是绿色化学和化工的发展目标
D.最近在星际介质中发现的分子薏(
),该分子中所有原子可以处于同一平面
高三化学选择题简单题查看答案及解析
-
【化学一选修3:物质结构与性质】铁、钻、镍等金属及其化合物在科学研究和工业生产中应用十分广泛。回答下列问题:
(1)基态钴原子的价电子排布式为________,铁、钴、镍的基态原子核外未成对电子数最少的是_____________
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,酞钴分子中与钴离子通过配位键结合的氮原子的编号是__________ (填1、2、3、4),三种非金属原子的电负性由大到小的顺序为____(用相应的元素符号表示);碳原子的杂化轨道类型为_________

(3)Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO) x晶体属于_______ (填晶体类型),若配合物Fe(CO) x的中心原子价电子数与配体提供电子数之和为18,则x=_________
(4)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO ______ FeO(填“>”“<”或“=”),原因是___________________________。
(5)NiAs的晶胞结构如图所示:
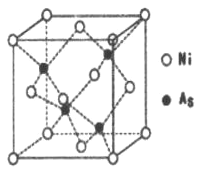
①镍离子的配位数为_________。
②若阿伏加德罗常数的值为NA,晶体密度为pg.cm-1,则该晶胞中最近的离子之间的距离为_____cm。(写出计算表达式)
高三化学综合题中等难度题查看答案及解析
-
物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_________,Li原子核外占据最高能层电子的电子云轮廓图形状为_________。
(2)As 的卤化物的熔点如下:
AsCl3
AsBr3
AsI3
熔点/K
256.8
304
413
表中卤化物熔点差异的原因是_________,AsCl3分子的立体构型为_________。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶休的密度是_________g/cm3(用含a、NA的式子表示)。
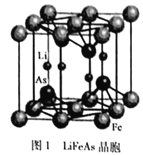
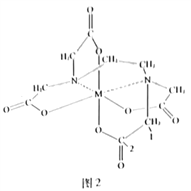
(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______个σ键,2号碳原子采取_________杂化方式;Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_________。
高三化学综合题中等难度题查看答案及解析
-
【化学——选修3:物质结构与性质】钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。
请回答下列问题:
(1)Co基态原子的电子排布式为 ;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
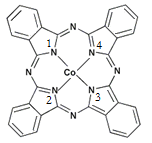
①酞菁钴中三种非金属原子的电负性由大到小的顺序为 ;(用相应的元素符号作答);碳原子的杂化轨道类型为 ;
②与钴离子通过配位键结合的氮原子的编号是 ;
(3)CoCl2中结晶水数目不同呈现不同的颜色。
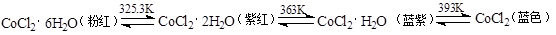
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用: ;
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,写出该反应的离子方程式: ;
(5)Co的一种氧化物的晶胞如右图所示,在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成是 。
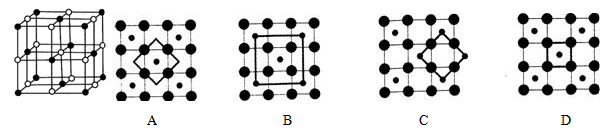
高三化学填空题困难题查看答案及解析
-
【化学一选修3:物质结构与性质】铜及其化合物在化工生产中有着广泛的应用。回答下列问题:
(1)铜元素在元素周期表中的位置为_________________,基态Cu原子核外电子占据的原子轨道数为____________________。
(2)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH3)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。
①乙二胺分子中C、N原子的杂化轨道类型分别为_______________、_________________。
②与硫酸根离子互为等电子体的分子为___________(任写一种)。
③四配位离子的结构式为_____________________,该离子中所有元素的电负性由大到小的顺序为____________________________。
(3)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为___________(填化学式),原因为________________________________________________。
(4)下图为铜与氧(O)、钇(Y)、钡(Ba)形成的一种超导体材料的长方体晶胞结构,其晶胞参数如图(i)所示,该结构中有平面正方形(CuO4)和四方锥(CuO6)结构单元如图(ii)所示。
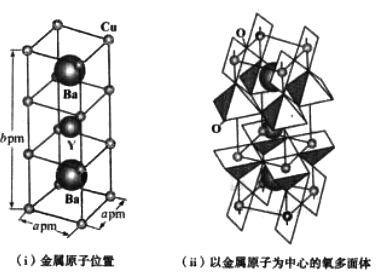
①该超导体材料的化学式为____________________________。
②已知该化合物的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,其密度为____g·cm-3(列出表达式即可)。
高三化学综合题中等难度题查看答案及解析
-
【化学-选修3:物质结构与性质】
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是______________,基态铜原子的核外电子排布式为________________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____________(填晶体类型)。
(3)CO和CO的一种生活中常见等电子体分子,两者相比较沸点较高的为__________(填化学式)。CN-中碳原子杂化轨道类型为_______________,C、N、O三元素的第一电离能最大的为_______________(用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示。每个铜原子周围距离最近的铜原子数目__________。
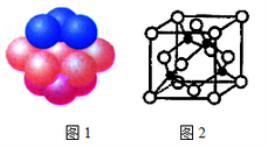
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为_____________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________________(填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的1/4,则该晶体中铜原子和M原子之间的最短距离为_______________pm(只写计算式)。
高三化学填空题极难题查看答案及解析