-
2SO2(g)+O2(g)⇌2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)被氧化为1mol SO3(g)的ΔH= -99kJ·mol-1。回答下列问题:
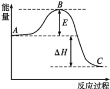
(1)图中A、C分别表示:________、________。
(2)图中ΔH=___kJ·mol-1。
(3)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH 并写出其热化学反应方程式:________。
-
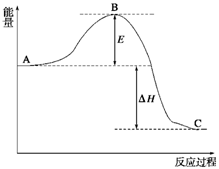
(12分) 2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
请回答下列问题:
(1) E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________;(2)图中ΔH=________kJ/mol;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式________;
;
(4)如果反应速率v(SO2)为0.05 mol/(L·min),则
 v(O2)=________mol/(L·min)、v(SO3)=________mol/(L·min);
v(O2)=________mol/(L·min)、v(SO3)=________mol/(L·min);
(5)已知S (s)+O2(g) SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH________。
SO2(g) ΔH=-296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH________。
-
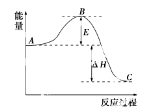
2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
请回答下列问题:
(1)图中A、C分别表示________、________;
(2)图中ΔH=________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式: ; 。
(4)在一定条件下,向体积为2L的容器中加入2mol O2和3mol SO2进行可逆反应: 2SO2(g)+O2(g) 2SO3(g),2min后测得O2的物质的量为1.6mol,则:若用O2的浓度变化来表示该反应的反应速率,则V(O2)= ;若用SO3的浓度变化来表示该反应的反应速率,则V(SO3)= .
2SO3(g),2min后测得O2的物质的量为1.6mol,则:若用O2的浓度变化来表示该反应的反应速率,则V(O2)= ;若用SO3的浓度变化来表示该反应的反应速率,则V(SO3)= .
(5)已知单质硫的燃烧热为296 kJ·mol-1,写出由S(s)生成3 mol SO3(g)的热化学方程式(要求写出简单计算过程)。(已知燃烧热是指25 ℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量)
-
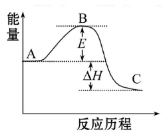
(10分)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示_________、_________,E的大小对该反应的反应热有无影响?_________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是__________________;
(2)图中ΔH=_________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒氧化物VO2;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式_____________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______(要求计算过程)。
-
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
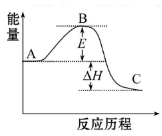
(1)图中A、C分别表示_________、_________,E的大小对该反应的反应热有无影响?_________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是__________________;
(2)图中ΔH=_________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒氧化物VO2;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式_____________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______(要求计算过程)。
-
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
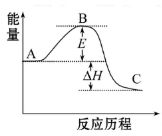
(1)图中A、C分别表示_________、_________,E的大小对该反应 的反应热有无影响?_________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是__________________;(2)图中ΔH=_________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒氧化物VO2;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式_____________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH_______(要求计算过程)。
-
2SO2(g)+O2(g)
 2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
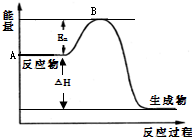
(1)图中A点表示________,a=________.
(2)Ea的大小对该反应的△H________(填“有”或“无”)影响.该反应常用V2O5作催化剂,加入V2O5会使图中B点________(填“升高”、“降低”或“不变”).
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:________,常温常压下,由单质硫和氧气经两步反应,生成3mol SO3(g),放出的总热量为_________.
-
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
请回答下列问题:
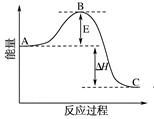
图中A、C分别表示________________、________________,
E的大小对该反应的反应热有无影响?______________。
(2)图中ΔH=____________ kJ·mol-1;
(3) 反应速率v(SO2)为0.05 mol · L-1 · min-1,则v(O2)=____________mol · L-1 · min-1、
v(SO3)=____________mol · L-1 · min-1;
(4) 已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH=________。
-
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:

(1)图中A点表示:___________, B点表示:__________,E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
-
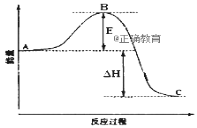
已知2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H = -99kJ/mol。请回答下列问题:
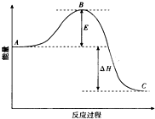
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。
(2)图中△H = kJ/mol。
(3)该反应通常用V2O5作催化剂,V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式为
、 。
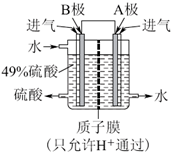
(4)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图所示,电极A、B为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
①该原电池的B为 (填“正极”、“负极”),其电极反应式为 。
②电解质溶液中H+通过质子膜 (填“向左”“向右”、“不”)移动。
③电池总反应式为 。
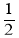 O2(g)=CO2(g) ∆H=–283.0 kJ/mol
O2(g)=CO2(g) ∆H=–283.0 kJ/mol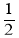 O2(g)=H2O(l) ∆H=–285.8 kJ/mol
O2(g)=H2O(l) ∆H=–285.8 kJ/mol









