-
已知2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H = -99kJ/mol。请回答下列问题:
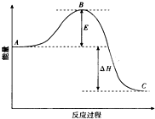
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。
(2)图中△H = kJ/mol。
(3)该反应通常用V2O5作催化剂,V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式为
、 。
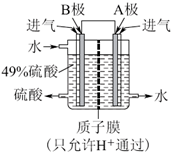
(4)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图所示,电极A、B为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
①该原电池的B为 (填“正极”、“负极”),其电极反应式为 。
②电解质溶液中H+通过质子膜 (填“向左”“向右”、“不”)移动。
③电池总反应式为 。
-
(13分) 2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的 ΔH=—99kJ·mol-1.请回答下列问题:

(1)图中A、C分别表示________、________
(2) E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________
 (3)图中△H=________KJ·mol-1;
(3)图中△H=________KJ·mol-1;
(4)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
________ 、 ________
 (5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H________(要求写出计算过程)。
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H________(要求写出计算过程)。
-
(11分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2( g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:

(1)图中A、C分别表示________、
________,E的大小对该反应的反应热________(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点________(填“升高”还是“降低”),△H________(填“变大”、“变小”或“不变”)。
(2)图中△H=________KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写出该催化循环机理的化学方程式________、________。
-
(6分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(1)图中A、C分别表示________、________,
(2)图中△H=________KJ·mol-1;
(3)已知单质硫的燃烧热为296 KJ·mol-1,
计算由S(s)生成3 molSO3(g)的△H________(要求计算过程)。
-
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.请回答下列问题:
(1)图中A、C分别表示______、______,
(2)图中△H=______KJ•mol-1;
(3)已知单质硫的燃烧热为296KJ•mol-1,计算由S(s)生成3molSO3(g)的△H______(要求计算过程).

-
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol-1.请回答下列问题:

(1)图中A、C分别表示________、________;
(2)图中△H=________KJ·mol-1;
 (3)已知单质硫的燃烧热为296 KJ·mol-1,写出表示硫燃烧的热化学方程式;
(3)已知单质硫的燃烧热为296 KJ·mol-1,写出表示硫燃烧的热化学方程式;
(4)计算由S(s)生成3 molSO3(g)的△H = ________。
-
2SO2(g)+O2(g)⇌2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)被氧化为1mol SO3(g)的ΔH= -99kJ·mol-1。回答下列问题:
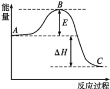
(1)图中A、C分别表示:________、________。
(2)图中ΔH=___kJ·mol-1。
(3)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH 并写出其热化学反应方程式:________。
-
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
(1)图中E的大小对该反应的反应热________(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___________ (填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式______________________________________。
-
(最后一空2分,其余每空1分,共8分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:

 (1)图中A、C分别表示、,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由
(1)图中A、C分别表示、,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由
是;
(2)图中△H=________KJ·mol-1;
 (3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求
计算过程)。
-
2SO2(g)+O2(g)==2SO3(g)反应过程中的能量变化如下图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示__________的能量、___________的能量;
(2)图中ΔH=______________________;
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=___________;
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为____________________。










