-
已知A、B、D是食品中的常见有机物,A是生物的主要供能物质。以A和水煤气(CO、H2)为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知E是CO和H2以物质的量之比1:2反应的产物,F为具有特殊香味、不易溶于水的油状液体。
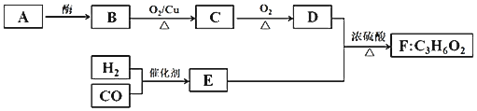
请回答:
(1)有机物D中含有的官能团名称是______。
(2)B→C化学方程式是______。
(3)下列说法不正确的是______(填字母)。
A.有机物B与金属钠反应比水与金属钠反应要剧烈
B.除去F中含有D、E杂质可用NaOH溶液洗涤、分液
C.D和E反应生成F时,浓硫酸主要起强氧化剂作用
D.C在一定条件下可以与H2反应转化为B
-
已知 A、B、D 是食品中的常见有机物,A 是生命体的主要供能物质。以 A 和水煤气(CO、H2)为原料在一定条件下可获得有机物 B、C、D、E、F,其相互转 化关系如图。已知 E 是 CO 和 H2 以物质的量之比 1:2 反应的产物,F 为具有特殊香味、 不易溶于水的油状液体。
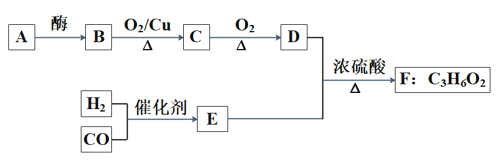
请回答:
(1)有机物 D 中含有的官能团名称是____________________。
(2)B→C 化学方程式是______________________________。
(3)D 和 E 生成 F 的反应方程式为_____________________,反应类型为_____________________。
(4)下列说法正确的是_________________________(填字母)。
A.有机物 A 可由淀粉或纤维素水解得到
B.除去 F 中含有的 D、E 杂质可用 NaOH 溶液洗涤、分液
C.D 和 E 反应生成 F 时,浓硫酸主要起强氧化剂作用
D.75%的 B 溶液可以用作消毒剂,有效灭活新冠病毒
-
已知 A、B、D 是食品中的常见有机物,A 是生命体的主要供能物质。以 A 和水煤气(CO、H2)为原料在一定条件下可获得有机物 B、C、D、E、F,其相互转 化关系如图。已知 E 是 CO 和 H2 以物质的量之比 1:2 反应的产物,F 为具有特殊香味、 不易溶于水的油状液体。
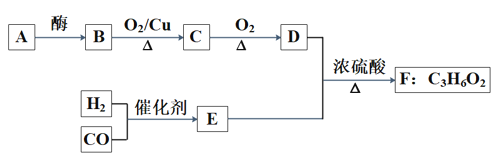
请回答:
(1)有机物 D 中含有的官能团名称是____________________。
(2)B→C 化学方程式是______________________________。
(3)D 和 E 生成 F 的反应方程式为_____________________,反应类型为_____________________。
(4)下列说法正确的是_________________________(填字母)。
A.有机物 A 可由淀粉或纤维素水解得到
B.除去 F 中含有的 D、E 杂质可用 NaOH 溶液洗涤、分液
C.D 和 E 反应生成 F 时,浓硫酸主要起强氧化剂作用
D.75%的 B 溶液可以用作消毒剂,有效灭活新冠病毒
-
煤的气化和液化可实现煤的综合利用,提高煤的利用价值。煤的间接液化是指以煤为原料,先气化(主要以水作气化剂)制成合成气,然后再通过一系列作用将合成气转化成烃类燃料、醇类燃料和化学品的过程。
Ⅰ.煤的气化
煤与水蒸气发生反应生成水煤气的反应为:C(s)+H2O(g)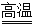 CO(g)+H2(g)。
CO(g)+H2(g)。
(1)一定温度下,在一个恒容的密闭容器中,加入足量的炭粉(体积忽略不计)与10 mol的水蒸气发生上述反应,下列叙述能说明该反应一定达到化学平衡状态的是______(填字母序号)。
A.v(H2O)=v(H2)时
B.容器内气体的密度不再随时间改变而变化
C.形成1 mol H-O键的同时,形成1 mol H-H键
D.容器内气体的平均摩尔质量不再随时间改变而变化
Ⅱ.合成气的液化
将产生的CO与H2的混合气体,通过反应CO(g)+H2(g)→X(未配平,该反应为放热反应)合成X,是煤的液化的常用方法。
(2)图中能够正确表示上述反应的能量变化的图像是______(填“A”或“B”)。
(3)将等物质的量的CO和H2分别充入一个2 L的密闭容器内,在一定条件下发生上述反应,反应过程中各物质的转化关如图。
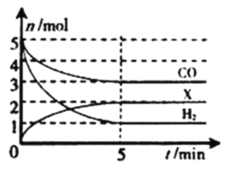
①该反应的方程式为______(注:X要用具体的分子式或结构简式表示)。
②该反应前5 min内用H2表示的平均反应速率v(H2)=______mol/(L·min)。
-
下列说法中正确的是
A.烃是指含有碳、氢元素的有机物
B.燃烧后能产生CO2和H2O的有机物一定是烃
C.天然气、沼气、坑气、煤气的主要成分都是甲烷
D.形成化合物种类最多的元素位于周期表中第二周期第IVA族
-
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)一定条件下,H2 、CO在体积固定的绝热密闭容器中发生如下反应:4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g),下列选项能判断该反应达到平衡状态的依据的有________。
CH3OCH3(g)+H2O(g),下列选项能判断该反应达到平衡状态的依据的有________。
A.v(H2)=2v(CO)
B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量不随时间而变化
(2)工业可采用CO与H2反应合成再生能源甲醇,反应:CO(g)+2H2(g)  CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T )、压强(p)的关系如下图1所示。
CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T )、压强(p)的关系如下图1所示。

①合成甲醇的反应为________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为________,p1和p2的大小关系为______。
③若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为_______ L。
④ CO的平衡转化率(α)与温度(T )、压强(p)的关系如上图2所示,实际生产时条件控制在250 ℃ 、1.3×104 kPa左右,选择此压强的理由是_________________。
-
物质W、X、Y、Z的转化关系如图所示,其中X、W是单质,Y、Z是化合物.
(1)若X、W是常见的非金属单质,该反应在工业上可用来生产水煤气.
①该反应的化学方程式是______ CO+H2

-
煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关重要。请回答下列问题:
(1)煤的气化。原理是C(s)+2H2(g) CH4(g) ΔH。
CH4(g) ΔH。
在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
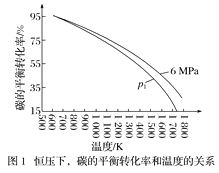
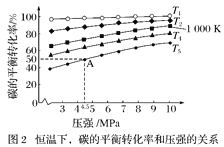
①有关图1、图2的说法正确的有___(填字母)。
a.p1<6MPa b.T1<1000K
c.ΔH<0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=__(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO+H2)与N2的体积之比为3.1~3.2,发生的反应有C(s)+H2O(g) CO(g)+H2(g),C(s)+
CO(g)+H2(g),C(s)+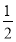 O2(g)
O2(g) CO(g)。从能量角度考虑,通入空气的目的是___。
CO(g)。从能量角度考虑,通入空气的目的是___。
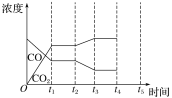
②如图是反应CO(g)+H2O(g) H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
-
CH4、CH3OH既是重要的化工原料,又是未来重要的能源物质。
(1)将1.0 mol CH4和2.0 mol H2O(g) 通入容积为2L的反应室,在一定条件下发生反应CH4(g)+H2O(g)  CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
(2)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g)  CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
a.恒容条件下充入He b.增大体积
c.升高温度 d.投入更多的H2O(g)
(3)在恒容条件下进行反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________ (填选项序号)。
CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________ (填选项序号)。
a.消耗1 mol CO2同时生成1 mol CH3OH b.容器内压强保持不变
c.混合气体的密度保持不变 d.CH3OH(g)的浓度保持不变
(4)以KOH为电解质的甲醇-空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图。 回答下列问题:
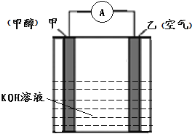
①该原电池的正极是____(填“甲”或“乙”),电解过程中乙电极附近pH____(填“增大”或“减小”);
②负极的电极反应式________________________________。
-
制取水煤气的反应为C(s)+H2O(g)  CO(g)+H2(g) ΔH>0;在一定条件下达到化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是( )
CO(g)+H2(g) ΔH>0;在一定条件下达到化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是( )
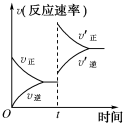
A.加压 B.升温 C.增大水蒸气浓度 D.增大碳的物质的量



 CO(g)+H2(g)。
CO(g)+H2(g)。


 CH4(g) ΔH。
CH4(g) ΔH。

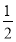 O2(g)
O2(g)

