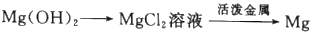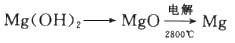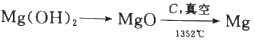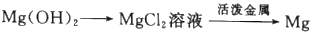-
海洋是巨大的资源宝库。大连市充分利用沿海优势,优先发展海水淡化生 产与综合利用一体化绿色循环经济产业,逐步建立起较为完善的海水淡化产业链,全 面推动海水淡化相关技术研发、装备制造、原材料生产和盐化工等产业集聚发展。
Ⅰ.从海水中提取食盐和溴的过程如下:
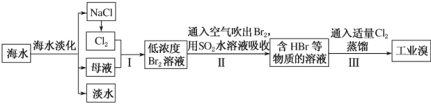
(1)海水淡化的方法主要有蒸馏法、_________________等(写出一种即可)。
(2)步骤Ⅰ中已获得 Br2,步骤Ⅱ中又将 Br2 还原为 Br-,其目的为_____________。
(3)步骤Ⅱ用 SO2 水溶液吸收 Br2,吸收率可达 95%,有关反应的离子方程式为_____;由此反应可知,除环境保护外,在该工业生产中应解决的主要问题是________。
(4)步骤Ⅲ蒸馏过程中,温度应控制在 80~90 ℃。温度过高或过低都不利于生产, 若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则_____________________________。
Ⅱ.某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下 实验装置(夹持装置略去)和操作流程。已知:Br2 的沸点为 59 ℃,微溶于水,有毒。
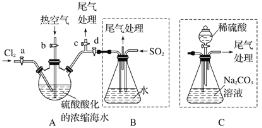
①连接 A 与 B,关闭活塞 b、d,打开活塞 a、c,向 A 中缓慢通入 Cl2 至反应完全;
②关闭活塞 a、c,打开活塞 b、d,向 A 中鼓入足量热空气;
③进行步骤②的同时,向 B 中通入足量 SO2;
④关闭活塞 b,打开活塞 a,再通过 A 向 B 中缓慢通入足量 Cl2;
⑤将 B 中所得液体进行萃取、分液,蒸馏并收集液溴。 请回答下列问题:
(1)步骤②中鼓入热空气的作用是_______________________________。
(2)进行步骤③时,B 中尾气可用___________________(填字母)吸收处理。
a.水 b.浓硫酸 c.NaOH 溶液 d.饱和 NaCl 溶液
(3)若直接连接 A 与 C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸, 再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C 中反应生成了 NaBrO3、NaBr、CO2,则该反应的化学方程式为____________________。
(4)与 B 装置相比,采用 C 装置的优点为___________________________。
-
海洋是巨大的资源宝库。大连市充分利用沿海优势,优先发展海水淡化生 产与综合利用一体化绿色循环经济产业,逐步建立起较为完善的海水淡化产业链,全 面推动海水淡化相关技术研发、装备制造、原材料生产和盐化工等产业集聚发展。
Ⅰ.从海水中提取食盐和溴的过程如下:
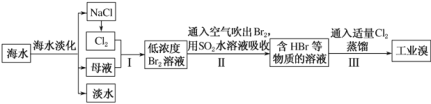
(1)海水淡化的方法主要有蒸馏法、_________________等(写出一种即可)。
(2)步骤Ⅰ中已获得 Br2,步骤Ⅱ中又将 Br2 还原为 Br-,其目的为_____________。
(3)步骤Ⅱ用 SO2 水溶液吸收 Br2,吸收率可达 95%,有关反应的离子方程式为_____;由此反应可知,除环境保护外,在该工业生产中应解决的主要问题是________。
(4)步骤Ⅲ蒸馏过程中,温度应控制在 80~90 ℃。温度过高或过低都不利于生产, 若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则_____________________________。
Ⅱ.某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下 实验装置(夹持装置略去)和操作流程。已知:Br2 的沸点为 59 ℃,微溶于水,有毒。
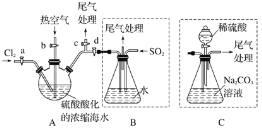
①连接 A 与 B,关闭活塞 b、d,打开活塞 a、c,向 A 中缓慢通入 Cl2 至反应完全;
②关闭活塞 a、c,打开活塞 b、d,向 A 中鼓入足量热空气;
③进行步骤②的同时,向 B 中通入足量 SO2;
④关闭活塞 b,打开活塞 a,再通过 A 向 B 中缓慢通入足量 Cl2;
⑤将 B 中所得液体进行萃取、分液,蒸馏并收集液溴。 请回答下列问题:
(1)步骤②中鼓入热空气的作用是_______________________________。
(2)进行步骤③时,B 中尾气可用___________________(填字母)吸收处理。
a.水 b.浓硫酸 c.NaOH 溶液 d.饱和 NaCl 溶液
(3)若直接连接 A 与 C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸, 再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C 中反应生成了 NaBrO3、NaBr、CO2,则该反应的化学方程式为____________________。
(4)与 B 装置相比,采用 C 装置的优点为___________________________。
-
地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面根据海水资源综合利用,请回答下列问题:
(1)淡化海水的方法有________________(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________(填化学式),之后________(填操作名称),再加入适量________(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)由无水MgCl2制取金属镁的常用工业方法是__________________。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是__________。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式____________。再H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________。
-
海洋是一座巨大的化学资源宝库,从中可以提取多种化学物质。从淡化海水中提取溴是海水综合利用的重要途径,其流程如图:

完成下列填空
(1)写出一种工业上海水淡化的方法_____。
(2)过程Ⅱ中物质X可以选SO2吸收溴,写出该反应的化学方程式_____。
(3)过程I、Ⅱ要达到的目的是_____。
(4)写出过程Ⅲ反应的离子方程式_____。
-
地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面是海水资源综合利用的部分流程图,请根据该图回答下列问题:
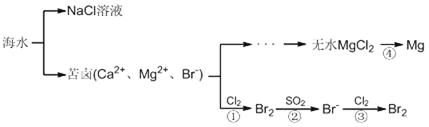
(1)淡化海水的方法有__________________(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________(填化学式),之后________(填操作名称),再加入适量________(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)反应④由无水MgCl2制取金属镁的常用工业方法是__________________。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是_________________________。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式__________________________________。最后再用H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________________________。
-
海洋约占地球表面积的71%,是一个远未完全开发的巨大化学资源宝库,海水水资源的利用和海水化学资源的利用具有非常广阔的前景.回答下列问题:
(1)海水淡化处理多用蒸馏法.如图是海水蒸馏原理示意图.蒸馏法的特点是设备结构、操作简单,淡水质量好,但也具有明显的缺陷.
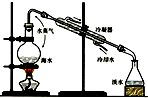
1你认为蒸馏法进行海水淡化的主要缺陷是________;
②我省某沿海地区拟采用蒸馏法兴建一座大型海水淡化工厂,为克服蒸馏法海水淡化的缺陷,请你为该地区提出一条合理化建议________;
(2)海水淡化后得到的淡水应进行技术处理后才能得到完全满足生产、生活要求的水,使用离子交换树脂与水中的离子进行交换是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,已知丙烯酸钠的化学式为CH2=CH-COONa试写出生成聚丙烯酸钠的化学方程:________;
(3)从海水中可以获取食盐、镁、钾、溴及其化工产品.空气吹出法是目前从海水中提取溴的常用方法,具体流程如下:
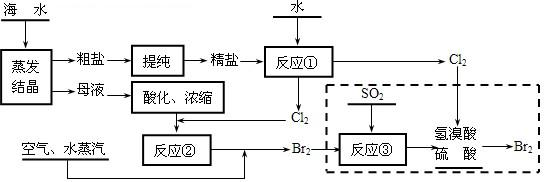
①实验室中粗盐提纯的步骤是________;在反应②中得到的溶液中通入空气、水蒸汽的作用是________;
②反应的离子方程式分别为________;
③在反应中消耗标况下896m3SO2时,共转移________ mol电子;
(4)上述流程中虚线方框内生产流程的作用是________.
-
(本题12分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列;从海水中提取食盐和溴的过程如下

(1)请列举海水淡化的两种方法: ________ 、 ________ 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 ________
________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除保护环境外,在工业生产中应解决的主要问题是 ________ 。
(4)某化学研究性学习小组为了解从工业生产中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
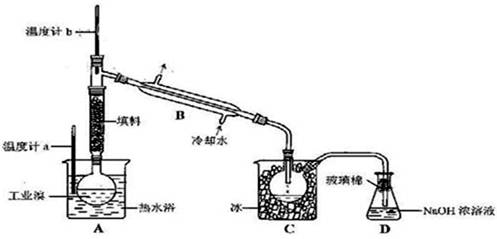
请你参与分析讨论:
① 图中仪器B的名称: 。
② 整套实验装置中仪器连接均不能使用橡胶塞和橡胶管,其原因是 。
③ 实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: ________ 。
④ C中液体颜色为 。为除去产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 ________ 。
-
海洋是非常巨大的资源宝库,以下有关海洋资源开发和利用的说法,不正确的是( )
A.海水中的元素种类很多,富集程度大
B.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
C.海水中除H2O外,还含有Cl、Na、K、Mg、Ca、S、F等多种元素
D.由于与岩石、大气和生物相互作用,海水中溶解和悬浮着大量无机物和有机物
-
海洋是生命的摇篮、资源的宝库。中国要实施海洋强国战略,实现由海洋大国向海洋强国迈进的梦想。海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。其流程如下图所示:
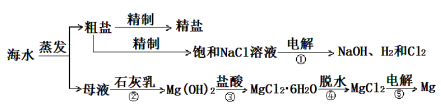
(1)写出①、②反应的离子方程式:
①______________________,②______________________。
(2)工业上利用电解饱和食盐水产生的氢气和氯气制取盐酸,为了体现绿色化学理念,使氯气充分反应,采取将氯气在氢气中燃烧的办法,可避免氯气燃烧不完全污染空气,请写出氯气在氢气中燃烧的实验现象:______________________。
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得到饱和NaC1溶液。现有下列除杂试剂:A.盐酸 B.氢氧化钡溶液 C.碳酸钠溶液。精制时加入过量除杂试剂的正确顺序是______________。(填序号)
(4)金属镁在空气中燃烧时,除生成MgO外,还有少量Mg3N2生成。把等物质的量的金属镁分别放在:A.纯氧气(O2)中;B.二氧化碳气体中;C.空气中。完全燃烧后,得到的固体物质的质量由大到小的顺序是______________。(填序号)
(5)将电解饱和NaCl溶液生成的氯气通入氢氧化钠溶液中可以得到NaClO。某化学兴趣小组探究NaClO与尿素CO(NH2)2的反应产物,通过实验发现产物除某种盐外,其余产物都是能参与大气循环的物质,则该反应的化学方程式为____________。
-
海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
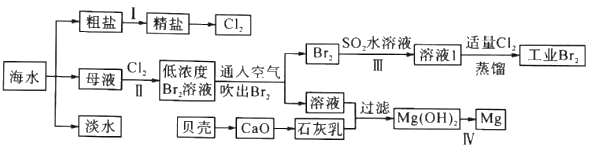
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________、_________。
(2)步骤Ⅱ中已获得Br2,步骤Ⅲ中又将Br2还原为Br-,其目的是_________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A. 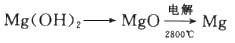
B.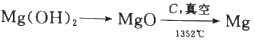
C.
D.