-
Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、K2Cr2O7等试剂测定某工厂废水中Ba2+ 的物质的量浓度。
(1)在容量瓶的使用方法中,下列操作不正确的是___(填字母序号)。
a.使用容量瓶前先检查是否漏水
b.使用容量瓶前必须用蒸馏水将其洗净并干燥
c.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管逐滴滴加蒸馏水至刻度线
d.盖好瓶塞,用食指顶住瓶塞,另一手拖住瓶底,将容量瓶反复倒转摇匀
(2)现需配制250mL0.1000mol∙L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、玻璃棒、烧杯外,还需要__________。
(3)需准确称取Na2S2O3固体的质量为__________g。
(4)若配制标准Na2S2O3溶液时,出现如下错误操作,所配溶液的浓度将如何变化?
①若将洗涤液转移至容量瓶时,不小心洒落部分洗涤液,会导致所配溶液的浓度_____(填“偏高”、“偏低”或“无影响”,下同)。
②若观察液面时俯视容量瓶刻度线,会导致所配溶液的浓度_______。
(5)另取50.00mL废水,控制适当的酸度,加入足量的K2Cr2O7溶液,得到BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-,再向其中滴加上述标准Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关反应的离子方程式为Cr2O72-+6S2O32-+14H+ = 2Cr3++3S4O62-+7H2O。则该工厂废水中Ba2+的物质的量浓度为_________。
高二化学实验题中等难度题查看答案及解析
-
Ba2+是一种重金属离子,某环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。
(1)现需配制250mL0.100mol·L-1标准Na2S2O3溶液,所需要的玻璃仪器除250mL容量瓶、玻璃棒外、烧杯,还需要 。
(2)需准确称取Na2S2O3固体的质量为 g(精确到0.01,)。
(3)取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加上述Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为:①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;②I2+2S2O32-=2I-+S4O62-。试计算该工厂废水中Ba2+的物质的量浓度 (写出计算过程) 。
高二化学计算题困难题查看答案及解析
-
某工厂的工业废水中含有Fe3+、Cu2+、SO42-等离子,为了减少污染并变废为宝,工厂计划从该废水中回收金属铜并得到硫酸亚铁.生产流程如下图所示(所加试剂均为过量):
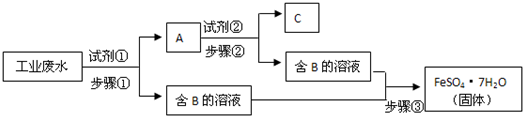
请回答:
(1)试剂①应该是______,A中含有的物质是______.步骤①中发生反应的离子方程式为______.
(2)步骤①、②、③中共同的分离提纯方法是______,步骤③中还需要的分离提纯方法是______.
(3)某同学为了验证长期放置的FeSO4•7H2O固体是否变质,取少量该固体于试管中,加入少量蒸馏水,再滴入几滴______溶液,若观察到______,则证明该固体已经变质.高二化学解答题中等难度题查看答案及解析
-
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol−1)可用作定影剂、还原剂。回答下列问题:
(1)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至_________中,加蒸馏水至____________。
②滴定:取0.00950 mol/L的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应: Cr2O72−+6I−+14H+==3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32−==S4O62−+2I−。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
(2)①该实验中应该用_______式滴定管装K2Cr2O7标准溶液
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为____________________________________________。
高二化学填空题中等难度题查看答案及解析
-
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g·mol-1)可用作定影剂、还原剂。回答下列问题:
(1)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水配制成100mL溶液。
②滴定:取0.00950mol/L的K2Cr2O7标准溶液20.00mL,硫酸酸化后加入过量KI,写出发生反应的离子方程式:____________________________________。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-=S4O62-+2I-。加入____________作为指示剂,继续滴定,当溶液________________________,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为____________%(保留1位小数)。
(2)①该实验中应该用____________式滴定管装K2Cr2O7标准溶液;
②开始时,滴定管尖嘴处无气泡,结束后发现尖嘴处有气泡出现,则测定结果____________(填“偏高”或“偏低”或“无影响”)。
(3)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为_______________________。
高二化学实验题中等难度题查看答案及解析
-
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol−1)可用作定影剂、还原剂。利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
(1)溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶解,完全溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
(2)滴定:取0.00950 mol·L−1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:Cr2O72−+6I−+14H+
3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32−
S4O62−+2I−。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,三次测定数据如下表:
实 验 序 号
1
2
3
消耗样品溶液体积/mL
24.79
22.30
24.81
则样品纯度为_________%(保留1位小数)。
(3)判断下列操作对测定硫代硫酸钠的纯度的影响(填“偏高”“偏低”或“无影响”)。
①若在溶液配制时,烧杯中的溶液有少量溅出,则测定结果________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果_______。
高二化学实验题中等难度题查看答案及解析
-
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol-1)可用作定影剂、还原剂。利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在_____________中溶解,完全溶解后,全部转移至100 mL的_____________中,加蒸馏水至_______________。
②滴定:取0.00950 mol·L-1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:Cr2O72-+6I-+14H+=3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-=S4O62-+2I-。加入淀粉溶液作为指示剂,继续滴定,当溶液_____________________________________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_______%(保留1位小数)。
高二化学填空题中等难度题查看答案及解析
-
某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,工厂为了防止环境污染,变废为宝,利用废铁屑和其他化学试剂进行如下操作,得到了绿矾(FeSO4·7H2O)、Al2O3和金属Cu,回答下列问题:
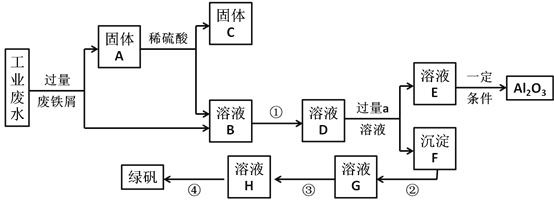
(1)固体C是_________(用化学式表示)。
(2)在过程①中需要通入足量的氯气,该过程中发生反应的离子方程式为__________。
(3)溶液E焰色反应呈黄色,溶液a是______________。
(4)沉淀F→溶液H中所用试剂:②_________,③____________。溶液G→溶液H反应的离子方程式是_______________________。
(5)实验室中由溶液H得到绿矾的操作是:蒸发、浓缩___________、过滤。
高二化学综合题中等难度题查看答案及解析
-
某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,工厂为了防止环境污染,变废为宝,利用废铁屑和其他化学试剂进行如下操作,得到了铁红、Al2O3和金属Cu,回答下列问题:

(1)固体A的成分是____(用化学式表示)。
(2)写出B→D的离子方程式____,该反应中氧化剂是____,2 mol Cl2参加反应转移电子数____,溶液D中滴加KSCN溶液的现象是____。
(3)D→E反应的离子方程式是____。
高二化学工业流程中等难度题查看答案及解析
-
工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
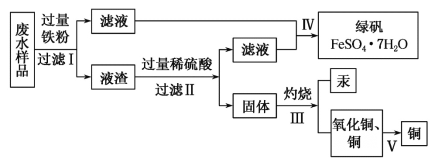
(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是__________设计简单实验检验绿矾是否变质,简述你的操作:__________。
(2)步骤Ⅰ中加入过量铁粉的目的是__________,步骤Ⅱ中__________(填“能”或“不能”)用盐酸代替硫酸。
(3)步骤V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案__________不好;从产品纯度考虑,方案__________不好。
(4)写出步骤Ⅱ中涉及反应的离子方程式:__________;步骤Ⅳ得到绿矾的操作蒸发浓缩__________、__________。
高二化学实验题困难题查看答案及解析