-
(10分)A、B、D、E 四种短周期元素,其原子序数逐渐增大。A 元素原子的核外电子数、电子层数和最外层电子数均相等,B、D、E 三种元素在周期表中相对位置如图①所示,E 的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z 七种物质均由A、B、D 三种元素中的一种或几种组成,其中只有M 分子同时含有三种元素;W 为A、B 两元素组成的18 电子分子,可做火箭燃料;甲、乙为非金属单质;X 分子含有10个电子。它们之间的转化关系如图②。
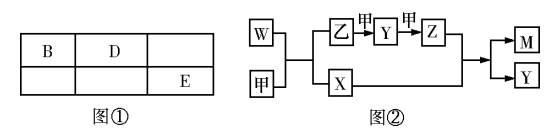
回答下列问题:
(1)Z的化学式为________。
(2)E 的单质与水反应的离子方程式为________。
(3)W—空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~30%的KOH溶液。W—空气燃料电池放电时,负极反应式为 ________。
(4)将一定量的A2、B2 的混合气体放入2L密闭容器中,在500°C、2°C×107 Pa下达到平衡。测得平衡气体的总物质的量为0.5mol,其中A2 为0.3mol,B2 为0.1mol。则该条件下A2 的平衡转化率为________,该温度下反应2BA3(g )
3A2(g)+B2(g)的平衡常数为________。
高三化学填空题简单题查看答案及解析
-
A、B、D、E四种元素均为短周期元素,原子序数逐渐增大。A元素原子的核外电子数、电子层数和最外层电子数均相等。B、D、E三种元素在周期表中的相对位置如图①所示,只有E元素的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子含有10个电子。它们之间的转化关系如图②所示。
B
D
E
图①
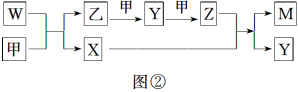
请回答下列问题:
(1)Z的化学式为__________________。
(2)E的单质与水反应的离子方程式为________________________________________。
(3)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W空气燃料电池放电时,正极反应式为________________________________,负极反应式为____________________。
(4)将一定量的A2、B2的混合气体放入1 L密闭容器中,在500 ℃、2×107 Pa下达到平衡。测得平衡气体的总物质的量为0.50 mol,其中A2为0.3 mol,B2为0.1 mol。则该条件下A2的平衡转化率为________,该温度下的平衡常数为____________(结果保留3位有效数字)。
高三化学填空题困难题查看答案及解析
-
有五种短周期主族元素 X、 Y、 Z、 M、 Q, 它们的原子序数逐渐增大; 在周期表中的位置如图所示, M 的电子层数与主族序数相等。 下列说法错误的是
A. 工业上用电解熔融的 Z 的氯化物制 Z
B. Y 和 Q 的最简单氢化物熔点: Y<Q
C. Z、 M、 Y 的简单离子半径: Y>Z>M
D. X 和 Y 的最简单氢化物的稳定性: X<Y
高三化学单选题中等难度题查看答案及解析
-
A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素。A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能。E是第四期第IB族元素,回答下列问题:
A
B
D
⑴E原子的基态电子排布式 ______;
⑵A、B、C三种元素的第I电离能由大到小的顺序是 ______;
⑶D能形成多种价态的含氧酸,其酸性由强到弱的顺序为 ______;
⑷已知金属C单质的晶胞为
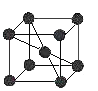 ,则C原子的堆积方式为 ______ ,C原子的配位数是 ______ ;
,则C原子的堆积方式为 ______ ,C原子的配位数是 ______ ;⑸向E、D形成的稳定化合物溶液中不断加入A的常见氢化物水溶液,最后E的最主要存在形式为
写真实符号
______。
高三化学综合题简单题查看答案及解析
-
图甲为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
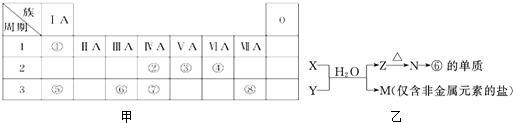
(1)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:______,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.
(2)以上元素可形成多种化合物,其中既含离子键又含非极性共价键的化合物的电子式为______.
(3)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
(4)由图甲中元素形成的常见物质X、Y、Z、M、N可发生图乙所示反应:编号 性质 化学方程式 示例 氧化性 H2WO3+3H3PO3═3H3PO4+H2W↑ 1 ______ ______ 2 ______ ______
X溶液与Y溶液反应的离子方程式______;
N→⑥的单质的化学方程式为______电解4Al+3O2↑高三化学解答题中等难度题查看答案及解析
-
【选修3:物质结构与性质】(13分)原子序数逐渐增大的元素A,B,C,D,E,F的有关信息如下:

根据以上表格信息回答:
(1)元素F在周期表中的位置是 ,E形成的低价离子的电子排布式为 。
(2)A、C的氢化放沸点较高的是(用所形成的氢化物表示) ,A,B,C的第一电离能大小顺序是(用元素符号表示) .
(3)A与氢元素形成的A2H2含有的
键数目之比为 。
(4)KCl的晶胞如图:则该晶胞中含有K+为 个.已知晶胞参数为:629.8pm(lpm=10-12m),求KCl晶体的密度为 g/cm3(只写出表达式,不要求计算结果).
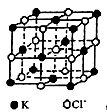
(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl。请写出析出白色固体的阴极反应式 .
高三化学简答题困难题查看答案及解析
-
元素性质随着原子序数的递增呈周期性变化的根本原因是( )
A.核电荷数逐渐增大,元素化合价呈现周期性变化
B.元素的相对原子质量逐渐增大
C.核外电子排布呈由不稳定结构到稳定结构的周期性变化
D.元素原子半径呈由大到小的周期性变化高三化学选择题中等难度题查看答案及解析
-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期元素的第一电离能随原子序数的增大,总趋势逐渐增大。镓
的基态电子排布式是_____,
的第一电离能明显低于
,原因是______。
(2)多酚氧化酶与植物的抗病性有关。配合物
是多酚氧化酶的模型配合物。
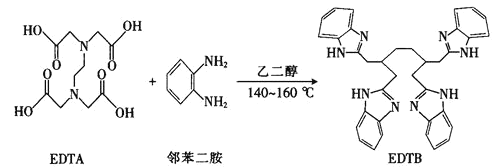
一个EDTA分子中
键的数目为______________。
分子中所含元素的电负性由小到大的顺序为______________________。
与
互为等电子体的一种阴离子为___________________。
配离子
中的配位原子是__________________。
(3)向盛有硫酸铜水溶液的试管中加氨水,首先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,再向该溶液中加入乙醇,析出深蓝色晶体。蓝色沉淀先溶解,后析出的原因是____________________________________________
用相关的离子方程式和简单的文字说明加以解释
。
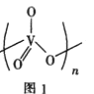
(4)
溶解在NaOH溶液中,可得到钒酸钠
,该盐阴离子中V的杂化轨道类型为______________;也可以得到偏钒酸钠,其阴离子呈如图1所示的无限链状结构,则偏钒酸钠的化学式为_________________________。
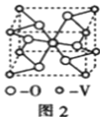
(5)钒的某种氧化物晶胞结构如图2所示。该氧化物的化学式为_____________,若它的晶胞参数为
,则晶胞的密度为__________
写计算式
。
高三化学综合题困难题查看答案及解析
-
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。
镓(31Ga)的基态电子排布式是_________________________________________;
31Ga的第一电离能却明显低于30Zn,原因是______________________________________;
Ⅱ.第四周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为________________。NH3 分子中N原子的杂化方式为_______杂化,NH3分子的空间立体构型是____________。
(2)向盛有硫酸铜水溶液的试管中加氨水,首先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加乙醇,析出深蓝色晶体。蓝色沉淀先溶解,后析出的原因是:__________________________________________(用相关的离子方程式和简单的文字说明加以解释)
(3)如图甲所示为二维平面晶体示意图,所表示的化学式为AX3的是________。
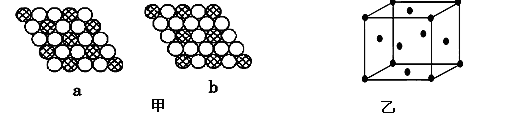
(4)图乙为一个金属铜的晶胞,此晶胞立方体的边长为acm,Cu的相对原子质量为64,金属铜的密度
为ρ g/cm3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
高三化学填空题困难题查看答案及解析
-
元素性质呈周期性变化的基本原因是
A.元素的原子量逐渐增大 B.核外电子排布呈周期性变化
C.核电荷数逐渐增大 D.元素化合价呈周期性变化
高三化学单选题简单题查看答案及解析