-
铁触媒常作为合成氨的催化剂,CO会使催化剂中毒。可用CH3COO[Cu(NH3)2]溶液吸收CO。
(1)Cu2+基态核外电子排布式为________________。
(2)C、N、O的电负性由大到小的顺序为________________。
(3)1 mol CH3COO[Cu(NH3)2]中含有σ键的数目为________________mol,其中C原子轨道的杂化类型是________________。
(4)与CO分子互为等电子体的阴离子为________________。
(5)Cu和Fe都可以形成多种氧化物。其中FexO晶胞结构为NaCl型,由于晶体缺陷,x值小于1。若FexO中的x=0.92,则该此晶体化学式为________________(用Fe2+aFe3+bO形式表示)。
高三化学综合题中等难度题查看答案及解析
-
工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是__(填字母序号)。
a.
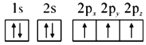 b.
b.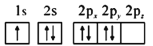
c.
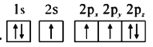 d.
d.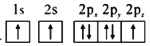
(2)写出CO的一种常见等电子体的结构式:___;C、N、O的第一电离能由大到小的顺序为__(用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是___。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,1mol[Cu(NH3)2]+中含有σ键的数目___。则其中碳原子的杂化轨道类型是__,NH3分子的价电子对互斥理论模型是___。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
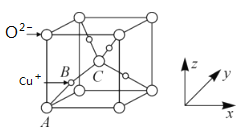
①若坐标参数A为(0,0,0),B为(
,
,
),则C的坐标参数为__;
②若阿伏加德罗常数为NA,该晶胞的边长为apm,则晶体的密度为___g•cm-3。
高三化学综合题中等难度题查看答案及解析
-
工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是______(填字母序号)。
a.
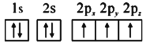 b.
b.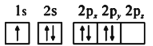
c.
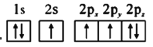 d.
d.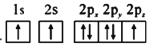
(2)写出CO的一种常见等电子体的结构式:_______;C、N、O的电负性由大到小的顺序为______(用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们简单氢化物的沸点从高到低的顺序为______,其原因为______。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价, [Cu(NH3)2]+中中心离子的电子排布式为______,其中碳原子的杂化轨道类型是______,NH3分子的VSEPR模型为______。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:
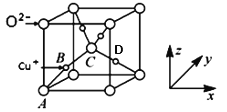
①若以A点为原点建立坐标系,A的坐标为(0,0,0),B的坐标为(
),则D的坐标为______;
②若阿伏加德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为______g•cm-3。
高三化学综合题中等难度题查看答案及解析
-
选做[化学—物质结构与性质](13分)氨是重要的化工原料,用途很广。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 (填元素名称)。
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有 (填标号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有 种(不含Cu)。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3 = F3B—NH3 。
①BF3和NH3分子的空间构型分别为 、 。
②晶体F3B—NH3中,B原子的杂化轨道类型为 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质易溶于水,在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
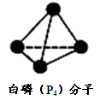
①下列相关说法中,正确的是 (填序号)。
a.N4是N2的同分异构体
b.1mol N4 分解生成N2,形成了4mol π键
c.白磷的沸点比N4高,原因是P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键): 。
高三化学填空题极难题查看答案及解析
-
氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度 g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 。
②写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是 (填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 mol π键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键) 。
高三化学填空题困难题查看答案及解析
-
氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是____________。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有________(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有____种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度_____ g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 ______________。
②写出两种与BF3具有相同空间构型的阴离子_____________。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是_____________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键)___________。
高三化学简答题困难题查看答案及解析
-
合成氨工业中,原料气(N2、H2,混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为:CH3COO[Cu(NH3)2]+CO+NH3CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是________________________________________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是_____________________________。
(3)吸收CO后的醋酸二氨合铜(Ⅰ)溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是__________________________________________________________。
高三化学填空题中等难度题查看答案及解析
-
CO 易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5; [Cu(NH3)2]Ac 溶液用于除去CO的化学反应方程式:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3] Ac·CO (式中Ac-代表醋酸根)。请回答下列问题:
(1)C、N、O的第一电离能最大的是_____________,原因是___________________________。基态Fe 原子的价电子排布图为___________________________。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_____________,羰基铁的结构如图,根据该图可知CO作为配位体是以__________原子为配位原子与Fe原子结合。
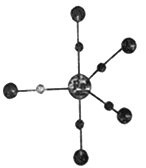
(3)离子水化能是气态离子溶于大量水中成为无限稀释溶液时释放的能量。离子在溶液中的稳定性可以从离子的大小、电荷、水化能等因素来解释。Cu2+和Cu+的水化能分别是-2121kJ·mol-1和-582 kJ·mol-1,在水溶液里Cu2+比Cu+稳定的原因是_______________________________。[Cu(NH3)2]+在水溶液中相对稳定,在配合物[Cu(NH3)2]Ac中碳原子的杂化类型是________________________________。
(4)用[Cu(NH3)2]Ac除去CO的反应中,肯定有形成________________。
a.离子键 b.配位键 c.非极性键 d. σ键
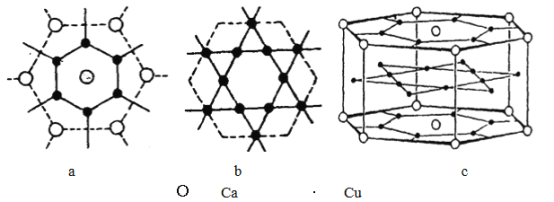
(5)钙铜合金的晶体结构可看成(a) (b) 两种原子层交替堆积排列而成图(c),则该合金六方晶胞(即平行六面体晶胞)中含为Cu________个。已知同层的Ca-Cu的距离为294pm,根据图示求同层相邻Ca-Ca的距离__________pm (已知
=1.73 计算结果保留整数)。
高三化学综合题困难题查看答案及解析
-
在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸)Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。
请回答下列问题:
(1)化合物Cu(NH3)3(CO)Ac中,铜元素的化合价为___。
(2)该反应中含有的第二周期非金属元素的第一电离能由大到小的顺序是___。
(3)写出基态Cu2+的电子排布式:___,向Cu2+的溶液中加入过量NaOH溶液,可生成Cu2+配位数为4的配位离子,写出该配位离子的结构式___。
(4)CO与N2互为等电子体,二者沸点较高的是___,理由是____。
(5)在一定条件下,NH3和CO2能合成尿素CO(NH2)2,尿素中碳原子和氮原子的杂化轨道类型分别是:___和___。
(6)Cu与O形成的某种化合物的晶胞结构如图所示。
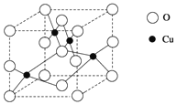
①在一个晶胞中,氧原子的数目为___。
②该化合物的化学式为____。
③晶胞的边长为apm,则该晶胞的密度为_____g•cm-3。
高三化学综合题中等难度题查看答案及解析
-
铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:除去CO的化学反应方程式为:[Cu(NH3)]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
请回答下列问题
(1)基态Fe原子的核外电子排布式为______________________;
(2)铁的一种配合物Fe(CO)x的中心原子价电子数与配体用于成键提供的电子数之和为18,则x=__________;已知该配合物的熔点为-20.5℃,沸点为103℃,易溶于CC14,据此可以判断Fe(CO)x晶体属于___________(填晶体类型)。与CO互为等电子体的分子的分子式为___________。
(3)配合物[Cu(NH3)]OOCCH3中碳原子的杂化类型是___________。用[Cu(NH3)]OOCCH3除去CO的反应中,肯定有___________形成。
a.离子键 b.配位键 c.非极性键 d.σ键
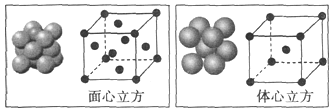
(4)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为___________。铁晶体的体心立方堆积空间利用率为___________(用含π的式子表示)。
高三化学综合题困难题查看答案及解析