-
氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度 g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 。
②写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是 (填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 mol π键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键) 。
高三化学填空题困难题查看答案及解析
-
氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是____________。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有________(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有____种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度_____ g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3+NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 ______________。
②写出两种与BF3具有相同空间构型的阴离子_____________。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是_____________(填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 molπ键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键)___________。
高三化学简答题困难题查看答案及解析
-
选做[化学—物质结构与性质](13分)氨是重要的化工原料,用途很广。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 (填元素名称)。
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有 (填标号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有 种(不含Cu)。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3 = F3B—NH3 。
①BF3和NH3分子的空间构型分别为 、 。
②晶体F3B—NH3中,B原子的杂化轨道类型为 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质易溶于水,在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
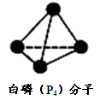
①下列相关说法中,正确的是 (填序号)。
a.N4是N2的同分异构体
b.1mol N4 分解生成N2,形成了4mol π键
c.白磷的沸点比N4高,原因是P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键): 。
高三化学填空题极难题查看答案及解析
-
氨是重要的化工原料,用途很广。
合成氨工厂常用醋酸二氨合铜
由
和
构成
溶液吸收对氨合成催化剂有毒害的CO气体。
醋酸二氨合铜所含的元素中,第一电离能最大的是 ______
填元素名称
。
醋酸二氨合铜所含元素组成的单质,所属的晶体类型有 ______
填标号
。
离子晶体
分子晶体
原子晶体
金属晶体
第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有 ______ 种
不含
。
气体与
相遇立即生成一种白色晶体:
。
和
分子的空间构型分别为 ______ 、 ______ 。
晶体
中,B原子的杂化轨道类型为 ______ 。
可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为
的物质。该物质易溶于水,在水溶液中以
和
两种正四面体构型的离子存在。
遇碱生成一种形似白磷的
分子。

下列相关说法中,正确的是 ______
填序号
。
是
的同分异构体
分解生成
,形成了4mol
键
白磷的沸点比
高,原因是
键键能比
键大
白磷的化学性质比
活泼,说明P的非金属性比N强
画出
的结构
标明其中的配位键
: ______ 。
高三化学综合题中等难度题查看答案及解析
-
合成氨工业中,原料气(N2、H2,混有少量CO、NH3)在进入合成塔之前,常用醋酸二氨合铜(Ⅰ)溶液来吸收CO,其反应为:CH3COO[Cu(NH3)2]+CO+NH3CH3COO[Cu(NH3)3]·CO(正反应为放热反应)。
(1)必须除去CO的原因是________________________________________________________。
(2)醋酸二氨合铜(Ⅰ)溶液吸收原料气中CO的适宜条件是_____________________________。
(3)吸收CO后的醋酸二氨合铜(Ⅰ)溶液经适当处理又可再生,恢复其吸收CO的能力而循环使用,其再生的条件是__________________________________________________________。
高三化学填空题中等难度题查看答案及解析
-
合成氨工业中原料气(H2、CO的混合气)在进入合成塔前常用醋酸亚铜氨溶液来吸收原料气中的CO:Cu(NH3)2Ac(溶液)+CO(g)⇌Cu(NH3)2Ac•CO(溶液)+Q kJ(Q>0),吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨.
(1)写出该反应的平衡常数表达式K=______;升高温度K值将______(选填“增大”“减小”“不变”).
(2)必须除去原料气中CO的原因是______,欲充分吸收CO,适宜的条件是______(选填序号)
a.升高温度 b.增大压强 c.增大醋酸亚铜氨溶液浓度
吸收CO时,溶液中Cu(NH3)2Ac和Cu(NH3)2Ac•CO的浓度(mol/L)变化情况如下:
(3)前30min Cu(NH3)2Ac的平均反应速率为______;0min 30min 45min 60min 90min Cu(NH3)2Ac 2.0 1.2 0.9 0.9 1.8 Cu(NH3)2Ac•CO a 1.1 1.1 0.2
(4)60min时改变的条件可能是______.高三化学解答题中等难度题查看答案及解析
-
合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用[Cu(NH3)2]Ac [醋酸二氨合铜(I)]溶液来吸收原料气中的CO,其反应是:[Cu(NH3)2]Ac+CO+NH3
[Cu(NH3)3]Ac
⑴配合物[Cu(NH3)2]Ac中,中心离子的基态价电子排布式为_______。
(2)醋酸根离子中碳原子轨道杂化类型为__________。
(3)1mol 配离子[Cu(NH3)3CO]+中σ键和π键的数目之比为______。
(4)NH3的空间构型是___(用文字描述):与CO互为等电子体的阴离子可以是____。
(要求:由题中涉及的元素原子构成,用电子式表示)。
(5)铜的化合物种类很多,下图是某铜的氯化物的晶胞结构,该氯化物能溶于浓氨水可得无色溶液(配合物中配位数为2),请完成有关反应的离子方程式:______。
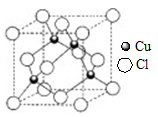
高三化学简答题中等难度题查看答案及解析
-
合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收原料气中的CO,其反应是:[Cu(NH3)2CH3COO]+CO+NH3
[Cu(NH3)3]CH3COO·CO(正反应为放热反应)
(1)必须除去原料气中的CO的原因是 。
(2)醋酸二氨合铜(Ⅰ)溶液吸收CO的生产适宜条件是 。
(3)吸收CO后的醋酸铜氨溶液经过适当处理又可再生,恢复其吸收CO的能力以供循环使用,醋酸铜氨溶液再生的适宜条件是 。
高三化学填空题中等难度题查看答案及解析
-
在炼油工业中常用醋酸铜氨溶液{含[Cu(NH3)2]+、CH3COO-和NH3}除去H2中的CO、O2及H2S气体。
(1)已知醋酸铜氨溶液吸收CO的反应为:
[Cu(NH3)2]+(aq)+CO(g)+NH3(g)
[Cu(NH3)3·CO]+(aq)
若反应在恒容密闭容器中进行,则能说明该反应已达到平衡状态的是 。
a.v(CO)正=v(NH3)正
b.容器内气体压强不再随时间变化
c.[Cu(NH3)2]+浓度不再随时间变化
(2)醋酸铜氨溶液吸收CO一段时间后将失效,用下列方法可回收废醋酸铜氨溶液中的铜。
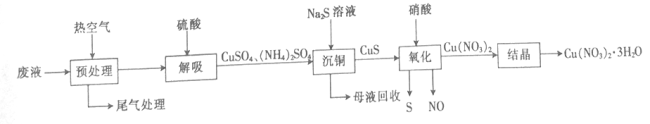
“预处理”时,尾气中除N2、CO、O2、CO2及H2O外,还有 。
②加入硫化钠溶液时发生反应的离子方程式为 。
③加入硝酸时发生反应的化学方程式为 。
④已知上述流程中只有“沉铜”和“结晶”步骤铜元素有损耗。“沉铜”时铜元素的损耗率为4%;“结晶”时铜元素的损耗率为2%。若1L废液最终制得Cu(NO3)2·3H2O 363g,则1L废液中铜元素的质量为 g。
高三化学填空题简单题查看答案及解析
-
合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用Cu(NH3)2Ac溶液来吸收原料气中的CO,其反应是:
Cu(NH3)2Ac + CO + NH3
[Cu(NH3)3]Ac·CO + Q
生产中必须除去原料气中CO的原因是________;Cu(NH3)2Ac溶液吸收原料气中的CO的生产适宜条件应是________。
高三化学选择题中等难度题查看答案及解析