-
氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
高三化学选择题中等难度题查看答案及解析
-
(14分)“氢能”将是未来最理想的新能源。
Ⅰ 在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 。
Ⅱ 氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g)
CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。
(1)若升高温度至950℃,达到新平衡状态时K (填“>”、“<”或“=”)1。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0 molCO、3.0mol H2O、1.0 molCO2和x mol H2,则:
①当x = 5.0时,上述平衡向 (填“正反应”或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是 。
③若设x=5.0 mol和x=6.0 mol,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a (填“>”、“<”或“=”)b。
Ⅲ 海水淡化获得淡水的过程也可以产生氢气。下面是利用电渗析法处理海水获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:
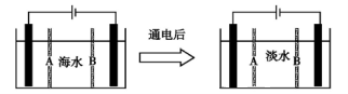
(1)阳离子交换膜是指______________ (填A或B)。
(2)写出通电后阳极的电极反应式:_________________________________________,在阴极区观察到的现象是:_________________________________________。
高三化学选择题困难题查看答案及解析
-
在新能源中,氢能将会成为21世纪最理想的能源,但现阶段氢气的主要用于合成氨工业。
Ⅰ.已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数据如下:
物质
氢气
原煤
(主要成份是C)
汽油
(主要成份C8H18)
热量(kJ)
285.8
250.9
4910
(1)H2燃烧的热化学方程式是__________________。
(2)工业上电解饱和盐水的副产物之一是H2,反应的离子方程式是_____________。
Ⅱ.德国人发明了合成氨反应,其原理为: N2(g)+3H2(g)
2NH3(g);已知298 K时,ΔH=-92.4 kJ·mol-1, 在500℃,20Mpa时,将氮气和氢气通入到体积为2升的密闭容器中,反应过程中各种物质的量变化如右图所示。
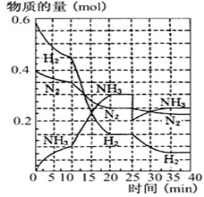
(1)10分钟内用氨气表示该反应的平均速率,V(NH3)= ________
(2)在10-20分钟内氨气浓度变化的原因可能是 (填空题)
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)N2(g)+3H2(g)
2NH3(g);该可逆反应达到平衡的标志 (填字母)
A.3v正(H2)=2v逆(NH3)
B.混合气体的密度不再随时间变化
C.容器内的压强不再随时间而变化
D.N2、H2、NH3的分子数比为1:3:2
E.单位时间生成nmolN2,同时生成3nmolH2
F.amol 氮氮三键断裂的同时,有6 amol氮氢键合成
高三化学填空题简单题查看答案及解析
-
在众多的新能源中,氢能将会成为21世纪最理想的能源。
Ⅰ. 已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数据如下:
物质
氢气
原煤
(主要成份是C)
汽油
(主要成份C8H18)
热量(kJ)
285.8
250.9
4910
(1)H2燃烧的热化学方程式是_____________________。
(2)H2可以代替原煤和汽油作为新能源的依据是_____________________。
(3)工业上电解饱和食盐水的副产物之一是H2,反应的离子方程式是_____________。
Ⅱ. 如图所示,硫酸工业中产生的SO2通过下列过程既能制得H2SO4又能制得H2。
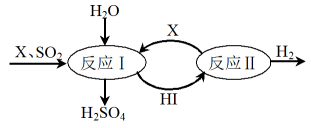
请回答:
(1)该过程可循环利用的物质是_______________(写化学式)。
(2)该过程总反应的化学方程式是_____________________。
(3)尾气中的SO2可用NaOH溶液吸收,同时可得含Na2SO3的样品,为测定样品中Na2SO3的质量分数,甲同学设计实验如下(夹持及加热装置略):
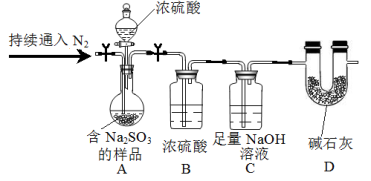
① 装置B的作用是 。
② 测定样品中Na2SO3的质量分数所需的数据是 。
高三化学实验题困难题查看答案及解析
-
“氢能”是人类未来最理想的新能源之一。
(1)实验测得,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为__________________________。
(2)利用核能把水分解制氢气,是目前正研究的课题。如图是其中的一种流程,流程中用了过量的碘(提示:反应②的产物是O2、SO2和H2O)。
完成下列反应的化学方程式:反应①________________;反应②________________。此法制取氢气的最大优点是____________________。
高三化学填空题简单题查看答案及解析
-
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料,而氢气、二甲醚等都是很有发展前景的新能源。
(1)在25℃、101kPa时,1gCH4完全燃烧生成液态水时放出的热量是55.64 kJ,则表示甲烷燃烧热的热化学方程式是___________________________________________。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(l)
ΔH=-2 220.0 kJ· mol-1,已知CO气体燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-565.14 kJ·mol-1,试计算相同物质的量的C3H8和CO燃烧产生的热量的比值________(保留小数点后一位)。
(3)氢气既能与氮气发生反应又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1
3H2(g)+N2(g)
2NH3(g) ΔH=-92.4 kJ· mol-1
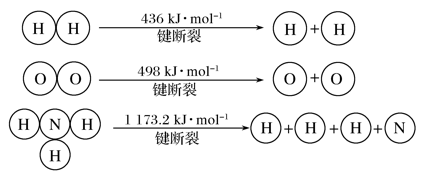
计算断裂1 mol N≡N键需要消耗能量________kJ。
(4)由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:①CO(g)+2H2(g)===CH3OH(g) ΔH1=-90.1 kJ· mol-1
②CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH2=-49.0 kJ· mol-1
水煤气变换反应:③CO(g)+H2O(g)===CO2(g)+H2(g) ΔH3=-41.1 kJ· mol
二甲醚合成反应:④2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ· mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为_______________________。根据化学反应原理,分析增大压强对直接制备二甲醚反应的影响:_________________________________________________。
高三化学简答题中等难度题查看答案及解析
-
科学家预测“氢能”将是未来最理想的新能源.请回答下列问题:
(1)实验测得,1克氢气燃烧生成液态水放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为______
A.2H2(g)+O2(g)=2H2O(l);△H=-142.9kJ/mol
B.H2(g)+1/2O2(g)=H2O(l);△H=-285.8kJ/mol
C.2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
D.H2(g)+1/2O2(g)=H2O(g);△H=-285.8kJ/mol
(2)根据“绿色化学”的思想,为了制备H2,某化学家设计了下列化学反应步骤:
①CaBr2+H2OCaO+2HBr ②2HBr+Hg
HgBr2+H2↑
③HgBr2+CaOHgO+CaBr2 ④2HgO
2Hg+O2↑
上述过程的总反应可表示为______.
(3)利用核能把水分解,制出氢气,是目前许多国家正在研究的课题.下图是国外正在研究中的一种流程(硫-碘热循环法),其中用了过量的碘.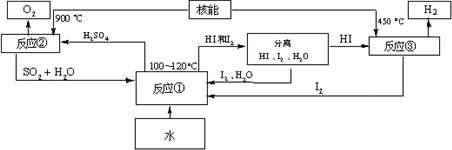
请写出反应①的化学方程式:______.
用硫-碘热循环法制取氢最大的优点是______.
(4)也有人认为利用氢气作为能源不太现实.你的观点呢?请说明能够支持你的观点的两点理由______.高三化学解答题中等难度题查看答案及解析
-
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
(1)在25℃、101kPa时,16gCH4完全燃烧生成液态水时放出的热量是890.31kJ,则CH4燃烧的热化学方程式为 .
(2)已知:C(s)+O2(g)═CO2(g);△H=﹣437.3 kJ•mol﹣1
H2(g)+O2(g)═H2O(g);△H=﹣285.8 kJ•mol﹣1
CO(g)+O2(g)═CO2(g);△H=﹣283.0 kJ•mol﹣1
则煤气化反应C(s)+H2O(g)═CO(g)+H2(g) 的焓变△H= kJ•mol﹣1.
(3)如图所示组成闭合回路,其中,甲装置中CH4为负极,O2和CO2的混合气体为正极,稀土金属材料为电极,以熔融碳酸盐为电解质;乙装置中a、b为石墨,b极上有红色物质析出,CuSO4溶液的体积为200mL.
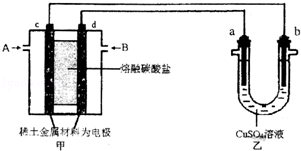
①装置中气体A为 (填“CH4”或“O2和CO2”),d极上的电极反应式为 .
②乙装置中a极上的电极反应式为 .若在a极产生112mL(标准状况)气体,则甲装置中消耗CH4 mL(标准状况),乙装置中所得溶液的pH= .(忽略电解前后溶液体秋变化)
③如果乙中电极不变,将溶液换成饱和Na2SO3溶液,当阴极上有a mol气体生成时,同时有w g Na2SO4•10H2O晶体析出,若温度不变,剩余溶液中溶质的质量分数应为 (用含w、a的表达式表示,不必化简).
高三化学填空题困难题查看答案及解析
-
“氢能”将是未来最理想的新能源。
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
A.2H2(g)+O2(g)
2H2O(l) △H= -142.9kJ·mol—1
B.H2(g)+1/2 O2(g)
H2O(l) △H= -285.8kJ·mol—1
C.2H2+O2
2H2O(l) △H= -571.6kJ·mol—1
D.H2(g)+1/2 O2(g)
H2O(g) △H= -285.8kJ·mol—1
Ⅱ.某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤
①CaBr2+H2O
CaO+2HBr ②2HBr+Hg
HgBr2+H2
③HgBr2+_____
______________ ④2HgO
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:____________。
根据“绿色化学”的思想评估该方法制H2的主要缺点:______________。
Ⅲ.利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。(提示:反应②的产物是O2、SO2和H2O)

完成下列反应的化学方程式:
反应①__________________________;反应②__________________________。
此法制取氢气的最大优点是_______________________________________________。
Ⅳ.氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g)
CO2(g)+ H2(g); △H<0。
在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2 和 x mol H2,则:
①当x=5.0时,上述平衡向___________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a _______ b(填“大于”、“小于”或“等于”)。
Ⅴ.氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。
(1)现有8克氧化铜被氢气还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是________;
(2)若将6.8克上述混合物与足量的稀硫酸充分反应后过滤,可得到固体________g;
(3)若将6.8克上述混合物与一定量的浓硝酸充分反应,
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是________,其物质的量之比是________;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68g。经分析,原溶液中的Cu2+有20%残留在母液中。求所得晶体的化学式
高三化学填空题中等难度题查看答案及解析
-
下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧后都恢复至常温,后者放热量多
B.在101 kPa 时,2 g H2 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为:2H2 (g) + O2 (g) = 2H2O (l) ;△H = +285.8 kJ / mol
C. 已知中和热为57.3 kJ·mol-1,若将含0.5mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量大于57.3kJ
D.Ba(OH)2·8H2O (s) + 2NH4Cl (S) = BaCl2 (s) + 2NH3(g) + 10H2O(l); △H<0
高三化学选择题中等难度题查看答案及解析