-
工业上制取三氧化硫反应的热化学方程式为:
2SO2(g)十O2(g)  2SO3(g) △H=-198kJ·mol-1
2SO3(g) △H=-198kJ·mol-1
(1)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是________(填序号)。
A.每生成1mol SO3的同时生成0.5mol O2
B.容器中混合气体的密度不变
C.SO2、O2、SO3的物质的量之比为2:1:2
D.容器中气体总压强不变
(2)400℃,1.01×105Pa下,上述反应中n(SO3)和n(O2)随时间变化的关系如图所示。下列叙述正确的是________(填序号)。

A.点a的正反应速率比点b的大
B.点c处反应达到平衡状态
C.点d和点e处的n(O2)相同
D.500℃,1.01×105Pa下,反应达到平衡时,n(SO3)比图中e点的值大
(3)已知该反应的K(400℃)=7200mol-1·L。在400℃时,容积为1.0L的密闭容器中充入0.05mol SO2(g)和0.03mol O2(g),反应一段时间后,有0.04mol SO3生成。此时,该反应________(填“是”、“否”或“无法判断”)达到化学平衡状态,理由是________。
-
工业上制取三氧化硫反应的热化学方程式为:2SO2(g)十O2(g)⇔2SO3(g)△H=-198kJ•mol-1
(1)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是________(填序号).
A.每生成1mol SO3的同时生成0.5mol O2
B.容器中混合气体的密度不变
C.SO2、O2、SO3的物质的量之比为2:1:2
D.容器中气体总压强不变
(2)400℃,1.01×105Pa下,上述反应中n(SO3)和n(O2)随时间变化的关系如图所示.下列叙述正确的是________(填序号).
A.点a的正反应速率比点b的大
B.点c处反应达到平衡状态
C.点d和点e处的n(O2)相同
D.500℃,1.01×105Pa下,反应达到平衡时,n(SO3)比图中e点的值大
(3)已知该反应的K(400℃)=7200mol-1•L.在400℃时,容积为1.0L的密闭容器中充入0.05mol SO2(g)和0.03mol O2(g),反应一段时间后,有0.04mol SO3生成.此时,该反应________(填“是”、“否”或“无法判断”)达到化学平衡状态,理由是________.

-
(16分)
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g)
2SO3(g)
(1)此反应是工业上生产 的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 (填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
① 根据有关数据,请分析在工业生产中选择常压反应器的原因:
。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g) △H= 。
2SO3(g) △H= 。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下:

① 求该温度时,氨水的电离平衡常数K= 。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1 ~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
① a b (填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3·H2O)= 。
(用含有a、b的式子表示)
-
已知热化学方程式 2SO3(g) 2SO2(g) + O2(g);△H1 = +197kJ/mol, 热化学方程式:2SO2(g) + O2(g)
2SO2(g) + O2(g);△H1 = +197kJ/mol, 热化学方程式:2SO2(g) + O2(g) 2SO3(l);△H2 = — a kJ/mol 则下列说法正确的是( )
2SO3(l);△H2 = — a kJ/mol 则下列说法正确的是( )
A.a>197
B.a<197
C.a=197
D.热方程式中化学计量数可表示分子个数
-
二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:
I:2SO2(g)+O2(g) 2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
为研究该反应,某同学设计了以下三种已装固体V2O3催化剂的密闭容器装置

(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2 mol SO2、1molO2投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为___________(用“甲、乙、丙”表示)。
(2)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应得到数据如下表:
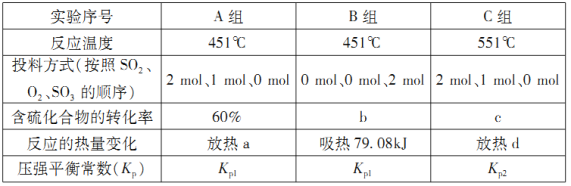
①表中:a=___________;b=___________。
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1=___________;Kp1___________Kp2(填“>”、“<”或“=”)。
③若按0.4 mol SO2、0.4molO2、0.4 mol SO3进行投料,则反应开始时v正(SO2)_______v逆(SO2)(填“>”、“<”或“=”)。
(3)将上述固体催化剂V2O5换成NO2气体同样可以对该反应起到催化作用,此催化过程如下:
Ⅱ:SO2(g)+NO2(g) SO3(g)+NO(g) △H2 K2(浓度平衡常数)
SO3(g)+NO(g) △H2 K2(浓度平衡常数)
Ⅲ:2NO(g)+O2(g) 2NO2(g) △H3=-114.1kJ·mol-1 K3(浓度平衡常数)
2NO2(g) △H3=-114.1kJ·mol-1 K3(浓度平衡常数)
△H2=___________;K3=___________(用含有K1、K2的表达式表示)。
-
“绿水青山就是金山银山”。研究含氮和含硫化合物的性质在工业生产和环境保护中有重要意义。
(1)制备硫酸可以有如下两种途径:
2SO2(g)+O2(g)2SO3(g)ΔH=-198 kJ· mol-1
SO2(g)+NO2(g)SO3(g)+NO(g) ΔH=-41.8 kJ· mol-1
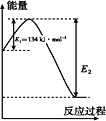
若CO的标准燃烧热为 283 kJ· mol-1,则1 mol NO2和1 mol CO反应生成CO2和NO的能量变化示意图中E2=________kJ· mol-1。
(2)已知某温度下,H2SO3的电离常数为K1≈1.5×10-2,K2≈1.0×10-7,用NaOH溶液吸收SO2。当溶液中HSO3-、SO32-离子浓度相等时,溶液的pH约为_______________。
(3)连二亚硫酸钠(Na2S2O4)具有强还原性,废水处理时可在弱酸性条件下加入亚硫酸氢钠电解产生连二亚硫酸根,进而将废水中的HNO2还原成无害气体排放,连二亚硫酸根氧化为原料循环电解。产生连二亚硫酸根的电极反应式为________________,连二亚硫酸根与HNO2(HNO2的电离常数为Ka=5.1×10-4)反应的离子方程式为________________________________。
(4)锅炉烟道气含CO、SO2,可通过如下反应回收硫:2CO(g)+SO2(g) S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。
S(l)+2CO2(g)。某温度下在2 L恒容密闭容器中通入2 mol SO2和一定量的CO发生反应,5 min后达到平衡,生成1 mol CO2。
①其他条件不变时,随着温度的升高,SO2的平衡转化率变化如图A,请解释其原因________________________________。(已知硫的沸点约是445°C)
②保持其他条件不变,第8分钟时,将容器体积迅速压缩至1 L,在10分钟时达到平衡,CO的物质的量变化了1 mol。请在图B中画出SO2浓度6~11分钟的变化曲线。______

-
已知热化学方程式:2SO2(g)+O2(g)⇌2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 ( )。
A. 相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B. 将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ
C. 增大压强或升高温度,该反应过程放出更多的热量
D. 如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化
-
硫及其化合物对人类的生产和生活有着重要的作用.
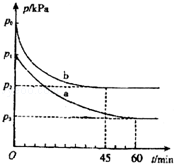
2SO2(g)+O2(g)⇌2SO3(g)△H=﹣198kJ•mol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如图所示.与实验a相比,实验b改变的条件是 ,判断的依据 .
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)⇌SO3(g)+NO(g)△H=﹣42kJ•mol﹣1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| | N(SO2) | N(NO2) | N(NO) |
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= ,该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,Tl T2(填“>”“<’’或“=”),判断的理由是 .
-
下列表述中正确的是
A.任何能使熵值减小的过程都能自发进行
B.已知热化学方程式2SO2(g)+O2(g) 2SO3(g);△H=-Q kJ·mol-1
2SO3(g);△H=-Q kJ·mol-1
(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出
Q kJ的热量
C.1mol NaOH分别和1mol CH3COOH、1molHNO3反应,后者比前者△H小
D.在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在
-
已知2SO2(g)+O2(g) 2SO3(g),△H=-198kJ/mol,在 V2O5存在时反应过程中的能量变化如图所示。下列叙述正确的是
2SO3(g),△H=-198kJ/mol,在 V2O5存在时反应过程中的能量变化如图所示。下列叙述正确的是
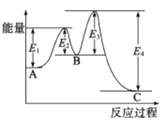
A. △H= E4- E3+E2-E1
B. 加入V2O5后反应经过两步完成,其中第一步决定反应速率
C. 加入V2O5,△H不变,但反应速率改变
D. 向密闭容器中充入2molSO2和1molO2,发生上述反应达平衡时,反应放热198kJ








