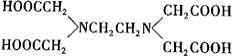-
[化学—选修物质结构和性质](15分)
下表为部分短周期元素的性质或原子结构,已知A—D的原子序数依次增大。
| 元素编号 | 元素性质或原子结构 |
| A | A原子所处的周期数、族序数、原子序数均相等 |
| B | 核外电子有6种不同运动状态 |
| C | 最简单氢化物的水溶液呈碱性 |
| D | 基态原子的S轨道电子数等于P轨道电子数 |
请结合表中信息完成下列各小题(答题时用所对应的元素符号)
A:(1)写出C原子的电子排布图____________
(2)A、B、C、D的第一电离能由大到小的顺序为______________
(3)用电离方程式表示C的最简单氢化物的水溶液呈碱性的原因 _______________
B:按照共价键理论,分子中每个原子的最外电子层电子数均已饱和。已知ABCD分子可能有三种不同结构,它们的结构可以从其他物质的结构中获得启发。
(4)ABC的结构式是___________。向其中插入一个D原子,若形成配位键(用→表示)则ABCD的结构式为______________分子中C的原子的杂化类型是______________;若无配位键则ABCD的结构式为___________分子中D原子的杂化类型为______________。
(5)BD2的电子式是____________将D原子换成等电子的 所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
所得ABCD的结构式为________,分子中C原子的杂化类型是______________。
(6)在ABCD的三种可能结构中B原子的杂化类型__________(填“相同”或“不相同”)
-
[化学选修3:物质结构与性质]
Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同.
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)化合物M的空间构型为______,其中心原子采取______杂化;化合物N在固态时的晶体类型为______.
(2)R、X、Y三种元素的第一电离能由小到大的顺序为______;
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为______(写分子式)
(4)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质.该反应的离子方程式为______.
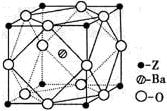
(5)Z原子基态时的外围电子排布式为______;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为______.
-
[化学-选修物质结构与性质]
Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
①Q为周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同.
请回答下列问题:(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)RQ4Y分子的某中心原子采用的杂化轨道类型是______杂化.
(2)R、X、Y三种元素的第一电离能由小到大的顺序为______.
(3)已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征.与RY分子互为等电子体的分子和离子分别为______和______(填化学式).
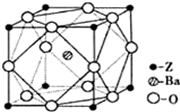
(4)Z元素位于周期表的______分区.Z原子基态时的外围电子排布式为______,Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个“Z”原子等距离且最近的氧原子数为______.
-
【化学——选修物质结构与性质】(15分)A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D原子的S电子与P电子数相等,E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式回答下列问题:
(1)A、B、C的电负性由小到大的顺序为 __;D的稳定离子核外有 种运动状态的电子 .
(2)A的最高价氧化物对应的水化物分子中其中心原子采取 杂化。
(3)已知A、C形成的化合物分子甲与B的单质分子结构相似, 1 mol甲中含有 键的数目为 。
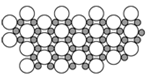
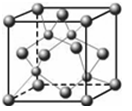
(4)科学家发现硼化D在39K时呈超导性,在硼化D晶体的理想模型中,D原子和硼原子是分层排布的,一层D一层硼相间排列。下图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是D原子投影,黑球是硼原子投影,图中的硼原子和D原子投影在同一平面上。根据图示确定硼化D的化学式为_______。
(5)E的外围电子排布式是 ;E的氢化物的晶体结构如下图所示,此氢化物化学式是 ;写出此氢化物在氯气中燃烧的化学方程式 。
-
化学选修:物质结构与性质分W、X、Y、M、Z为元素周期表中前四周期元素,且原子序数依次增大。W的基态原子中占据哑铃形原子轨道的电子数为3,X2+与W3-具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列,M是第四周期中核外未成对电子数最多的元素。
请回答:
(1)Z的基态原子M层的电子排布式为 ;
(2)W的简单氢化物分子中W原子的 轨道与H原子的 轨道重叠形成W-Hσ键。(填轨道名称)
(3)比较Y的含氧酸酸性:HYO2 HYO(填“>”或“<”),原因为 。
(4)强酸条件下,M2O72-离子能与乙醇反应生成M3+离子,该反应的离子方程式为 。
(5)关于Z的化合物[Z(EDTA)]SO4(EDTA的结构简式如图)的说法正确的是( )
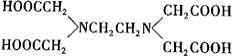
A.[Z(EDTA)]SO4中所含的化学键有离子键、共价键和配位键和氢键
B.EDTA中碳原子的杂化轨道类型为sp2、sp3
C.[Z(EDTA)]SO4的组成元素中第一电离能最大的是氧元素
D.[Z(EDTA)]SO4的外界离子的空间构型为正四面体
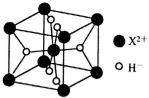
(6) ①离子型氢化物XH2的晶胞如图所示,其中阴离子的配位数为 。
②XH2是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为 。
③若该晶胞的密度为ρg.cm-3,则晶胞的体积为 nm3。
-
[化学——选修物质结构与性质](15分)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置;(2分)
D元素基态原子电子排布式为_____________________________。(2分)
(2)E的气态氢化物在同族元素中沸点最高的原因是:
________。(2分)
(3)A、C两元素第一电离能________>________。(填元素符号)(2分)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是________的原子。(2分)
(5)A元素可与氢元素形成离子化合物,电子式为_______________;(2分)这种离子化合物可与水反应,化学方程式为________________________________。(3分)
-
【化学—选修5:物质结构与性质】(15分)
现有A、B、C、D、E原子序数依次增大的五种元素,它们位于元素周期表的前四周期。A元素原子的价层电子总数是内层电子总数的2倍;C元素原子的L电子层中只有两对成对电子;D元素与E元素在同周期相邻的族,它们的原子序数相差3,且D元素的基态原子有4个未成对电子。请回答下列问题:
⑴A、B、C三种元素的名称分别为________、________、________。
⑵用元素符号表示A、B、C三种元素的第一电离能由低到高的排序为________。
⑶E元素基态原子的核外电子排布式为________。
⑷A元素与氢元素能形成种类繁多的化合物,其中只含sp3杂化且相对分子质量最小的分子的VSEPR空间构型为________;其中只含sp2杂化且相对分子质量最小的化合物的结构式为________;其中同时含sp杂化、SP2杂化、sp3杂化且相对分子质量最小的化合物的化学式为________。
⑸A元素的一种单质的晶体结构如图甲所示,D元素的一种单质的晶体结构如图乙所示。
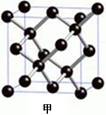
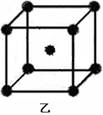
图甲中A原子的配位数与图乙中D原子的配位数之比为________。
-
【化学——选修3:物质结构与性质】A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C第一电离能由大到小的顺序为: (用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是: (填化学式);该分子中心原子的杂化类型为: 。
(3)A、C元素形成的常见含氧酸中,分子的中心原子的价层电子对数为4的酸是 ;(填化学式,下同)酸根呈平面三角形的酸是 。
(4)E和F形成的一种化合物的晶体结构如图所示,则该化合物的化学式为 ;F的配位数为 。

(5)D的离子可以形成多种配合物,由Dn+、Br-、C的
最高价含氧酸根和A的简单氢化物形成的1:1:1:5的某
配合物,向该配合物的溶液中滴加AgNO3溶液产生
淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物的化学式为: ;n值为 ;Dn+的基态电子排布式为: 。
-
[化学──选修3 :物质结构与性质](15分)X、Y 、Z、W为元素周期表前四周期的元素。其中X原子核外的L层电子数是K层电子数的两倍, Y的内层电子数是最外层电子数的9倍,Z在元素周期表的各元素中电负性最大,W元素的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题。
(1)W元素属于 区元素,其基态原子的电子排布式为 。
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。其中配体分子的空间构型为 ,写出该配离子的结构简式(标明配位键) 。
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为 ,1 mol 该分子中σ键的数目为 ,该物质易溶于水的主要原因是 。
(4)X的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为 。
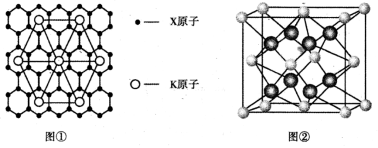
(5)元素Y与元素Z形成的晶体结构如图②所示,设晶胞中最近的Y的离子与Z的距离为a pm,该化合物的摩尔质量为bg/ mol ,则该晶胞密度的计算式为 g/cm3。
-
【化学——选修3:物质结构与性质】(15分)A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C第一电离能由大到小的顺序为: (用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是: (填化学式);该分子中心原子的杂化类型为: 。
(3)A、C元素形成的常见含氧酸中,分子的中心原子的价层电子对数为4的酸是 ;(填化学式,下同)酸根呈平面三角形的酸是 。
(4)E和F形成的一种化合物的晶体结构如图所示,则该化合物的化学式为 ;F的配位数为 。
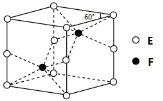
(5)D的离子可以形成多种配合物,由Dn+、Br-、C的最高价含氧酸根和A的简单氢化物形成的1:1:1:5的某配合物,向该配合物的溶液中滴加AgNO3溶液产生淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物的化学式为: ;n值为 ;Dn+的基态电子排布式为: 。