-
(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类:Na2CO3__________NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________(填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________(填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________、乙_________________。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________。
高二化学简答题中等难度题查看答案及解析
-
请按照下列要求回答问题:
(1)硫化钠水解的离子方程式:______。
(2)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理______。
(3)将25℃下pH=12的Ba(OH)2溶液a L与pH=1的HCl溶液b L混合,若所得混合液为中性,则a:b=_____。(溶液体积变化忽略不计)。
(4)pH=3的NH4Cl溶液,由水电离出的c(H+)=__。
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留的c(Fe3+)<10-5 mol·L-1),则溶液的pH应大于____。
(6)用如图装置进行模拟电解NO2气体实验,可回收硝酸。
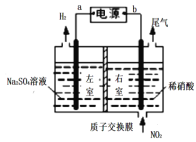
①外接电源a极为_____极,左室发生的电极反应式为_______。
②若有标准状况下2.24 LNO2被吸收,通过质子交换膜(只允许质子通过)的H+为__mol。
(7)在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。

①Ag2CrO4的Ksp为______。
②由Y点变到Z点的方法______。
高二化学综合题中等难度题查看答案及解析
-
按要求完成下列化学反应式
(1)硫酸氢钠在水溶液中的电离方程式 ________ ;
(2)Na2CO3溶液水解的离子方程式 ________ ;
(3)Al2(SO4)3溶液与NaHCO3溶液混合反应的离子方程式 ________ ;
(4)Mg3N2与水反应的化学方程式 ________ ;
高二化学填空题中等难度题查看答案及解析
-
(l4分)(1)①常温下,0.01mol/L的二元酸H2A溶液的pH=5,其电离方程式为________。
②用Al2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
③ 比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa___________NaClO;CuSO4_________KHCO3。(填“>”、“<”或“=”)
(2) 25℃时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
①混合溶液中由水电离出的c(H+)________0.1mol/LNaOH溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合物中下列算式的计算结果(填具体数字):
c(A-)+c(HA)=________mol/L; c(OH-)-c(HA)=________mol/L。
高二化学填空题简单题查看答案及解析
-
完成下列各问题
(1)泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷守恒__________________;②物料守恒______________________;③质子守恒______________________________;④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)______。
高二化学填空题中等难度题查看答案及解析
-
下列与盐的水解有关的是( )
①不能用Al2(SO4)3溶液与Na2S溶液反应制备Al2S3固体
②NaHCO3溶液与Al2(SO4)3溶液可做泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
A.只有①②③ B.只有②③④ C.只有①④⑤ D.①②③④⑤
高二化学单选题中等难度题查看答案及解析
-
泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈现碱性的原因是________(用相关离子方程式表示);灭火器内另一容器中装有
Al2(SO4)3溶液,该溶液呈酸性.当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出CO2和Al(OH)3,阻止火势蔓延,其相关的离子方程式为________.高二化学填空题中等难度题查看答案及解析
-
下列操作中的试剂、方法和对应原理都正确的是
选项
目的
试剂与方法
原理
A
灭火
混合Al2(SO4)3与NaHCO3两种溶液
两物质直接发生化学反应产生CO2
B
制备胆矾
将CuSO4溶液加热直至蒸干
加热促进Cu2+的水解
C
配制AlCl3溶液
AlCl3溶液中加硫酸
抑制Al3+水解
D
除铁锈
NH4Cl溶液
NH4Cl溶液显酸性
高二化学选择题中等难度题查看答案及解析
-
下列操作中的试剂、方法和对应原理都正确的是
选项
目的
试剂与方法
原理
A
灭火
混合Al2(SO4)3与NaHCO3两种溶液
两物质直接发生化学反应产生CO2
B
制备胆矾
将CuSO4溶液加热直至蒸干
加热促进Cu2+的水解
C
配制AlCl3溶液
AlCl3溶液中加硫酸
抑制Al3+水解
D
除铁锈
NH4Cl溶液
NH4Cl溶液显酸性
高二化学单选题中等难度题查看答案及解析
-
(共16分)按要求回答下列问题
(1)用离子方程式解释纯碱溶液去除油污的原因:________
(2)写出泡沫灭火器中反应的离子方程式[内液:Al2(SO4)3 ,外液:NaHCO3]:
________
(3)SOCl2是一种液态化合物,沸点为77℃。向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2 ,可观察到剧烈反应,液面上有白雾生成,并有无色有刺激性气味气体逸出,该气体中含有使品红溶液褪色的SO2,根据实验现象,写出SOCl2与水反应的化学方程式:________
________
蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H20混合并加热,可得到无水AlCl3,解释原因:________
(4)已知:铅蓄电池总的化学方程式为:Pb+PbO2 +2H2SO4
2PbSO4+2H2O
①铅蓄电池在放电时负极反应为________,
②铅蓄电池在充电时阳极反应为;
③如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4________mol。
(5)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):
c(OH-)-c(HA)= ___________ mol/L。
高二化学填空题简单题查看答案及解析