
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学式为C12H16
C.在一定条件下,1mol的始祖鸟烯能与2mol H2发生加成
D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的
高三化学选择题中等难度题

高三化学选择题中等难度题

高三化学选择题中等难度题查看答案及解析
最近科学家公布了新合成的一种烯烃,始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式如图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是

A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=CH3,则其化学式为C12H16
C.若R1=R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种
D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的
高三化学选择题中等难度题查看答案及解析

高三化学选择题中等难度题查看答案及解析
始祖鸟烯(Pterodactyladiene)形状宛如一只展翅飞翔的鸟,其键线式结构表示如下,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )

A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学式为C12H16
C.若R1=R2=甲基,则始祖鸟烯的一氯代物有3种
D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,且两反应的反应类型是相同的
高三化学选择题简单题查看答案及解析
始祖鸟烯(Pterodactyladiene)形状宛如一只展翅飞翔的鸟,其键线式结构表示如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是

A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学式为C12H16
C.若R1=R2=甲基,则始祖鸟烯的一氯代物有3种
D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则两反应的反应类型是相同的
高三化学选择题中等难度题查看答案及解析
始祖鸟烯形状宛如一只展翅飞翔的鸟,其键线式结构表示如图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是

A.始祖鸟烯与CH2===CH-CH===CH2互为同系物
B.若R1=R2=甲基,则其化学式为C12H16
C.若R1=R2=甲基,在一定条件下烯烃双键上的碳原子上的氢也能取代,则始祖鸟烯的一氯代物有3种
D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,且两反应的反应类型是相同的
高三化学单选题中等难度题查看答案及解析
科学家最近在-100 ℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键)。下列说法不正确的是
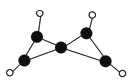
A.X在常温下不能稳定存在
B.X的性质与烯烃类似,容易发生加成反应
C.X不能使酸性KMnO4溶液褪色
D.充分燃烧等质量的X和甲烷,X消耗氧气比甲烷少
高三化学选择题中等难度题查看答案及解析
最近中国科学院上海高等研究院在合成气直接制烯烃研究获重大突破。已知:
反应①:C(s)+1/2O2(g)=CO(g) △H1
反应②:C(s)+H2O(g)=CO(g)+H2(g) △H2
反应③:CO(g)+2H2(g)=CH3OH(g) △H3=-90.1kJ·mol-1
反应④:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H4=-134.0kJ·mol-1
反应⑤:3CH3OH(g)=CH3CH=CH2(g)+3H2O(g) △H5=-31.0kJ·mol-1
下列说法正确的是
A.△H1-△H2<0
B.反应②为放热反应
C.3CH3OCH3(g)=2CH3CH=CH2(g)+3H2O(g) △H=-103.0kJ·mol-1
D.3CO(g)+6H2(g)=CH3CH=CH2(g)+3H2O(g) △H=-301.3kJ·mol-1
高三化学选择题困难题查看答案及解析
CO2的回收与利用是科学家研究的热点课题,可利用CH4与CO2制备“合成气”(CO、H2),还可制备甲醇、二甲醚、低碳烯烃等燃料产品。
I.制合成气
科学家提出制备:“合成气”反应历程分两步:
反应①: CH4(g)⇌C(ads)+2H2(g) (慢反应)
反应②:C(ads)+CO2(g)⇌2CO(g) (快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如下图:
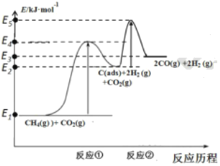
(1) CH4与CO2制备“合成气”的热化学方程式为____。 能量变化图中:E5+E1_______E4+ E2(填“>” 、 “< ” 或 “= ”)。
II.甲醇合成
在某 CO 催化加氢制甲醇的反应体系中,发生的主要反应有:
i. CO2(g) + 3 H2(g)⇌CH3OH(g)+H2O(g)△H1< 0
ii.CO2(g) + H2(g)⇌CO (g)+H2O(g) △H2>0
iii . CO(g)+2H2( g)⇌CH3OH(g) (g) △H3< 0
(2)5MPa 时,往某密闭容器中按投料比n(H2) :n ( CO2) =3:1 充入H2和CO2。反应达到平衡时, 测得各组分的物质的量分数随温度变化的曲线如图所示。
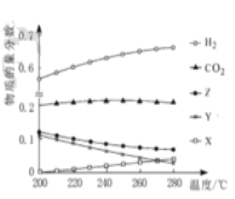
①体系中CO2的物质的量分数受温度的影响不大, 原因是_____。
②250°C时,反应 i i 的平衡常数____1(填“> ”“< ”或“=”)
③下列措施中,无法提高甲醇产率的是____(填标号)。
A.加入适量CO B.增大压强 C.循环利用原料气 D.升高温度
④在下图中画出n(H2)/ n(CO2)随温度变化趋势图_____。
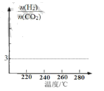
(3)反应i可能的反应历程如下图所示。
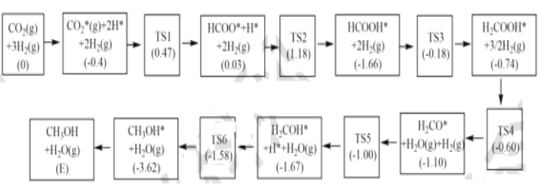
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中TS表示过渡态、*表示吸附在催化剂上的微粒,反应历程中,生成甲醇的决速步骤的反应方程式为__。
高三化学综合题中等难度题查看答案及解析
CO2的回收与利用是科学家研究的热点课题,可利用CH4与CO2制备“合成气”(CO、H2),还可制备甲醇、二甲醚、低碳烯烃等燃料产品。
I.制合成气
科学家提出制备“合成气”反应历程分两步:
反应①:CH4(g)C(ads)+2H2 (g) (慢反应)
反应②:C(ads)+ CO2(g)2CO(g) (快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
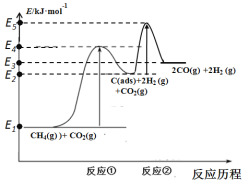
(1)CH4与CO2制备“合成气”的热化学方程式为_________。能量变化图中:E5+E1_________E4+E2(填“>”、“<”或“=”)。
II.脱水制醚
利用“合成气”合成甲醇后,甲醇脱水制得二甲醚的反应为:
2CH3OH(g)CH3OCH3(g) + H2O(g) ΔH,其速率方程式为:v正= k正·c2(CH3OH),v逆=k逆·c(CH3OCH3)·c(H2O),k正、k逆为速率常数且只与温度有关。经查阅资料,上述反应平衡状态下存在计算式:lnKc = −2.205+
(Kc为化学平衡常数;T 为热力学温度,单位为K)。
(2)反应达到平衡后,仅升高温度,k正增大的倍数_________ k逆增大的倍数(填“>”、“<”或“=”)。
(3)某温度下(该反应平衡常数Kc为200),在密闭容器中加入一定量 CH3OH,反应到某时刻测得各组分的物质的量如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 物质的量/mol | 0.4 | 0.4 | 0.4 |
此时正、逆反应速率的大小:v正 ____v逆 (填“>”、 “<”或“=”)。
(4)500K下,在密闭容器中加入一定量甲醇 CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为_________(填标号)。
A < B
C >
D 无法确定
高三化学综合题中等难度题查看答案及解析