A.在0.1mol•L-1的Na2A溶液中,c(A2-)+c(HA-)+2c(Na+)=0.5mol•L-1
B.在0.1mol•L-1的H2A溶液中,c(H+)>0.12mol•L-1
C.分别将同浓度的NaHA和Na2A溶液等体积混合,其pH一定大于7
D.0.1mol•L-1的NaHA溶液中离子浓度为:c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-)
高三化学选择题中等难度题
高三化学选择题中等难度题
高三化学选择题中等难度题查看答案及解析
某二元酸(H2A)在水中的电离方程式为:H2A = H+ + HA- HA- H+ + A2- (Ka=1.0×10-2),下列说法正确的是
A.在0.1 mol·L-1的H2A溶液中,c(H+)> 0.12 mol·L-1
B.在0.1 mol·L-1的Na2A溶液中,c(A2-)+ c(HA-)+ c(Na+)= 0.2 mol·L-1
C.分别将同浓度(0.1 mol·L-1)的NaHA和Na2A溶液等体积混合,其pH一定小于7
D.0.1 mol·L-1的NaHA溶液中离子浓度为:c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-)
高三化学选择题中等难度题查看答案及解析
二元酸H2A在水中的电离情况是:H2A=H++HA-和HA-H++A2-,则下列物质的水溶液中粒子浓度之间存在的关系错误的是
A.NaHA:c(Na+)=c(A2-)+c(HA-)+c(H2A)
B.NaHA:c(Na+)>c(HA-)>c(H+)>c(OH-)
C.Na2A:c(Na+)>c(A2-)>c(OH-)>c(H+)
D.H2A:c(H+)=c(HA-)+2c(A2-)+c(OH-)
高三化学选择题困难题查看答案及解析
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H++HA-,HA-H++A2-
回答下列问题:
(1)Na2A溶液显________(填“酸性”“中性”或“碱性”),用离子方程式表示其原因
__________________________________________________
(2)在0.1 mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是________。
A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HA-)+2c(H2A)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+)
(3)常温下,已知0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中c(H+)可能
______(填“>”、“<”或“=”)0.11 mol·L-1;理由是____________________________
(4)比较①0.1 mol·L-1 Na2A溶液 ②0.1 mol·L-1 Na2SO4溶液,两种溶液中阴离子总浓度的大小①________②(填“>”、“<”或“=”)。
高三化学填空题困难题查看答案及解析
已知二元酸H2A在水中存在以下电离:H2A==H++HA-,HA-H++A2-,回答下列问题:
(1)Na2A溶液呈________性,理由是___________(用离子方程式表示)。
(2)NaHA溶液呈________性,理由是___________。
(3)0.1mol/L的NaHA溶液的PH=3,则Ka(HA-)=_____________。
(4)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至溶液中水的离子积常数Ka=c2(OH-),此时溶液呈___________性,V____________10 (填“<”“>”或“=”)c(K+)/c(Na+) ____________1(填“<”“>”或“=”),溶液中电荷守恒等式为____________。
高三化学填空题困难题查看答案及解析
某二元酸(用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA-H++A2-。回答以下问题:
(1)NaHA溶液________(填“显酸性”、“显碱性”、“显中性”或“酸碱性无法确定”),原因是______________________。
(2)某温度下,向0.1 mol·L-1的NaHA溶液中滴入0.1 mol·L-1 KOH溶液至中性,此时溶液中以下关系一定正确的是________(填字母)。
A.c(H+)·c(OH-)=1×10-14 mol·L-1
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
高三化学填空题中等难度题查看答案及解析
下列说法正确的是
A. 已知二元酸H2A在溶液中的电离方程式为:H2A=H++HA- HA-H++A2-,则NaHA溶液中离子浓度的关系有:c(Na+)=c(A2-)+c(HA-)+c(H2A)和c(A2-)=c(H+)- c(OH-)
B. 已知:室温时Ka(HA)=10-5.则室温时 0.1mol/LNaA溶液的pH约为10
C. HCN溶液加水稀释的过程中c(H+)/c(CN-)减小
D. 向明矾溶液中逐滴滴入Ba(OH)2溶液至硫酸根离子刚好完全沉淀时,所得溶液中离子浓度关系有:c(K+)>c(AlO2-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A====H++HA- HA-H++A2-
完成以下问题:
(1)Na2A溶液显__________________(填“酸性”“中性”或“碱性”),理由是__________________________________________(用离子方程式表示)。
(2)已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度_________0.11 mol·L-1(填“>”“=”或“<”)。
(3)0.1 mol·L-1 Na2A溶液中各种离子浓度由大到小的顺序是:________________________。
高三化学填空题中等难度题查看答案及解析
常温下,0.1mol·L-1的H2A溶液中各种微粒浓度的对数值(lgc)与pH的关系如图所示。
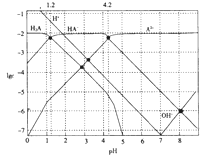
下列说法不正确的是
A. H2A是二元弱酸
B. HA-H++A2-的电离平衡常数Ka=10-12
C. 0.1mol·L-1的H2A溶液中:c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. pH=4.2 时:c(HA-)=c(A2-)>c(H+)>c(H2A)>c(OH-)
高三化学单选题中等难度题查看答案及解析
某二元酸H2A在水溶液中以下列方式进行电离:H2A=H++HA- HA-H++A2-
下列说法正确的是
A.室温时,NaHA溶液pH<7,是由于HA-的电离程度大于其水解程度
B.在0.1 mol/L的Na2A溶液中:c(A2-) + c(HA-) + c(H2A) = 0.1 mol/L
C.在0.1 mol/L的NaHA溶液中,一定有:c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)
D.向两份等体积NaHA、Na2A的浓度比为1 : 1的混合溶液中分别加入适当浓度的盐酸与氢氧化钠,其pH随加入酸、碱量的变化图像为:
高三化学选择题困难题查看答案及解析