-
(1)CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键
C-H
C=C
C-C
H-H
键能(kJ/mol)
414.4
615.3
347.4
435.3
计算该反应的反应热 (写出计算过程)
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(3)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试计算1 mol肼和二氧化氮完全反应时放出的热量为__________________kJ,写出肼与二氧化氮反应的热化学方程式:______________________
高二化学填空题中等难度题查看答案及解析
-
CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
计算该反应的反应热.________kJ/mol.化学键 C-H C=C C-C H-H 键能(kJ/mol) 414.4 615.3 347.4 435.3 高二化学填空题中等难度题查看答案及解析
-
反应CH3—CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键
C-H
C=C
C—C
H—H
键能(kJ/mol)
414.4
615.3
347.4
435.5
则该反应的反应热△H为
A.+288.8kJ/mol B.-703.4kJ/mol C.+125.4 kJ/mol D.-125.4kJ/mol
高二化学选择题中等难度题查看答案及解析
-
已知CH3CH3→CH2=CH2+H2,有关化学键的键能如表所示。则该反应的反应热为
化学键
C-H
C=C
C-C
H-H
键能E/(kJ·mol-1)
414.4
615.3
347.4
435.3
A. +125.6kJ·mol-1 B. -125.6kJ·mol-1
C. +393.5kJ·mol-1 D. -393.5kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
CH3CH3→CH2=CH2+H2的反应热为( )
化学键
C-H
C=C
C-C
H-H
键能kJ/mol
414.4
615.3
347.4
435.3
A.-125.6kJ/mol B.+125.6kJ/mol C.+46.1kJ/mol D.-46.1kJ/mol
高二化学单选题简单题查看答案及解析
-
依据下表判断CH3CH3
CH2=CH2+H2的反应热为
化学键
C-H
C=C
C-C
H-H
键能(kJ·mol-1)
414.4
615.3
347.4
435.3
A.125.6kJ·mol-1 B.-125.6kJ·mol-1
C.46.1kJ·mol-1 D.-46.1kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
有关化学键的键能(指将1mol气态分子拆开形成气态原子时,每个化学键断裂所需的最低能量)数据如表所示:
化学键
C-H
C=C
H-H
C-C
键能/(KJ/mol)
413.4
x
436.0
347.7
已知CH2=CH2(g)+H2(g)
CH3CH3(g) ΔH=-123.5kJ/mol,x的值为
A. 136.8 B. 307.5 C. 615.0 D. 177.3
高二化学单选题中等难度题查看答案及解析
-
乙苯催化脱氢制苯乙烯反应:
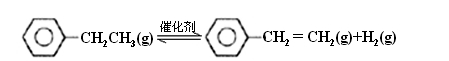
(1)已知:
化学键
C-H
C-C
C=C
H-H
键能/kJ·molˉ1
412
348
612
436
计算上述反应的△H=____________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________ (用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和 水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
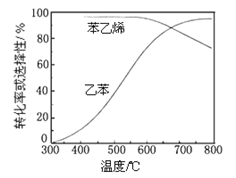
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实______________。
②控制反应温度为600℃的理由是 ____________。
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有__________(填编号)。
① CO2与H2反应,使乙苯脱氢反应的化学平 衡右移
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利于CO2资源利用
高二化学填空题中等难度题查看答案及解析
-
乙苯催化脱氢制苯乙烯反应:

(1)已知:
化学键
C-H
C-C
C=C
H-H
键能/kJ·molˉ1
412
348
612[
436
计算上述反应的△H=____________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=____________(用含α等字母的代数式表示)。
高二化学填空题中等难度题查看答案及解析
-
乙苯催化脱氢制苯乙烯反应:
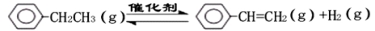
已知:1 mol C-H键完全断裂时吸收热量412kJ,1 mol C-C键完全断裂时吸收热量348kJ
1 mol C=C键完全断裂吸收热量612kJ,1 mol H-H键完全断裂时吸收热量436kJ。
上述反应的△H等于 kJ·mol-1。
A.-124 B.+124 C.-288 D.+288
高二化学选择题中等难度题查看答案及解析