-
反应CH2=CH2+ H2→CH3-CH3,有关化学键的键能如下:
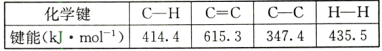
则该反应的反应热△H为
A.+288.8kJ/mo1 B.-703.4 kJ/mo1
C.+125.4kJ/mo1 D.-125.4 kJ/mo1
高二化学选择题中等难度题查看答案及解析
-
(1)CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键
C-H
C=C
C-C
H-H
键能(kJ/mol)
414.4
615.3
347.4
435.3
计算该反应的反应热 (写出计算过程)
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(3)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试计算1 mol肼和二氧化氮完全反应时放出的热量为__________________kJ,写出肼与二氧化氮反应的热化学方程式:______________________
高二化学填空题中等难度题查看答案及解析
-
CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
计算该反应的反应热.________kJ/mol.化学键 C-H C=C C-C H-H 键能(kJ/mol) 414.4 615.3 347.4 435.3 高二化学填空题中等难度题查看答案及解析
-
反应CH3—CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键
C-H
C=C
C—C
H—H
键能(kJ/mol)
414.4
615.3
347.4
435.5
则该反应的反应热△H为
A.+288.8kJ/mol B.-703.4kJ/mol C.+125.4 kJ/mol D.-125.4kJ/mol
高二化学选择题中等难度题查看答案及解析
-
1,3﹣丁二烯和2﹣丁炔分别与氢气反应的热化学方程式如下:CH2=CH﹣CH=CH2 (g)+2H2 (g)→ CH3CH2CH2CH3 (g) ∆H=-236.6kJ/mol CH3﹣C≡C﹣CH3 (g)+2H2 (g)→ CH3CH2CH2CH3 (g) ∆H=-272.7kJ/mol。由此不能判断 ( )
A. 1,3﹣丁二烯和2﹣丁炔稳定性的相对大小
B. 1,3﹣丁二烯和2﹣丁炔分子储存能量的相对高低
C. 1,3﹣丁二烯和2﹣丁炔相互转化的热效应
D. 一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
高二化学单选题中等难度题查看答案及解析
-
已知CH3CH3→CH2=CH2+H2,有关化学键的键能如表所示。则该反应的反应热为
化学键
C-H
C=C
C-C
H-H
键能E/(kJ·mol-1)
414.4
615.3
347.4
435.3
A. +125.6kJ·mol-1 B. -125.6kJ·mol-1
C. +393.5kJ·mol-1 D. -393.5kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH2=CH-CH=CH2(g)+2H2(g)→CH3CH2CH2CH3(g) ΔH=-236.6 kJ·mol-1
CH3-C≡C-CH3(g)+2H2(g)→CH3CH2CH2CH3(g) ΔH=-272.7 kJ·mol-1
由此不能得出的结论是
A. 1,3-丁二烯比2-丁炔更加稳定
B. 1,3-丁二烯转化为2-丁炔为吸热反应
C. 1,3-丁二烯分子比2-丁炔分子储存能量低
D. 一个碳碳三键的键能小于两个碳碳双键的键能之和
高二化学选择题中等难度题查看答案及解析
-
CH3CH3→CH2=CH2+H2的反应热为( )
化学键
C-H
C=C
C-C
H-H
键能kJ/mol
414.4
615.3
347.4
435.3
A.-125.6kJ/mol B.+125.6kJ/mol C.+46.1kJ/mol D.-46.1kJ/mol
高二化学单选题简单题查看答案及解析
-
烃基异构化是当前环保的急切要求,正戊烷异构化为异戊烷的热化学方程式是: CH3CH2CH2CH2CH3
CH3CH(CH3)CH2CH3 △H=-7.1 kJ·mol-1
(1)正戊烷异构化反应选择的温度条件是____________。
(2)由于副反应较为复杂,提髙产率的最佳方法是____________。
(3)如果提高温度,反应速率___________,转化率___________(填“升高"“不变”或“降低” ),同时还会产生积炭现象,假如在反应物中掺入一定量水,则可以减弱这种现象,理由是___________ (用化学方程式表示)。
(4)在573 K时,正戊烧转化率为54%,则此时平衡常数为___________ (保留两位有效数字)。
高二化学选择题困难题查看答案及解析
-
已知通过乙醇制取氢气有如下两条路线:
a.CH3CH2OH(g)+H2O(g)==4H2(g)+2CO(g) △H= +255.6kJ·mol-1
b.CH3CH2OH(g)+1/2O2(g)==3H2(g)+2CO(g) △H= +13.8kJ·mol-1
则下列说法不正确的是
A. 降低温度,可提高b路线中乙醇的转化率
B. 从能量消耗的角度来看,b路线制氢更加有利
C. 乙醇可通过淀粉等生物原料发酵制得,属于可再生资源
D. 由a、b知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ·mol-1
高二化学单选题中等难度题查看答案及解析