-
2017年5月10日中国在南海成功开采出可燃冰,下列有关说法中正确的是
A. 可燃冰是冰的另一种存在形态
B. 可燃冰无毒,可以放心大规摸开采
C. 相比煤、石油,可燃冰属于一种较清沽能源
D. 常温常压下,可燃冰呈固态,可像煤一样开采
高三化学选择题中等难度题查看答案及解析
-
化学与生活、环境密切相关,下列有关说法正确的是
A.我国在南海成功开采的可燃冰
可能会带来酸雨等环境污染
B.大量使用含丙烷、二甲醚等辅助成分的“空气清新剂”,会对环境造成新的污染
C.在人体内酶的作用下,纤维素可以发生水解反应生成葡萄糖
D.我国全面启动的北斗导航系统的信号传输与硅有关
高三化学单选题中等难度题查看答案及解析
-
化学与生活、环境密切相关,下列有关说法正确的是
A. 我国在南海成功开采的可燃冰(CH4∙nH2O)可能会带来酸雨等环境污染
B. 大量使用含丙烷、二甲醚等辅助成分的“空气清新剂”,会对环境造成新的污染
C. 某些筒装水使用的劣质塑料桶常含有乙二醇(HOCH2-CH2OH),乙二醇不溶于水
D. 我国全面启动的北斗导航系统的信号传输与硅有关
高三化学单选题简单题查看答案及解析
-
2017年5月18日国土资源部中国地质调查局宣布,我国正在南海北部神孤海域进行的可燃冰试采获得成功,这也标志着我国成为全球第一个实现了在海域可燃冰试开采中获得连续稳定产气的国家。可燃冰中甲烷含虽为80%~99.9%,甲烷的用途很广,可用来作为燃料及制造氢气、一氧化碳、甲醇等物质的原料。
回答下列问题:
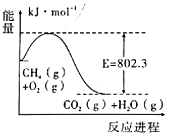
(l)甲烷可用作燃料。右图是lmolCH4在O2充分燃烧生成CO2气体与水蒸气过程中能量变化示意图,已知H2O(l)=H2O(g) △H=+44.0kJ/mol,则1molCH4在O2充分燃烧生成CO2气体与液态水的热化学方程式为_________。
(2)甲烷可以合成甲醇来代替日益供应紧张的燃油。工业上用甲烷为原料制备甲醇分为两个阶段:
① 制备合成气:CH4(g)+H2O(g)
CO(g)+3H2(g)。在恒温恒容的密闭容器中,下列各项能作为判断该反应达到化学平衡状态依据的是______(填标号)。
a.v(CH4)正=3v(H2)逆
b.混合气体的密度不发生变化
c.容器内混合气体的总压强不发生变化
d.混合气体的平均摩尔质且不发生变化
② 合成甲醇:CO(g)+2H2(g)
CH3OH(g)。实验室在恒温(500℃)、恒容(1L)密闭容器中进行模拟合成实验。将lmolCO和2molH2通入容器中,l0min、40min、50min时分别测得容器中甲醇的浓度为0.60mol/L、0.80mol/L、0.80mol/L。则此条件下该反应开始10min内,H2的平均反应速率为_______;平衡常数K的数值为________。
(3)甲烷可以用作如图燃料电池的燃料。
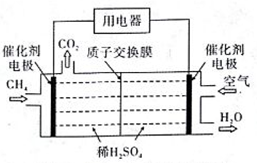
① 负极的电极反应式为_______。
② 常温下,用此电池电解0.5L饱和食盐水(足量),若两极(均为惰性电极)共生成气体l.12L (已折算为标准状况下的体积),则电解后溶液的pH为_______(忽略溶液的体积变化)。
高三化学简答题中等难度题查看答案及解析
-
2017年中国首次海域可燃冰(CH4·nH2O,密度ρ1g·cm-3)试开采成功。若以辛烷代表汽油(密度ρ2g·cm-3)的组成,下列说法不正确的是
①CH4(g) + 2O2(g)=CO2(g)+ 2H2O(l) △H 1=-a kJ·mol-1
②2C8H18(l) + 25O2(g) =16CO2(g) +18H2O(l) △H2 =-bkJ·mol-1
A. 可燃冰适宜保存在低温,高压的环境中
B. 1m3可燃冰可释放出标准状況下[22.4ρ1/(16+18n)]m3的CH4
C. 汽油的燃烧热约为0.5b kJ·mol-1
D. 1m3可燃冰释放出的甲烷燃烧放出的热量约为等体积汽油的 [228aρ1/(16+18n)bρ2]倍
高三化学单选题中等难度题查看答案及解析
-
2017年3月28 日,中国成功开采可燃冰,主要成分为甲烷,属于一次能源。下列不属于 一次能源的是( )
A. 石油 B. 风能 C. 太阳能 D. 氢能
高三化学选择题简单题查看答案及解析
-
2017年3月,中国成功开采可燃冰(主要成分为甲烷)。直接从自然界得到的能源为一次能源,下列不属于一次能源的是
A. 石油 B. 氢能 C. 太阳能 D. 煤
高三化学单选题简单题查看答案及解析
-
(1)2017年5月,我国在南海成功开采“可燃冰”(甲烷水合物),标志着在技术方面取得了突破性进展。甲烷是优质的清洁能源,综合开发利用能有效缓解大气污染问题。
已知:CH4(g)+2O2(g)=CO2(g) +2H2O(g) ΔH =- 802 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH =-566kJ·mol-1
H2O(g)=H2O(l) ΔH =- 44kJ·mol-1
则1mol CH4(g)不完全燃烧生成CO和H2O(l) 的热化学方程式为:________________。
(2)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH>0。
①一定条件下,CH4的平衡转化率与温度、压强的关系如下图1所示。则P1________P2(填“<”、“>”或“=”) ;A、B、C 三点处对应的平衡常数(KA、KB、KC)由大到小的顺序为___________________。
②将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为________________。
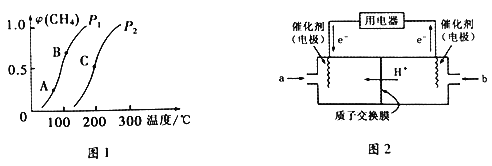
(3)甲烷燃料电池工作原理如上图2所示。a气体是______________,b气体通入电极的反应式为__________。
高三化学填空题困难题查看答案及解析
-
(1)2017年5月,我国在南海成功开采“可燃冰”(甲烷水合物),标志着在技术方面取得了突破性进展。甲烷是优质的清洁能源,综合开发利用能有效缓解大气污染问题。
已知:CH4(g)+2O2(g)=CO2(g) +2H2O(g) ΔH =- 802 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH =-566kJ·mol-1
H2O(g)=H2O(l) ΔH =- 44kJ·mol-1
则1mol CH4(g)不完全燃烧生成CO和H2O(l) 的热化学方程式为:___________________________。
(2)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH>0。
①一定条件下,CH4的平衡转化率与温度、压强的关系如下图1所示。则P1________P2(填“<”、“>”或“=”) ;A、B、C 三点处对应的平衡常数(KA、KB、KC)由大到小的顺序为___________________。
②将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为________________。
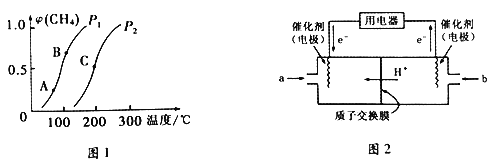
(3)甲烷燃料电池工作原理如上图2所示。a气体是______________,b气体通入电极的反应式为__________。用该燃料电池作电源、以石墨作电极电解硫酸铜溶液,一段时间后,若将0.1mol Cu2(OH)2CO3溶解于该溶液,恰好使溶液恢复至起始成分和浓度,则燃料电池中理论上消耗CH4的体积(标准状况)为_________________。
(4)25℃时,H2CO3的电离常数分别为:Ka1=4.4×10-7mol·L-1;Ka2=5.0×10-11 mol·L-1。在20mL0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液20mL,所得溶液pH=8。此溶液中各阴离子的物质的量浓度大小关系为__________________,
=__________________。
高三化学综合题中等难度题查看答案及解析
-
2017年5月18日,中国国土资源部地质调查局宣布,我国在南海进行的可燃冰试采获得成功,成为全球第一个海域试采可燃冰成功的国家,可燃冰即天然气水合物,甲烷含量占80%至99.9%。化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇或合成氨,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g)=CO(g)+2H2(g) △H1 =-36kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2 =+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,每生产lmolCO,转移电子的数目为__________。
(2)甲醇是一种用途广泛的化工原料,工业上常用下列两种反应制备甲醇:
CO(g)+2H2(g)=CH3OH(g) △H1 =-90kJ·mol-1 K1
CO2(g)+3H2(g)= CH3OH(g)+H2O(l) △H2 K2
己知: CO(g)+H2O(g)= CO2(g)+H2(g) △H3 =-41.1kJ·mol-1 K3
H2O(l)=H2O(g) △H4 =+44.0kJ·mol-1 K4
则△H2=______ K2=_______ (用含K1、K3、K 4的代数式表示)
(3)在一恒温恒容密闭容器中充入1molCO2和3molH2模拟工业合成甲醇的反应:CO2(g)十3H2(g)
CH3OH(g)十H2O(g)
①下列能说明该反应已达到平衡状态的是______________________。
A.混合气体平均相对分子质量不变 B.混合气体密度不变
C.容器内压强恒定不变 D.反应速率满足以下关系:V正(CO2)=3V逆(H2)
E.CO2、H2、CH3OH、H2O物质的量浓度之比为1:3:1:1
F.单位时间内断裂3NAH-H键的同时形成2molH-O键
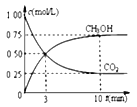
②模拟过程中测得CO2和CH3OH(g)浓度随时间变化如图所示,若此时容器内压强为P,则用平衡分压代替平衡浓度表示的化学平衡常数KP为_____________(用含P的代数式表示,数值保留两位小数),若此时再向容器内充入0.25molCO2和0.25molCH3OH的混合气体,则平衡______(填“正向“逆向“不”)移动。(已知:气体分压=气体总压×体积分数)
(4)甲醇可在电解银催化作用下制甲醛,从贵金属阳极泥中可提取“粗银”“粗银”(含Ag、Cu、Au)可用电解槽电解精炼,纯银作阴极,采用AgNO3和稀HNO3的混合液作电解液,阴极的主要电极反应式为_____。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为_______。硝酸浓度不能过大,其原因是___________________________________________。
高三化学综合题困难题查看答案及解析