-
用如下装置可以完成一系列实验(图中夹持装置已略去)。

请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | | | 褪色 | 浅黄色 |
| 体现SO2的性质 | | | | |
II.若用装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)p中盛装试剂为。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式________。①处包有的某固体物质可能是________。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到________。
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:。
-
用如下装置可以完成一系列实验(图中夹持装置已略去).
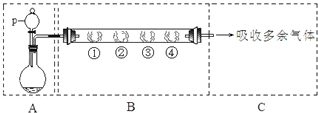
请回答下列问题:
Ⅰ.若装置A中选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
II.若装置A中选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液.请回答下列问题:
(1)写出用浓硫酸和浓盐酸混合制取HCl气体时,有利于HCl气体逸出的原因(写出两点)______,______.
(2)反应开始后,观察到②处棉花变成棕黄色,则①处包有的某固体物质可能是______.
a.MnO2 b.KCl c.KMnO4 d.Cu
写出②处发生反应的离子方程式______.
(3)在实验过程中,在③处能观察到______.
(4)反应较长时间后,②处的棕黄色褪去,产物之一为HIO3(强酸),写出该反应的离子方程式:______.
-
用如下装置可以完成一系列实验(图中夹持装置已略去).
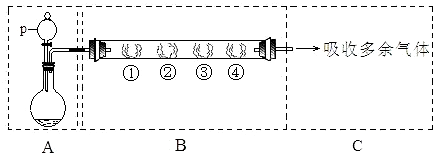
请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | ______ | ______ | ______ | ______ |
II.若用装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液.回答下列问题:
(1)p中盛装试剂为______.
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式______.①处包有的某固体物质可能是______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到______.
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:______.
-
(用如下装置可以完成一系列实验(图中夹持装置已略去)。

请回答下列问题:
Ⅰ.若在装置A中选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中所设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘 水混合液 | 氢硫酸 |
| 现象 | a__________ | b__________ | 褪色 | 浅黄色 |
| 体现SO2的性质 | c__________ | d__________ | e__________ | f__________ |
Ⅱ.若在装置A中选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)P中所盛试剂为__________________。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式__________________;①处包有的某固体物质可能是_____________。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象为__________________。
(4)反应较长时间后,②处棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:_______________。
(5)Ⅰ. Ⅱ两实验中尾气均可采用_________溶液吸收。(填化学式)
-
用如图所示装置可以完成一系列实验(图中夹持装置已略去)

请回答下列问题:
Ⅰ.(1)仪器p的名称是______,若用装置A由浓硫酸和亚硫酸钠固体制取SO2气体,并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
(2)写出③中反应的离子方程式:______.
Ⅱ.若用装置A由浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液.
(1)仪器p中盛装试剂的化学式为______.
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式:______.
①处包有的某固体物质可能是(填序号)______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在实验过程中,在③处能观察到______.
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO-3,写出该反应的离子方程式:______.
-
用如图装置可以完成一系列实验(图中夹持装置已略去):
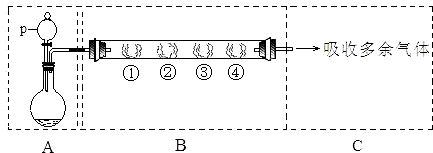
若装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊试液、④蘸有浓NaOH溶液.
(1)p中盛装的试剂为______.
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式:______.①处包有的某固体物质可能是______(填字母).
A.MnO2B.KMnO4C.KCl D.Cu
(3)在整个实验过程中,在③处能观察到的现象为______.
(4)反应较长时间后,②处棕黄色褪去,生成无色的 ,写出该反应的离子方程式:______.
,写出该反应的离子方程式:______.
-
焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂(易被氧化)。实验室利用如图所示装置制取少量焦亚硫 酸钠,并探究 SO2 的性质 (夹持装置已略去)。

请回答下列问题:(实验前已除去装置中的空气)
(1)仪器 a 的名称是_____。
(2)关闭 K2、K3,打开 K1,装置 B 中发生反应的离子方程式为_________,观察到装 置 C 中发生的现象是_____。
(3)装置 D 和 F 的作用是____。
(4)实验前,E 中所用蒸馏水需经煮沸后迅速冷却,目的是_____, 关闭 K1、K3,打开 K2,一段时间后 E 中有 Na2S2O5 晶体析出,装置 E 中发生反应的化学方程式为__________________。
(5)设计实验验证 Na2S2O5 晶体在空气中已被氧化,所需试剂为_____。
(6)在测定某葡萄酒中Na2S2O5 残留量时,取 40.00 mL 葡萄酒样品,加入指示剂,用 0.01000 mol·L−1 的碘标准液滴 定,当溶液_________,即为终点。测定实验中,消耗碘标准液 10.00 mL,该样品中Na2S2O5的残留量为_____g·L−1(以 SO2 计)。
-
实验室用如图装置(略去夹持仪器)制取硫代硫酸钠晶体。

已知:①Na2S2O3.5H2O是无色晶体,易溶于水,难溶于乙醇。
②硫化钠易水解产生有毒气体。
③装置C中反应如下:Na2CO3+SO2=Na2SO3+CO2;2Na2S+3SO2=3S+2Na2SO3;S+Na2SO3 Na2S2O3。
Na2S2O3。
回答下列问题:
(1)装置B的作用是___。
(2)该实验能否用NaOH代替Na2CO3?___(填“能”或“否”)。
(3)配制混合液时,先溶解Na2CO3,后加入Na2S·9H2O,原因是___。
(4)装置C中加热温度不宜高于40℃,其理由是___。
(5)反应后的混合液经过滤、浓缩,再加入乙醇,冷却析出晶体。乙醇的作用是___。
(6)实验中加入m1gNa2S·9H2O和按化学计量的碳酸钠,最终得到m2gNa2S2O3·5H2O晶体。Na2S2O3·5H2O的产率为___(列出计算表达式)。[Mr(Na2S·9H2O)=240,Mr(Na2S2O3·5H2O)=248]
(7)下列措施不能减少副产物Na2SO4产生的是___(填标号)。
A.用煮沸并迅速冷却后的蒸馏水配制相关溶液
B.装置A增加一导管,实验前通人N2片刻
C.先往装置A中滴加硫酸,片刻后往三颈烧瓶中滴加混合液
D.将装置D改为装有碱石灰的干燥管
-
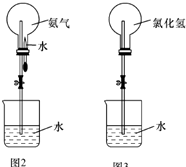
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去).
(1)写出实验室制取氨气的化学方程式:________.
(2)(每空1分)若实验室只有浓硫酸、浓盐酸、浓氨水、氢氧化钠固体、氯化铵固体、氧化钙、无水氯化钙、石蕊试液和如图1所示气体发生装置,你认为他们能制得所需的气体吗?把你的判断填入下表:
| 你的判断 | NH2 | HCl | 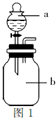 |
| 能够制的 | a中药品:________
b中药品:________ | a中药品:________
b中药品:________ |
| 不能制的 | 原因:________ | 原因:________ |
收集氯化氢气体应该使用________法,要得到干燥的氨气可选用________作干燥剂.
(3)如果用图2装置进行喷泉实验,上部烧瓶已装满干燥氨气,打开止水夹,挤出胶头滴管中的水引水上喷.该实验的原理是________.
(4)如果用图3装置进行喷泉实验,上部烧瓶已装满干燥氨气气体,请说明引发喷泉的方法.________
(5)若至喷泉实验停止时,图2中剩有烧瓶容积1/5的气体;图3烧瓶中剩有烧瓶容积1/4的气体;则图3烧瓶中盐酸的物质的量浓度为________ (两种气体均在标准状况下收集);图2烧瓶中氨水的物质的量浓度________(填“大于”、“小于”、“等于”)图3烧瓶中盐酸的物质的量浓度.
(6)若使上述两种溶液混合后,溶液中铵离子和氯离子浓度相等,应如何操作:________.
-
(14分)某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | | H2O |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | Na2SO3固体、浓H2SO4[来 | SO2 | |
| Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
⑴实验过程中,使用分液漏斗滴加液体的操作是________。
⑵该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?________(填“可行”或“不可行”),原因是________.
⑶实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中,现象是________.发生反应的离子方程式是________.
⑷实验Ⅱ中量气管中的液体最好是____(填字母编号,下同)
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有________.
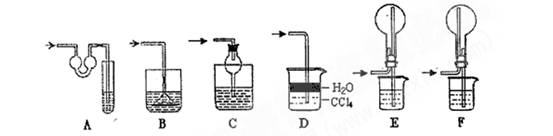
⑸本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②________,③视线与凹液面最低处相平.
⑹实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为____________.










