某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是

A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:CO+O2- ―2e-=CO2
C.当传感器中通过2×10-3mol电子时,说明通过的尾 气中含有2. 24mL CO
D.传感器中通过的电流越大,尾气中CO的含量越高
高三化学选择题中等难度题
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是

A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:CO+O2- ―2e-=CO2
C.当传感器中通过2×10-3mol电子时,说明通过的尾 气中含有2. 24mL CO
D.传感器中通过的电流越大,尾气中CO的含量越高
高三化学选择题中等难度题
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示(上端为多孔电极a,下断为多孔电极b),该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是

A.工作时电极b作正极,O2-由电极b流向电极a
B.工作时电子由电极a通过介质流向电极b
C.负极的电极反应式为:CO+O2—―2e-=CO2
D.传感器中通过的电流越大,尾气中CO的含量越高
高三化学选择题中等难度题查看答案及解析
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是

A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:CO+O2- ―2e-=CO2
C.当传感器中通过2×10-3mol电子时,说明通过的尾 气中含有2. 24mL CO
D.传感器中通过的电流越大,尾气中CO的含量越高
高三化学选择题中等难度题查看答案及解析
CO分析仪以燃料电池为工作原理,用来测量汽车尾气中的CO的含量,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是( )。
A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
高三化学选择题中等难度题查看答案及解析
某固体燃料电池以固体氧化铝——氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a.b均不参与电极反应。下列判断不正确的是

A.在电池内部氧离子(O2-)向负极移动
B.b极对应的电极反应式为:C3H8+10O2-—20e-=3CO2+4H2O
C.该电池的总反应方程式为:C3H8+5O2=3CO2+4H2O
D.用该电池做电源电解CuSO4溶液时,每消耗1molC3H8时理论上能得到Cu的最大量为5mol
高三化学选择题中等难度题查看答案及解析
CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是

A.a 电极发生氧化反应,b电极发生还原反应
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,说明通入的CO越多
高三化学选择题简单题查看答案及解析
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是
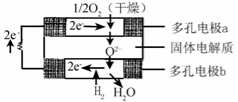
A.有O2参加反应的a极为电池的负极
B.有H2参加反应的b极为电池的正极
C.a极对应的电极反应式为O2 + 2H2O -4e = 4OH-
D.该电池的总反应方程式为:2H2+O2 = 2H2O
高三化学选择题困难题查看答案及解析
(1)汽车尾气是城市空气污染的一个重要因素,一种CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,在高温熔融状态下能传导O2-(过程中无气体产生),则负极的反应式为___。
(2)以上述电池为电源,通过导线连接成图一电解池。
①若X、Y为石墨,a为2L0.1mol/LKCl溶液,写出电解总反应的离子方程式___。
②若X、Y分别为铜、银,a为1L0.2mol/LAgNO3溶液,写出Y电极反应式___。
(3)室温时,按上述(2)①电解一段时间后,取25mL上述电解后的溶液,滴加0.4mol/L醋酸得到图二(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
①结合图二计算,上述电解过程中消耗一氧化碳的质量为___g。
②若图二的B点pH=7,则滴定终点在___区间(填“AB”、“BC”或“CD”)。
高三化学综合题中等难度题查看答案及解析
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
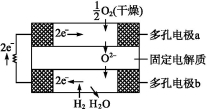
A.有O2放电的a极为电池的负极
B.有H2放电的b极为电池的正极
C.a极对应的电极反应为O2+2H2O+4e-4OH-
D.该电池的总反应方程式为2H2+O22H2O
高三化学选择题中等难度题查看答案及解析
用气体传感器可以检测汽车尾气中CO的含量。传感器是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇−氧化钠,其中O2- 可以在固体介质NASICON中自由移动。下列说法正确的是

A.燃料电池工作时,电极b作负极
B.工作时,电流由负极通过传感器流向正极
C.b电极的电极反应式为:O2+2H2O+4e-=4OH-
D.当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子
高三化学选择题中等难度题查看答案及解析
加强汽车尾气、燃煤企业废气的监测和处理,对于减少雾霾具有重要意义。
(1)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如下图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向_____(填“从a到b”或“从b到a”),负极发生的电极反应式为_______________________。

(2)汽车尾气的主要污染物为NO,用H2催化还原NO可以达到消除污染的目的。
已知:2NO(g)N2(g)+O2(g) △H=﹣180.5kJ•mol﹣1
2H2O(l) = 2H2(g)+O2(g) △H= +571.6kJ•mol﹣1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是_________________________________________________。
(3)上述消除过程中第一步反应起决定作用,某研究小组模拟研究如下:向1L恒容密闭容器中充入a mol NO,其浓度与温度和时间的关系如图所示

①T2下,在0~t1时间内,ν(O2)= mol•L﹣1•min﹣1;反应N2(g)+O2(g) 2NO(g)平衡常数K= (用相关字母表示)。
②该反应进行到M点放出的热量 进行到W点放出的热量 (填”大于” ”小于”或’等于”);M点时再加入一定量NO,平衡后NO的转化率 (填”变大” ”变小”或’不变”)
③反应开始至达到平衡的过程中,容器中下列各项发生变化的是 (填序号).
a.混合气体的密度
b.混合气体的压强
c.逆反应速率
d.单位时间内,N2和NO的消耗量之比
e.气体的平均相对分子质量
(4)工业上用氨水吸收废气中的SO2。已知NH3·H2O的电离平衡常数Kb=1.8×10-5mol·L-1 H2SO3的电离平衡常数Ka1=1.2×10-2mol·L-1 Ka2=1.3×10-8mol·L-1。在通入废气的过程中
①当恰好形成正盐时,溶液中离子浓度的大小关系为______________________________。
②当恰好形成酸式盐时,加入少量NaOH溶液,反应的离子方程式为________________。
高三化学填空题极难题查看答案及解析