镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。实验室模拟海水中提取镁的主要步骤如下:
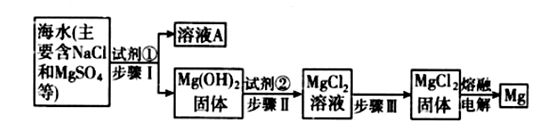
(1) 步骤Ⅰ分离物质需要的主要玻璃仪器有_____________;试剂①是__________(填化学式)。
(2)溶液A中的阴离子主要有______________________。
(3)由MgCl2.6H2O固体得到MgCl2应在什么条件下加热?____________________。
高三化学简答题简单题
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。实验室模拟海水中提取镁的主要步骤如下:

(1) 步骤Ⅰ分离物质需要的主要玻璃仪器有_____________;试剂①是__________(填化学式)。
(2)溶液A中的阴离子主要有______________________。
(3)由MgCl2.6H2O固体得到MgCl2应在什么条件下加热?____________________。
高三化学简答题简单题
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。实验室模拟海水中提取镁的主要步骤如下,下列说法错误的是( )

A. 步骤Ⅰ分离物质需要的主要玻璃仪器有烧杯、漏斗、玻璃棒
B. 溶液A中的阴离子主要有Cl-、SO、OH-
C. 试剂②应选用稀盐酸
D. 步骤Ⅲ可直接加热MgCl2溶液得到MgCl2固体
高三化学选择题中等难度题查看答案及解析
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。实验室模拟海水中提取镁的主要步骤如下:

(1) 步骤Ⅰ分离物质需要的主要玻璃仪器有_____________;试剂①是__________(填化学式)。
(2)溶液A中的阴离子主要有______________________。
(3)由MgCl2.6H2O固体得到MgCl2应在什么条件下加热?____________________。
高三化学简答题简单题查看答案及解析
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
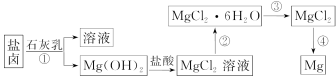
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是___ __ __ __ __ ___。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有__ ___ _溶液(填写化学式)的烧杯中,充分搅拌后经__ _ __ _ __、__ _ __ __ __(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
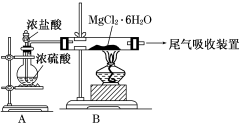
其中装置A的作用是___ ___ __ _ __ __ ___ __ __。
(4)写出过程④中发生反应的化学方程式___ __ __ __ __ ___。
(5)金属Mg在CO2中完全燃烧生成MgO和C,下列说法正确的是___ ___。
A.碳单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒半径:r(Mg2+) > r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
高三化学实验题简单题查看答案及解析
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
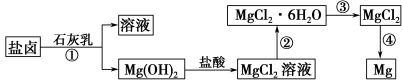
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是 。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有 溶液的烧杯中,充分搅拌后经 、 (填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
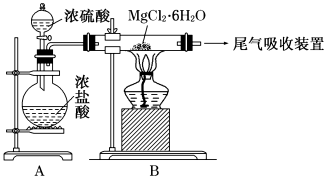
其中装置A的作用是 。
(4)写出过程④中发生反应的化学方程式 。
高三化学填空题中等难度题查看答案及解析
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校研究性学习小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:回答下列问题:
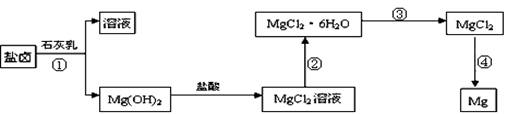
(1)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有________饱和溶液的烧杯中,充分搅拌后经、________(填操作方法)可得纯净的Mg(OH)2。写出有关反应的离子方程式________。
(2)右图是该校研究性学习小组设计进行过程③的实验装置图。其中装置A的作用是。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是。
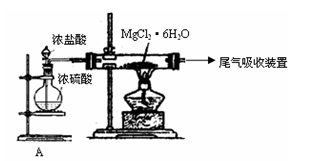
(3)写出过程④中发生反应的化学方程式。该过程得到的镁蒸气需要在特定的循环中冷却,应选用(填试剂名称)作冷却剂。
高三化学填空题中等难度题查看答案及解析
(9分)镁及其合金是一种用途很广的金属材料,海水中镁的含量为1.10 mg·L-1,目前世界上60%的镁是从海水中提取的。主要步骤如下:
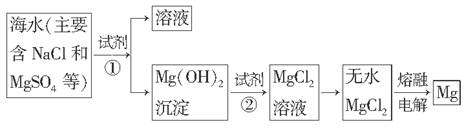
(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用__________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
________________________________________________________________________。
(3)试剂②可以选用________,其反应的离子方程式为_________________________
________________________________________________________________________。
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式________________________________________________________________________
________________________________________________________________________。
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为____mg·L-1,若某工厂每天生产1.00 t镁,则每天需要海水的体积为________L。
高三化学填空中等难度题查看答案及解析
镁及其合金是一种用途很广的金属材料,海水中镁的含量为1.10 mg·L-1,目前世界上60%的镁是从海水中提取的。主要步骤如下:
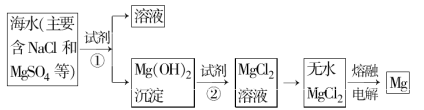
(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②可以选用 ,其反应的离子方程式为 。
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式 。
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为 mg·L-1,若某工厂每天生产1.00 t镁,则每天需要海水的体积为 L。
高三化学填空题中等难度题查看答案及解析
目前世界上60%的镁是从海水中提取的.主要步骤如下:
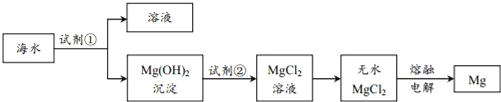
下列说法不正确的是( )
A. 为使海水中的MgSO4转化成Mg(OH)2,试剂①可选择石灰乳
B. 加入试剂①后,分离得到Mg(OH)2沉淀的方法是过滤
C. 加入试剂②反应的离子方程式为:OH﹣+H+=H2O
D. 通过电解熔融的无水MgCl2得到48gMg,共转移4mol电子
高三化学单选题中等难度题查看答案及解析
镁被称为“国防金属”,镁及其合金用途很广,目前世界上60%的镁从海水中提取。从海水中提取镁的流程如下:

请根据上述流程图和镁及化合物的性质回答下列问题:
(1)用贝壳煅烧生石灰的反应方程式:________________
(2)氢氧化镁溶于盐酸的离子方程式为:_____________。
(3)简述,由MgCl2·6H2O制无水MgCl2,加热时通HCl气体的主要原因是:___________。
(4)金属镁属于(填写下列编号):___________。
a.黑色金属 b.有色金属 c.轻金属 d.重金属 e.贵金属
(5)Mg(OH)2煅烧可得熔点很高的MgO,MgO的电子式为:____________。
(6)MgCl2和AlCl3的熔点均较低,加MgO和Al2O3的熔点都很高。为什么冶炼金属镁是电解MgCl2,而冶炼金属铝则电解Al2O3:_______________。
(7)某MgCl2溶液的浓度为0.01mol/L,在该溶液中滴加NaOH溶液至pH=10,此时溶液中的Mg2+是否沉淀完全?_________(填“是”或“否”),此时c(Mg2+)=_________。
(已知:Ksp[Mg(OH)2]=1.8×10-11)
高三化学简答题中等难度题查看答案及解析
世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成石灰乳
②在海水中加入石灰乳,过滤,洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤
④在氯化氢热气流中干燥晶体
⑤电解上述晶体的熔融物。
下列说法正确的是
A.镁元素在元素周期表中位于第4周期、第ⅡA族
B.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
C.在氯化氢热气流中干燥晶体的目的是加快干燥速度
D.步骤⑤也可以采用电解该晶体水溶液的方法
高三化学选择题中等难度题查看答案及解析