-
(12分)N2(g)+3H2(g)  2NH3(g)反应过程的能量变化如下图所示。
2NH3(g)反应过程的能量变化如下图所示。
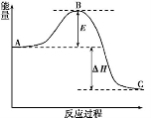
已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示 、 ;若该反应使用催化剂,会使图中B点升高还是降低? 。
(2)图中ΔH= kJ·mol-1。
(3)已知恒容时,该体系中各物质浓度随时间变化的曲线如图所示。
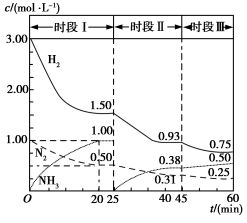
①在0.5 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②45 min时采取的措施是_______________________。
③比较I、II、III时段的化学平衡常数(分别用K1、K2、K3表示)大小________。
-
合成氨反应N2 ( g ) +3H2 ( g ) = 2NH3 ( g ) ,反应过程的能量变化如图所示。已知N2 ( g ) 与 H2( g )反应生成 17 gNH3(g),放出46. 1kJ的热量。请回答下列问题:
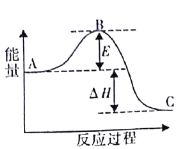
(1)该反应通常用铁作催化剂,加催化剂会使图中E_______________(填“变大”或“变小”) ,E 的大小对该反应的反应热有无影响?___________,理由是__________。
(2)图中△H=________kJ·mol -1。
(3)起始充入2mol·L-1N2和5.5mol·L-1H2,经过50min,NH3的浓度为1mol·L-1,则v(N2)=______mol·L-1·min-1,c(H2)=_____mol·L-1
(4)已知NH3(g)=NH3(l) △H=-QkJ·mol-1,则N2 ( g ) +3H2 ( g ) = 2NH3 ( l )的△H=_______kJ·mol-1
-
(1)化学反应N2+3H2 = 2NH3的能量变化如图所示,该反应的热化学方程式是:N2(g)+3H2(g) = 2NH3(l);⊿H =
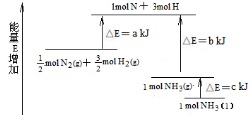
(2)在298K时,1mol C2H6 在氧气中完全燃烧生成CO2和液态水,放出热量1558.3kJ。写出该反应的热化学方程式 。
(3)已知:反应H2(g) + Cl2(g) = 2HCl(g) ΔH= —184 kJ/mol
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH= —115.6 kJ/mol
2Cl2(g)+2H2O(g) ΔH= —115.6 kJ/mol

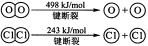
请回答:
H2与O2反应生成气态水的热化学方程式
断开1 mol H—O 键所需能量约为 kJ
-
合成氨反应N2(g)+3H2(g) 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
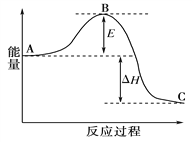
请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变________(填“大”或“小”),E的大小对该反应的反应热有无影响?_______。理由是____________________________;
(2)图中ΔH=______kJ·mol-1;
(3)起始充入2mol·L-1 N2和5.5 mol·L-1 H2 ,经过50 min,NH3的浓度为1mol·L-1,则v(N2)=_________mol·L-1·min-1、c(H2)=___________mol·L-1;
(4)已知NH3(g)=== NH3 (l) ΔH=-QkJ·mol-1,书写N2(g)+3H2(g)===2NH3 (l)的热化学方程式___________________________________。
-
合成氨反应N2(g)+3H2(g) 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
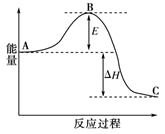
请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变_____(填“大”或“小”),E的大小对该反应的反应热有无影响?__________。理由是_________________;
(2)图中ΔH=________kJ·mol-1;
(3)起始充入2mol·L-1 N2和5.5 mol·L-1 H2 ,经过50 min,NH3的浓度为1mol·L-1,
则v(N2)=____________mol·L-1·min-1、C(H2)=______________mol·L-1;
已知NH3(g)= NH3 (l) ΔH=-QkJ·mol-1,书写N2(g)+3H2(g)=2NH3 (l)的热化学方程式 ________________。
-
(1)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是:N2(g)+3H2(g)=2NH3(l);⊿H= .

(2)在298K时,1mol C2H6 在氧气中完全燃烧生成CO2和液态水,放出热量1558.3kJ。写出该反应的热化学方程式 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2固体和H2O(l)。已知室温下2 g SiH4自燃放出热量89.2 kJ,该反应的热化学方程式为 。
(4)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
(5)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=+64.39 kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196.46 kJ·mol-1
③H2(g)+ O2(g)=H2O(l) ΔH3=-285.84 kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为_________________。
(6).已知:反应H2(g)+Cl2(g)=2HCl(g) ΔH=—184kJ/mol
4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=—115.6kJ/mol
2Cl2(g)+2H2O(g) ΔH=—115.6kJ/mol


请回答:
H2与O2反应生成气态水的热化学方程式
断开1 mol H—O 键所需能量约为 kJ
-
化学反应N2+3H2 2NH3的能量变化如下图所示,该反应的热化学方程式是
2NH3的能量变化如下图所示,该反应的热化学方程式是

A. N2(g)+3H2(g)  2NH3(1) △H=2(a-b-c)kJ·mol-1
2NH3(1) △H=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)  2NH3(g) △H=2(b-a)kJ·mol-1
2NH3(g) △H=2(b-a)kJ·mol-1
C.  N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(1) △H=(b+c-a)kJ·mol-1
NH3(1) △H=(b+c-a)kJ·mol-1
D.  N2(g)+
N2(g)+ H2(g)
H2(g)  NH3(g) △H=(a+b)kJ·mol-1
NH3(g) △H=(a+b)kJ·mol-1
-
3 H2(g) + N2(g)  2NH3(g) 反应过程中的能量变化如下图所示。有关说法错误的是( )
2NH3(g) 反应过程中的能量变化如下图所示。有关说法错误的是( )
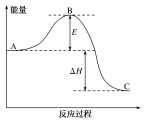
A.图中C表示生成物NH3(g)的总能量
B.断裂3mol 和1mol
和1mol  所吸收的总能量大于形成6mol
所吸收的总能量大于形成6mol  所释放的总能量
所释放的总能量
C.逆反应的活化能
D.3 H2(g) + N2(g)  2NH3(g) △H< 0
2NH3(g) △H< 0
-
化学反应N2+3H2=2NH3的能量变化如下图所示,该反应的热化学方程式是( )

A. N2(g)+3H2(g) === 2NH3(1) △H=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g) === 2NH3(g) △H=2(b-a)kJ·mol-1
C.  N2(g)+
N2(g)+ H2(g) === NH3(1) △H=(b+c-a)kJ·mol-1
H2(g) === NH3(1) △H=(b+c-a)kJ·mol-1
D.  N2(g)+
N2(g)+ H2(g) === NH3(g) △H=(a+b)kJ·mol-1
H2(g) === NH3(g) △H=(a+b)kJ·mol-1
-
已知:3H2(g)+N2(g)⇌2NH3(g)△H=-92kJ/mol,在催化剂存在时反应过程中的能量变化如图所示。下列叙述正确的是
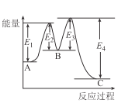
A.△H=E2-E1+E3-E4
B.加入催化剂后反应经过两步完成,其中第一步反应决定总反应速率
C.加入催化剂,△H、反应速率均发生改变
D.向密闭容器中充入3 mol H2和1molN2,发生上述反应,达到平衡时,反应放出92 kJ热量
2NH3(g)反应过程的能量变化如下图所示。














