-
甲醇(CH3OH)是一种优质燃料,
(1)已知一定条件下88gCO2和足量氢气完全反应三可生成气态甲醇(CH3OH)和水蒸汽并放出98kJ的热量.请回答:
①该反应的热化学方程式: .
②若生成3mol甲醇放出的热量为 .
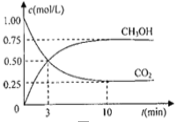
(2)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应,测得CO2和CH3OH(g)的浓度随时间变化如图.请回答:
①从反应开始到平衡,氢气的反应速率:v(H2)= .
②下列措施中能使v(CO2)增大的是 .
A.加入催化剂
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.升高温度
③能够说明该反应已达到平衡的是 .
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3molH2的同时生成1molCH3OH.
E.有2个C=O键断裂的同时,有3个H-H键断裂
-
(17分)甲醇(CH3OH)是一种优质燃料,(1)已知一定条件下每1MolCO2和足量氢气完全反应可生成1Mol气态甲醇(CH3OH)和1Mol 水蒸汽并放出49 kJ的热量。请回答:
①该反应的热化学方程式: 。
②其反应过程中能量的变化与如图所示最相符的是 。
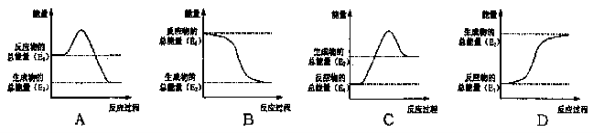
(2)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1MolCO2和3MolH2,一定条件下发生反应,测得CO2和CH3OH(g)的浓度随时间变化如图。
请回答:
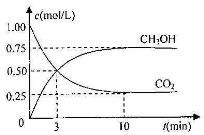
①从反应开始到平衡,甲醇和氢气的反应速率:
v(CH3OH)= 。
v(H2)= 。
②下列措施中能使v (CO2)增大的是 。
A.加入催化剂
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.升高温度
③能够说明该反应已达到平衡的是_________。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3MolH2的同时生成1MolCH3OH
-
开发、使用清洁能源发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g) CH3OH(g) △H= -90.8kJ•mol-1。
CH3OH(g) △H= -90.8kJ•mol-1。
①某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____,以CH3OH表示该过程的反应速率v(CH3OH)=______。
②要提高反应2H2(g)+CO(g)⇌CH3OH(g)中CO的转化率,可以采取的措施是_______。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2 e.加入惰性气体 f.分离出甲醇
(2)①氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是____________。
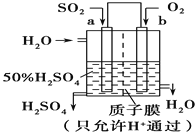
②科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为__________。
-
工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是
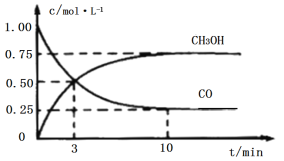
A.反应的化学方程式:CO+2H2⇌CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,ʋ(CO)=0.075mol/(L·min−1)
D.反应至3分钟,用甲醇来表示反应的平均速率为 mol/(L·min−1)
mol/(L·min−1)
-
工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是

A.反应的化学方程式:CO+2H2⇌CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,ʋ(CO)=0.075mol/(L·min−1)
D.反应至3分钟,用甲醇来表示反应的平均速率为 mol/(L·min−1)
mol/(L·min−1)
-
工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是
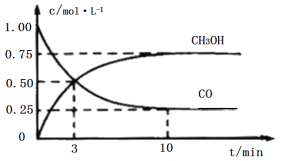
A.反应的化学方程式:CO+2H2⇌CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,ʋ(CO)=0.075mol/(L·min−1)
D.反应至3分钟,用甲醇来表示反应的平均速率为 mol/(L·min−1)
mol/(L·min−1)
-
工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是
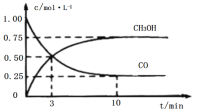
A.反应的化学方程式:CO+2H2⇌CH3OH
B.反应进行至3分钟时,正、逆反应速率相等,反应达到平衡状态
C.反应至10分钟,CO的转化率为75%
D.反应至3分钟,用甲醇来表示反应的平均速率为 mol/(L·min−1)
mol/(L·min−1)
-
工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是
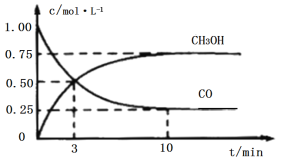
A.反应的化学方程式:CO+2H2⇌CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,ʋ(CO)=0.075mol/(L·min−1)
D.反应至3分钟,用甲醇来表示反应的平均速率为 mol/(L·min−1)
mol/(L·min−1)
-
25℃、101 kPa下,煤炭、氢气、天然气和甲醇(CH3OH)等几种燃料的热值(指一定条件下单位质量的物质完全燃烧所放出的热量)依次是33 kJ·g-1、143 kJ·g-1、56 kJ·g-1、23 kJ·g-1,则下列热化学方程式正确的是
A.C(s)+ O2(g)=CO(g) △H= -396 kJ·mol-1
O2(g)=CO(g) △H= -396 kJ·mol-1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H= -896 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l) △H= -286 kJ·mol-1
D.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H= +736kJ·mol-1
O2(g)=CO2(g)+2H2O(l) △H= +736kJ·mol-1
-
25℃、101 kPa下,煤炭、氢气、天然气和甲醇(CH3OH)等几种燃料的热值(指一定条件下单位质量的物质完全燃烧所放出的热量)依次是33 kJ·g-1、143 kJ·g-1、56 kJ·g-1、23 kJ·g-1,则下列热化学方程式正确的是
A.C(s)+O2(g)=CO(g) △H= -396 kJ·mol-1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H= -896 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l) △H= -286 kJ·mol-1
D.CH3OH(l)+O2(g)=CO2(g)+2H2O (l) △H= +736kJ·mol-1
(l) △H= +736kJ·mol-1








